Koordinative Kettentransfer- Polymerisation KKTP Hauptseminar Anorganische Chemie am 08.06.2010...
-
Upload
rein-boeglin -
Category
Documents
-
view
116 -
download
0
Transcript of Koordinative Kettentransfer- Polymerisation KKTP Hauptseminar Anorganische Chemie am 08.06.2010...

Koordinative Kettentransfer- Polymerisation KKTP
HauptseminarAnorganische Chemie
am 08.06.2010Theresa Neumann

2
Gliederung• Geschichte der PE-Synthese
• Überblick zu verschiedenen Polymerisationsmethoden
• Herausforderungen bei der PE-Synthese
• Mechanismus der KKTP
• Vergleich bekannter Katalysatorsysteme
• Zusammenfassung
• Ausblick
• Literatur

3
Geschichte der PE-Synthese
• 1933 I.C.I. Hochdruckverfahrens1000-2000 bar, 100-300°C,radikalische Substanzpolymerisation
• 1939 großtechnische Produktion von LDPE• 1953 Mülheimer-Normaldruckverfahren
nach Karl ZieglerNormaldruck bis 5 bar, RT bis 90°C
H2C CH2TiCl4 / Et2AlCl
25 °C; 1barPE-HD

4
Geschichte der PE-Synthese
• 1963 Nobelpreis für Chemie an K. Ziegler und G. Natta
• 1990 Metallocen-Katalysatoren1 bar, 25 °C, komplex katalytisch
• 1996 KKTP1 – 5 bar, 80 °C, komplex katalytisch

5
Überblick zu verschiedenen Polymerisationsmethoden
Polymerisationsprozess
Polymerisationsmethode
Reaktions-bedingungen
Struktur PDI = Mw/Mn
I.C.I. Hochdruck-verfahren
Radikalische Polymerisation
1000-2000 bar,100-300 °C,0,05-0,1 % O2 als Initiator
Langkettig, verzweigt:LDPE
Breit
Mülheimer Normaldruck-verfahren
Koordinative Polymerisation
5-10 bar,80-90 °C,TiCl4/AlEt3 als Katalysator
Hohe Kristallinität, unverzweigt linear:HDPE
4 - 8
Metallocen-Katalysatoren
Koordinative Polymerisation
1 bar,25 °C,MAO als Cokatalysator im Überschuss
Hohe Kristallinität, unverzweigt linear
1,5 - 2,5
KKTP Koordinative Polymerisation
1-5 bar,80°C
Hohe Kristallinität, unverzweigt linear
1,3 - 1,05

6
Herausforderungen bei der PE-Synthese
• Enge Molekulargewichtsverteilungen• Steuerung der Kettenverzweigungen• Vermeidung von Kettenabbruchreaktionen:
z.B. ß-H-Eliminierung
– ß-H-Eliminierung: Transfer zum Metall– ß-H-Eliminierung: Transfer zum Monomer
→KKTP: Katalysiertes Kettenwachstum
AlEt
3n+ 3 nC2H4 3 H n
+ AlEt3

7
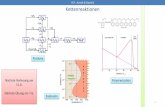
Mechanismus der KKTP
MGM= Hauptgruppenmetall cg = Kettenwachstum M = Nebengruppenmetall ct = Kettentransfer ß = ß-H-Eliminierung

8
Mechanismus der KKTP
Kettenwachstum << Kettentransfer kcg < kct1 ≈ kct2
Kettenabbruch unterdrückt kß < kcg oder kß1 < kß2

9
Sm/Mg- Katalysatorsystem
Erste Polymerisation mit KKTP
• M(L)x: [SmCl2Cp*2Li(OEt2)2]
mit Cp* = Pentamethylcyclopentadienyl
• MGM: Mg als n-Bu-Mg-Et
1996 Mortreux et al.
Mg/Sm Aktivität[g/mmol h bar]
Mn [g/mol]
PDI = Mw/Mn
10 564 1870 1,2
20 396 690 1,3
50 348 400 1,3

10
Fe+/Zn- Katalysatorsystem
• M(L)x: Bis(imino)pyridin Eisen (II)-dichlorid + MAO mit R2 = R3 = R4 = Me• MGM = Zn als ZnEt2
2005 Gibson et al.
Zn/Fe Aktivität[g/mmol h bar]
Mn [g/mol]
PDI = Mw/Mn
440 2000 1000 1,1

11
Y+/Al- Katalysatorsystem
Kationischer Organoyttrium-Katalysator
• M(L)x:
[YAp*(CH2SiMe3)(THF)3]+[B(C6H5)4]-
mit Ap* = Aminopyridinatoligand
• MGM: Alals TIBAO (Tetraisobutylalumoxan)
2006 Kempe et al.

12
Synthese von [YAp*(CH2SiMe3)(THF)3]+[B(C6H5)4]-
mit Ap* = Aminopyridinatoligand, R = CH3, R‘ = C6H5, Ar = C6H5

13
Temperaturabhängigkeit
Reaktionsbedingungen:[YAp*(CH2SiMe3)(THF)3]+[B(C6H5)4]- mit Y/B = 1/1,110 µmol in 260 ml ToluolTIBAO (Tetraisobutylalumoxan) mit Y/Al = 1/205 bar, 15 min

14
Temperaturabhängigkeit

15
Zeitabhängigkeit
[YAp*(CH2SiMe3)(THF)3]+[B(C6H5)4]- mit Y/B = 1/1,110 µmol in 260 ml ToluolTIBAO mit Y/Al = 1/205 bar

16
Zeitabhängigkeit
„heterogene“ WachstumsperiodePolymer-Präzipitation ab 22 min

17
Al/ Y-Verhältnis
Reaktionsbedingungen:[YAp*(CH2SiMe3)(THF)3]+[B(C6H5)4]- mit Y/B = 1/1,110 µmol in 260 ml ToluolTIBAO5 bar, 15 min, 80 °C

18
Al/Y-Verhältnis

19
Vergleich der KatalysatorsystemeVerhältnisMGM/M
Aktivität[kg/mol h]
Mn
[g/mol]T[°C]
t[min]
PDI
Mg/Sm 10 564 1870 80 5 1,2
Mg/Sm 50 348 400 80 5 1,3
Zn/Fe 440 2000 1000 RT 30 1,1
Al/Y 50 376 3940 80 15 1,09
Al/Y 100 168 1460 80 15 1,05
Mit Hilfe des Y+/Al-Katalysatorsystem wird PE mit den höchsten Molekulargewichten und dem niedrigsten PDI erzeugt.

20
Zusammenfassung
KKTP: Hoch effiziente Art PE zu synthetisieren• Poisson-Verteilung: PDI < 1,1• Mw bis zu 4000 g/mol
Möglich durch:• Lineares zeit-abhängiges Kettenwachstum• Sehr schneller, reversibler Kettentransfer• Unterdrückung des ß-H-Eliminierung

21
Ausblick
• Synthese von Olefin-BlockcopolymerenMit Semikristallinen und amorphen Blöcken
→ Flexibilität und Hitzebeständigkeit z.B. INFUSETM (The DOW Chemical Company)
• Einarbeitung von funktionellen oder polaren Gruppen in Polyolefine
• Synthese von UHMWPE (ultrahigh molecular weight PE) mit Mw > 3 • 106 g/mol

22
Vielen Dank für
IhreAufmerksamkeit!

23
Literatur
• K. Ziegler, H.G. Gellert, H. Kühlhorn, H. Martin, K. Meyer, K. Nagel, H. Sauer, K. Zosel, Angew. Chem. 1952, 64, 323-350.
• K. Ziegler, E. Holzkamp, H. Beil, H. Martin, Angew. Chem. 1955, 67, 541-636.
• L.L. Böhm, Angew. Chem. 2003, 115, 5162-5183.
• M. van Meurs, G.J.P. Britovsek, V.C. Gibson, S.A. Cohan, J. Am. Chem. Soc. 2005, 127, 9913-9923.
• R. Kempe, Chem. Eur. J. 2007, 13, 2764-2773.
• W.P. Kretschmer, S. Qayyum, R. Kempe, Chem. Eur. J. 2006, 12, 8969-8978.
• P.D. Hustad, Science 2009, 325, 704-707.
• R. Briquel, J. Mazzolini, T. Le Bris, O. Boyron, F. Boisson, F. Delolme, F. D`Agosto, Ch. Boisson, R. Spitz, Angew. Chem. Int. Ed. 2008, 47, 9311-9313.
• S. Padmanaghan, K.R. Sarma, Sh. Sharma, V. Patel, Macromol. React. Eng. 2009, 3, 257-262.