Struktur und Reaktivität Inhaltsverzeichnis/Gliederung der ... · Ein alter, wenig spezifischer...
Transcript of Struktur und Reaktivität Inhaltsverzeichnis/Gliederung der ... · Ein alter, wenig spezifischer...

Folie 1
• Organische Chemie (Definition)
• Aufbau (Struktur) organischer Verbindungen
• Unterscheidung organischer Verbindungen nach funktionellen Gruppen
• Typische Reaktionen monofunktioneller Verbindungen
• Analyse von Stoffgemischen (Chromatographie)
• Molekülstruktur und Sinneswahrnehmung
Struktur und Reaktivität organischer Verbindungen
Inhaltsverzeichnis/Gliederung der Experimentalvorlesung im Probestudium WS 2002/03 7.11.2002 Prof. Dr. P. Rademacher
Folie 2 Was ist organische Chemie?
F. Wöhler (1800-1882) A.W. v. Hofmann (1818-1892)1828: Harnstoffsynthese Ende der vitalistischen
Theorie (nach 1882)
Zu Beginn des 19. Jahrhunderts:Anorganische Chemie: Chemie der Mineralien und GesteineOrganische Chemie: Chemie des Pflanzen- und Tierreichs (heute: Biochemie)
O CNH2
NH2
NH4+OCN-
Ammoniumcyanat Harnstoff
CH4N2O
Bei seinen Arbeiten mit der Cyansäure versuchte Wöhler, das Ammoniumcyanat herzustellen. Beim Eindampfen einer wässrigen Lösung erhielt er zwar eine Verbindung mit der richtigen Formel, die sich aber als Harnstoff, also einem Isomer mit ganz anderer Struktur, entpuppte. 1828: F. Wöhler, Harnstoffsynthese, Ende der vitalistischen Theorie (nach 1882), propagiert hauptsächlich von A.W. v. Hofmann. Wöhler blieb zeit seines Leben ein Anhänger des Vitalismus. Näheres über Wöhler findet man z. B. im Internet unter: http://www.museum.chemie.uni-goettingen.de/
Folie 3
Es gibt mehr Verbindungen des Kohlenstoffs als aller übrigen Elemente zusammen.
C ist vierbindig; bildet starke kovalente Bindungen,Einfach-, Doppel- und Dreifachbindungen mit
sich selbst und anderen Atomen; Ketten, Ringe und Netze. Die meisten organischen Verbindungen sind
unter normalen Bedingungen stabil.
Definition: „Organische Chemie“
Organische Chemie ist die Chemie der Kohlenstoffverbindungen.
An der Luft sind die meisten organischen Verbindungen thermodynamisch nicht stabil. Die Verbrennung erfolgt jedoch nicht spontan, sondern erfordert eine relativ große Aktivierungsenergie, wie sie erst bei hoher Temperatur zur Verfügung steht. Dem entsprechend sind diese organischen Verbindungen kinetisch stabil. Auch hierin unterscheiden sich die Verbindungen des Kohlenstoff von denen anderer Elemente.

2
Folie 4
GraphitHärte = 1
DiamantHärte = 10
C60 C70 C76
Fullerene
����������������������������
����������������������
������������
����������
C20
Verbindungen, die nur aus Kohlenstoff bestehen
Bilder aus „Grundstock des Wissens“. Graphit leitet den elektrischen Strom, Diamant ist ein elektrischer Isolator. Diamant ist ein guter, Graphit ein schlechter Wärmeleiter. C60 � Fußball, C70 � Baseball.
Folie 5 Einfache organische Verbindungen: Kohlenwasserstoffe
CH3
CH2
CH2
CH2
CH2
CH3
CH2
CH2 CH2
CH2
CH2
CH2
CH2
CH2 CH2
CHCH
CH2
CHCH
CH
CHCH
CH
CH2
CH2
CH3
CH3
n-Hexan, ein Alkan
Cyclohexan, ein Cycloalkan
Cyclohexen, ein Cycloalken
Benzol (Benzen), ein Aromat
3-Hexin, ein Alkin
Kohlenwasserstoffe sind die Stammverbindungen der meisten organischen Verbindungen.
Methan
Adamantan
Im Adamantan sind die C-Atome wie im Diamant angeordnet. Die Struktur polycyclischer Aromaten ist analog zum Graphit.
Folie 6 Organische Verbindungen mit Heteroatomen
Siedepunkt / °C: 80 116 84 185 182Schmelzpunkt / °C: 6 -42 -38 -6 43Wasserlöslichkeit: - + - - +Basizität: - + - + -Azidität: - - - - +
Durch Heteroatome werden die Eigenschaften stark verändert.
N
NH2 OH
S
Benzen C6H6
Pyridin C5H5N
Anilin C6H7N
Phenol C6H6O
Thiophen C4H4S
Heteroatom-haltige Verbindungen sind besonders in der Biochemie wichtig. Die meisten Naturstoffe besitzen Heteroatome, häufig in einer cyclischen Struktur: Heterocyclen, größte Gruppe der organischen Verbindungen. Beispiele: Kohlenhydrate (Zucker, Cellulose), Nucleinsäuren, Alkaloide, Farbstoffe.

3
Folie 7 Die funktionelle Gruppe von Alkoholenund Phenolen
CH3
CH2
CH2
CH2
CH2
CH2
OH OH R OH
OHAr OH
CH
CH
CCH
CH
C OHCH3
R = Alkylrest
OH = Hydroxygruppe
1-Hexanol
Alkanol
Phenol
Ar = Arylrestp-Kresol
Alkohole und Phenole sind Derivate des Wassers, H2O, bei dem ein H-Atom durch einen Alkyl- bzw. Arylrest
ersetzt wurde.
Beispiel für eine funktionelle Gruppe (FG)
Folie 8 Funktionelle GruppenFunktionelle Gruppe Name Stoffklasse
C H
– Alkane (Paraffine)
C C
C,C-Doppelbindung Alkene (Olefine)
C C C,C-Dreifachbindung Alkine
-Hal (F, Cl, Br, I) Halogen- Fluor-, Chlor-, Brom-, Iodkohlenwasserstoffe
-OH Hydroxy- Alkohole, Phenole
-OR Alkoxy- Ether
-SH Thiol- Thiole (Mercaptane)
-NH2 Amino- Amine
Die Tabelle zeigt eine kleine Auswahl wichtiger funktioneller Gruppen. Viele organische Verbindungen besitzen mehr als eine FG. Man unterscheidet: mono-, di-, tri-, ... polyfunktionelle Verbindungen.
Folie 9 Funktionelle GruppenFunktionelle Gruppe Name Stoffklasse
C O
Carbonyl- Aldehyde, Ketone
C NH
Imino- Imine
C OH
O
Carboxyl- Carbonsäuren
C OR
O
Alkoxycarbonyl- Ester
C NH2
O Carboxamid- Amide

4
Folie 10 Reaktion verschiedener Kohlenwasserstoffe mit Brom
Br
Br
Br
Br
+ Br2 + HBrLicht
+ Br2
+ Br2 + HBrFeBr3
Alkan
Alken
Aromat
RadikalischeSubstitution SR
ElektrophileAddition AE
ElektrophileSubstitution SE
Alkane, Alkene und Aromaten unterscheiden sich inihrer Reaktionsweise.
Versuche mit Brom können aus Sicherheitsgründen in der Vorlesung wegen der Giftigkeit des Broms nicht durchgeführt werden. Statt dessen: Versuch Nachweis von Halogen in organischen Verbindungen mit der Beilsteinprobe, Hinweis auf die Spektralanalyse von Atomen
Folie 11 Alkoholtest
C2H5OH CH3CO2 H
K2Cr2O7 Cr2O3Kaliumbichromat Dichromtrioxid
Ethanol Essigsäure
gelb grün
3 C2H5OH + 2 K2Cr2O7 + 2 H2SO4 3 CH3CO2-K+ + 2 Cr2O3 + 2 K2SO4 + 5 H2O
Ethanol kann sogar in geringer Konzentration in der Atemluftnachgewiesen werden (Alcotest-Prüfröhrchen).
Redoxreaktion
Versuch Nachweis von Etnanol mit Alcoteströhrchen Prinzip Oxidation von Ethanol mit Kaliumbichromat. Farbänderung (gelb -> grün). Der Alkohol in der Atemluft besagt wenig über die Blutalkoholkonzentration. Die Formulierung der Redoxreaktionsgleichung ist nicht ganz einfach. Chemie-Studierende lernen so etwas in der Allgemeinen Chemie.
Folie 12
Glucose-Oxidase-Peroxidase-Farbreaktion, selektiver Nachweis von Glucose im Urin
Nachweis von Glucose
O
OH
OH
OH
OH
CH2OH
O
OH
OH
OH
CH2OH
OGlucose-Oxidase
Glucose Gluconolacton
+ O2 + H2O2
Farbstoff(reduziert, farblos)
Farbstoff(oxidiert, gelb-grün)
Peroxidase+ H2O2 + H2O
Redoxreaktion
Versuch Nachweis von Glucose mit Teststreifen von Roche (DIABUR-TEST 5000, Apotheke). Glucose = Traubenzucker = Dextrose Prinzip Die Halbacetalform der Glucose wird durch Glucose-Oxidase zum Lacton oxidiert. Dabei wird ein FAD zu FADH2 reduziert. Das FADH2 reduziert ein O2 zu H2O2. In der Indikatorreaktion wird ein Stoff (z.B. o-Tolidin) mit H2O2 zu einem Farbstoff oxidiert. Störung: Ascorbinsäure (Vitamin C) und andere Stoffe, die sich leichter als o-Tolidin oxidieren lassen. Anwendung Harnzucker-Selbstkontrolle bei Diabetes mellitus (Zuckerkrankheit).

5
Folie 13
Auch polyfunktionelle Verbindungen zeigen charakteristische Reaktionen.
Amylose, ein Polysaccharid,besteht aus Glucose-Molekülen, besitzt helicale Struktur.Iod-Moleküle werden als KI3 in die Kanäle eingelagert.
Iod-Stärke-Reaktion
Versuch Sehr empfindlicher Iod-Nachweis. Indikator in der Iodometrie. Anwendung z. B. in der Trinkwasseranalytik.
Folie 14 Fichtenspanprobe von Furan und Pyrrol
O
NH
Farbreaktion
grün
rot
Furan
Pyrrol
Aromatische Heterocyclen
Viele Verbindungen zeigen charakteristische Reaktionen, mit denen sie leicht zu erkennen sind.
Versuch Ein alter, wenig spezifischer Test auf Furan und Pyrrol. R.R. Runge (1795-1867), Prof. für Chemie, Breslau. Die genaue Struktur der Farbstoffe ist unbekannt. Sie können nicht isoliert werden.
Folie 15 Chromatographie mit Kreide
Die Farbe „Schwarz“ ist ein Gemisch aus vielen verschiedenen Farbstoffen.Eigentlich handelt es sich um Grau.
Trennung der Farbkomponenten von „schwarzem“ Filzstift
Bei der Chromatographie handelt sich um physikalische Trennverfahren, bei denen die Stofftrennung durch Verteilung zwischen einer stationären und einer mobilen Phase geschieht.
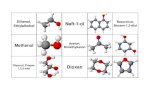
Versuch „Kreidechromatographie“. Einfache Methode zur Auftrennung von Farbstoffgemischen. Ein Stück Tafelkreide dient als stationäre Phase. Als mobile Phase kann im einfachsten Fall Wasser verwendet werden. Mit dieser Methode kann man z. B. zeigen, dass die schwarze Farbe von Kugelschreibern und Filzstiften aus einem Gemisch zahlreicher Farbstoffe besteht, die sich zu grau addieren. Auch die in (grünen) Blättern enthaltenen Farbstoffe (Chlorophyll, Phytochrome, Carotinoide, Anthocyane) lassen sich durch „Kreidechromatographie“ trennen. Eine Verbesserung der Trennung wird erreicht, wenn man statt Wasser ein organisches Lösungsmittel wie Alkohol (Ethanol) oder Aceton verwendet. Im Labor verwendet man die Dünnschichtchromatographie als eine einfache und schnelle Methode zur Analytik

6
von Stoffgemischen.
Folie 16 Hochdruck-Flüssigkeitschromatographie (HPLC)
Pumpe
Elutionsmittel
Proben-aufgabe
Trennsäule
mV - Schreiber Detektor
Signalwandler
Fraktionssammler
bis 40 MPa
Bei der Säulenchromatographiedient Kieselgel in der Trennsäule als stationäre Phase und ein organisches Lösungsmittel („Elutionsmittel“) als mobilePhase.Die HPLC ist eine Fortentwicklung dieser Methode.
Für die instrumentelle Analytik sind die Gaschromatographie (GC) und die Hochdrückflüssigkeitschromatographie (HPLC) Standardmethoden. Die HPLC findet auch in der präparativen organischen Chemie Anwendung.
Folie 17 Gaschromatographie (GC)
Bei der Gaschromatographie dient eine gefüllte dünne Glassäule als stationäre Phase und ein Inertgas (He, N2) als mobile Phase.Die GC ist eine sehr leistungsfähige Methode zur Analyse flüchtiger Substanzgemische. Als Detektor kann auch die menschliche Nase eingesetzt werden.
GC und HPLC lassen sich mit der Massenspektrometrie (MS) koppeln (-> GC/MS, HPLC/MS). Die Massenspektrometrie ist eine sehr empfindliche Methode zum Nachweis und zur Identifizierung von organischen Verbindungen.

7
Folie 18 Gaschromatogramm eines Parfüms
Das Gaschromatogramm zeigt zahlreiche Peaks. Jeder gehört zu einer Komponente.Um welche Verbindung es sich jeweils handelt, kann mit Hilfe derMassenspektrometrie bestimmt werden.
Inte
nsitä
t
Zeit
Folie 19
Foliensammlung des Fonds der Chemischen Industrie: Tenside

8
Folie 20 Molekülstruktur und Sinneswahrnehmung
Rezeptoren
Sensoren für spezifische physiologische Signale (Reize)
Thermo-Rezeptoren: Wärme/KältePhoto-Rezeptoren: Licht, SehenMechano-Rezeptoren: Berührung, Tastsinn
Schall, HörenChemo-Rezeptoren: Geschmack, Geruch
Die Chemie spielt eine entscheidende Rolle beim Sehen (Sehpurpur, Rhodopsin auf der Netzhaut des Auges), Riechen und Schmecken.
Folie 21 Chemilumineszenz von Luminol
Luminol wird zum Nachweis von Blut, Kupfer, Eisen, Cyaniden,Peroxiden und Peroxidasen verwendet.
Oxidation von Luminol in alkalischer wässriger Lösung.Energie wird als Licht abgegeben.
-+
N2
O2 O
O
O
OH2N
Na
Na
-
-
+
+
N
N
O
OH2N
OO
Na
Na
-
-
+
+
N
N
O
OH2N
Na
Na
-
-
+
+
NH
NH
O
OH2N
+ NaOH
- Licht
Versuch Luminol (3-Aminophthalsäurehydrazid), C8H7N3O2. Luminol zeigt bei alkalischer Oxididation mit H2O2 sehr starke Chemilumineszenz. Luminol wird zum Nachweis von Blut, Kupfer, Eisen, Cyaniden, Peroxiden und Peroxidasen verwendet, z. B. in der Kriminalistik. Lit.: Gundermann et al., Chemiluminescence in Organic Chemistry, Berlin: Springer 1987. Quelle: Römpp Lexikon Chemie – Version 2.0, Stuttgart/New York: Georg Thieme Verlag 1999.
Folie 22
Wahrnehmung visueller Reize.Sehprozess
Sehen: Wahrnehmung visueller Reize
RhodopsinMeta-rhodopsin II
1 ms
Intrazellulärraum(Außenglied des Stäbchens)
Licht
GTP
GDP GMP
Hyperpolarisation(sekundäresRezeptorpotential)
cGMP
Phospho-diesterase
EZR
Kanaloffen
Kanalzu
Zell-membran
Scheibchen-membran
Na+Gs - Protein
("Transducin")β
αs
γ
++++
+
+
Auf der Netzhaut befinden sich Photorezeptoren (Stäbchen u. Zapfen).Sie bewirken die Umwandlung von Lichtreizen in elektrische Signale.
Der Sehfarbstoff Rhodopsin entsteht aus dem Protein Opsin und dem Aldehyd 11-cis-Retinal. Das Licht bewirkt eine cis/trans-Isomerisierung.

9
Folie 23 Schmecken und Signalauslösung
ADAPTED FROM DAVID V. SMITH, STEVEN J. ST. JOHN, AND JOHN D. BOUGHTER JR., THE GUSTATORY SYSTEM, IN "NEUROSCIENCE IN MEDICINE," 2ND EDITION, EDITED BY P. M. CONN, HUMANA PRESS, TOWATA, N.J., IN PRESS
Die Geschmacksstoffe bewirken an den spezifischen Rezeptoren eine Veränderung der Ionenkanäle. Durch den Ionenfluss wird ein elektrostatisches Potential aufgebaut, das als Signal über die Nerven an das Gehirn weitergeleitet wird. Der Geschmackssinn ist die bislang am wenigsten verstandene Sinneswahrnehmung. Man unterscheidet beim Schmecken fünf Primärqualitäten, die verschiedenen Rezeptoren auf der Zunge Zugeordnet werden: Bitter, Sauer, Salzig, Süß, Umami
Folie 24 Riechen: Komponenten des olfaktorischen Nervensystems
Richard Axel "Die Entschlüsselung des Riechens" , Spektrum der Wissenschaft, Dezember 1995, 72-78.
Sehr gute Informationen zum Thema Sinnesphysiologie findet man im Internet: Internet: http://sinnesphysiologie.de/
Folie 25 Gerüche und Riechstoffe
Riechstoffe: müssen ausreichende Flüchtigkeit besitzenMolmasse < 300 DUm die Membran der Riechzellen zu durchdringenund einen Geruchsreiz auszulösen, müssen sie gute Fettlöslichkeit und hinreichende Wasserlöslickeit besitzen.Euosmophore: -CH=O, >C=O, -OH, -OR, -CN, -NO2
Kakosmophore: -CH=S, >C=S, -SH, -SR, -NC
Gerüche: Wir können Tausende von Gerüchen wahrnehmen und unterscheiden.
OsmophoreGruppen:
Die osmophoren Gruppen sind funktionelle Gruppen.

10
Folie 26
Schematische Darstellung zur Substratspezifität
Oben: Schlüssel-Schloss-Modell nach E. Fischer (1894)Unten: Anpassungsmodell (induced fit) nach D.E. Koshland (1958)
Schematische Darstellung zur Substratspezifität
Enzym Substrat Enzym - Substrat - Komplex
+
+
+
Folie 27 Molekülstruktur und Sinneswahrnehmung
Vorschläge für die Gestalt von Rezeptoren („Schlössern“) unterschiedlicher Geruchsklassen.Ein Molekül, das in eine dieser Strukturen passt, wirkt wie ein Schlüssel und löst ein Nervensignalaus.
Ein Wirkstoff in einem Rezeptordes Enzyms c-SRc-Kinase
Linkes Bild: P. W. Atkins, Moleküle. Die chemischen Bausteine der Natur, Spektrum, Heidelberg, 1988. S. 136, Abb. 5.13. Rechtes Bild: C & EN, Volume 80, Number 39, pp. 26-28: IMAGE COURTESY OF OLEKSANDR V. BUZKO AT UCSF
Folie 28 Camphrig Moschusartig Blumig Minzig Etherisch/Stechend Faulig
Kugel Ei Tennisschläger Stopfen StabSchwefel-VerbindungenAmine
Primärgerüche und Molekülform
Dieses einfache Modell besitzt begrenzte Gültigkeit.

11
Folie 29
Moschus und Muscon
Moschus und Muscon
R-(–)-Muscon
Moschus, schwarzbraune, gekörnte Masse mit ammoniakalisch-animalischem Geruch. Sekret einer Abdominaldrüse des Moschustiers (Moschus moschiferus), einer kleinen geweihlosen Hirschart, die auf den Hochplateaus Ostasiens (Himalaya, Sibirien) lebt.Muscon, wichtigster Duftstoff des Moschus, ist als Fixateur in der Parfüm-Industrie von großer Bedeutung.
O
CH3
Viele Duft- und Aromastoffe sind Naturprodukte.
Folie 30
R-(–)-Muscon,3-MethylcyclopentadecanonO
Molekülstruktur von Muscon
Folie 31
Exalton, CyclopentadecanonSynthese aus Pentadecandisäuredimethylester durch Acyloinkondensation nach Stoll, Hansley und Prelog (1947)Exalton besitzt nahezu die gleiche Duftnote wie Muscon.
O
OH
OH
O
OH
CO2CH3
CO2CH3
Zn/HCl
1. Na
2. H+
Synthese von Exalton
Die Cyclisierung langkettiger Moleküle zu großen Ringen ist eine schwierige Reaktion, da sich „Kopf“ und „Schwanz“ eines Moleküls treffen müssen. Die Cyclisierung steht in Konkurrenz zur Dimerisierung (Kopf-Kopf- oder Schwanz-Schwanz-Verknüpfung von zwei Molekülen).

12
Folie 32 Massenspektrum einer Parfüm-Komponente
Das Massenspektrum wurde bei der GC/MS-Analyse des Parfüms erhalten. Das Spektrum stimmt wird in einer Datenbank gefunden. Demnach handelt es sich bei dieser Komponente um den Moschus-Ersatzstoff „Exaltolide“.
m/z
Neben den Duftkomponenten des echten Moschus gibt es ca. 1000 Substanzen, die einen Moschus-ähnlichen Geruch haben. Als Moschus-Ersatz sind davon nur etwa 30 von Bedeutung. Da der Naturstoff selten und teuer ist, werden große Mengen der synthetischen Moschusverbindungen hergestellt. Vor allem Nitro-Moschusverbindungen und polycyclische Moschusverbindungen sind relativ einfach und billig herzustellen.
Folie 33 Moschus-Ersatz in einem Parfüm
O
O
O
O
Br
H
- HBr
K2CO3 Oxacyclohexadecan-2-onC15H28O2 (m/z = 240)ExaltolideR
Bei der Reaktion handelt es sich um eine intramolekulare nucleophile Substitution. Das Produkt ist ein cyclischer Ester (Lacton). Isoliert als Naturstoff aus Orient-Tabak: Demole, E.; Enggist, P.; Helv. Chim. Acta 61, 1978, 2318-2327.
Folie 34 Xylolmoschus
1-tert-Butyl-3,5-dimethyl-2,4,6-trinitrobenzol,moschusartig riechendegelbliche Kristalle, Schmp. 114 °C
H3C CH3
NO2
NO2O2N
C(CH3)3
Ähnliche Moschusersatzstoffe sind: 1-tert-Butyl-3,4,5-trimethyl-2,6-trinitrobenzol 4-tert-Butyl-3,5-dinitro-2,6-dimethylacetophenon (wurde im Parfüm ebenfalls nachgewiesen, ist physiologisch und ökologisch bedenklich). Diese und ähnliche Duftstoffe werden bzw. wurden auch in Waschmitteln verwendet. Eine Darstellung der Problematik der Verwendung solcher Stoffe findet man im Internet: http://www.arge-elbe.de/wge/Download/Berichte/Moschus.pdf

13
Folie 35
T. Rawlandson, 1819, Experimentalvorlesung in der Royal Institution, London
Experimentalvorlesung 1819
Der Karikaturist T. R. nahm das gesellschaftliche Flair einer großen öffentlichen Schauvorlesung der Chemie aufs Korn, als er um 1819 eine Veranstaltung der „Royal Institution“ über die Chemie der Gase zeichnete. Aus O. Krätz, 7000 Jahre Chemie, Nikol Verlagsges., Hamburg 1999, S. 221.
Folie 36
Liebigs Analytisches Labor in Giessen
Chemisches Laboratorium um 1840
Justus Liebig, der Namenspatron der Gießener Universität, wirkte in Gießen als Professor der Chemie von 1824 - 1852. Im Jahre 1920 wurde in den Räumen seines ehemaligen Instituts ein Museum eingerichtet. Es zählt zu den sechs wichtigsten Chemie-Museen der Welt und stellt eine historische Stätte erster Ordnung dar, denn hier hat der bedeutendste deutsche Chemiker seine bahnbrechenden Entdeckungen gemacht. http://www.uni-giessen.de/~gi04/
Folie 37
Grundpraktikum Organische Chemie, Universität Essen
Chemisches Laboratorium 2002
Hier werden die Liebigs von morgen ausgebildet.

14
Folie 38 MILESS
Die Folien, mit Erläuterungen, sind im Internet zugänglich:
http://miless.uni-essen.de/
Suche nach: Probestudium
Es handelt sich um eine Datei im pdf-Format.
(Befristet bis 31.12.2002)
http://miless.uni-essen.de/
Folie 39 Geschmacksempfinden
Qualität Substanz Schwelle
Bitter Chininsulfat 0.000008
Nicotin 0.000016
Sauer Salzsäure 0.0009
Zitronensäure 0.0023
Salzig NaCl 0.01
CaCl2 0.01
Süß Saccharose 0.01
Glukose 0.08
Saccharin 0.000023
Das Geschmacksempfinden ist für verschiedene Stoffe unterschiedlich stark ausgeprägt. Da viele Giftstoffe bitter schmecken, ist „bitter“ ein Warnsignal.










![Neue Fluoreszenzfarbstoffe mit Pyrrolo[3,4-c]pyrrol ... · • Da teuere und komplizierte anorganische Halbleiter-Technik durch Spin-Coating bzw. Vapor-Depositon-Verfahren ersetzt](https://static.fdokument.com/doc/165x107/5d63644f88c9938c4f8b8ed3/neue-fluoreszenzfarbstoffe-mit-pyrrolo34-cpyrrol-da-teuere-und-komplizierte.jpg)







![Synthese der Alkaloide Botryllazin B und (4- Hydroxyphenyl ... · PDF filehydroxyphenyl)-1H-imidazol-2-yl]methanon sowie Synthese von ... Pyrrol-Alkaloid Lamellarin (6) 2, das Benzopentathiepin](https://static.fdokument.com/doc/165x107/5a9e543c7f8b9a75458da0c7/synthese-der-alkaloide-botryllazin-b-und-4-hydroxyphenyl-1h-imidazol-2-ylmethanon.jpg)