5.5. Kurstag „Photosynthese“ 5.5.1. Ihre Vorbereitung · Lokalisation verschiedener...
Transcript of 5.5. Kurstag „Photosynthese“ 5.5.1. Ihre Vorbereitung · Lokalisation verschiedener...

M. Schessl & T. Hoppe – Skript zur Übung „Experimente zur allgemeinen Biologie“
Version für das WS 2011/12 Nur zum internen Gebrauch im Praktikum bestimmt! Seite 29
5.5. Kurstag „Photosynthese“
5.5.1. Ihre Vorbereitung
• Recherchieren Sie eine Definition der Photosynthese
Stichworte: Umwandlung, chemische Bindungsenergie, Autotrophe, Primärreaktion, Lichtreaktion,
Sekundärreaktion, Dunkelreaktion
• Welche Edukte braucht die Photosynthese, welches Produkt resultiert?
Stichworte: Nettogleichung, Bruttogleichung
• Was ist die „Hydrolyse des Wassers“?
• Warum setzen wir dem Aquarienwasser NaHCO3 zu?
Versuch 1: Untersuchung der Abhängigkeit der Photosynthese von der Lichtintensität
Material:
• 2 Stative, 1 Kreuzmuffe (nicht drehbar), 1 Bürettenhalter,
• 5-l-Aquarium, NaHCO3 für die Hälfte der Kursgruppen; die andere Hälfte arbeitet mit Leitungswasser
• Zollstock, Küvette (200 ml), Glastrichter, Thermometer, Reagenzglas
• Photosynthese-Lampe 220 V, Schutzbrille.
• Rasierklinge, Pinzette,
• Elodea-Spross,
Versuchsdurchführung:
• Das Aquarium wird mit NaHCO3-angereichertem Wasser (1%) befüllt bzw. Sie lösen die ausgeteilte Menge an
NaHCO3 im Aquarienwasser. Bitte markieren Sie für die nachfolgenden Kursgruppen, ob Sie NaHCO3
zugesetzt haben!
• Ein unverletztes Sprossstück (10 – 14 cm) von Elodea canadensis (Wasserpest) wird am Ende mit einer
entfetteten Rasierklinge (Mit Alkohol reinigen) unter Wasser schräg abgeschnitten und mit diesem Ende nach
oben in den Glastrichter eingebracht und im Aquarium aufgestellt (Abb. 16).
• Die Temperatur dieses Wassers muss konstant
gehalten werden (ständig kontrollieren und
gegebenenfalls Wasser erneuern!).
• Der während der Belichtung abgegebene Sauerstoff
erscheint am Sproßanschnitt in Form vieler kleiner
oder weniger größerer Gasblasen. Diese werden
nach einer Eingewöhnungsphase von 2 Min.
gezählt. Die Dauer, während der gezählt wird, hängt
von der Anzahl der Gasblasen ab und ist jeder
Gruppe überlassen.
Nicht selten kommt es vor, daß der Elodea-Stängel
überhaupt keine Gasblasen hervorbringt, oder diese
unregelmäßig aufsteigen. Dann Experiment
abbrechen und mit neuem Sproßstück beginnen.
• Die erhaltenen Werte sollen auf einen einheitlichen Zeitraum von 1 Minute umgerechnet werde und
tabellarisch an der Tafel notiert werden.
Abb. 16: Schema des Versuchsaufbaus zur Photosynthese

M. Schessl & T. Hoppe – Skript zur Übung „Experimente zur allgemeinen Biologie“
Version für das WS 2011/12 Nur zum internen Gebrauch im Praktikum bestimmt! Seite 30
• Messen Sie die Sauerstoffproduktion in jeweils 5 Minuten mit einem Lampenabstand (von der Pflanze) von 10
cm, 20 cm, 40 cm, 60 cm und 80 cm. Die Photosyntheselampen sind heiß und können implodieren, deshalb:
Schutzbrille aufsetzen, wenn in der Nähe eine Lampe in Betrieb ist!
Auswertung
• Zu diesem Versuch muss ein Protokoll geschrieben werden. Bitte berücksichtigen Sie in diesem Protokoll
auch die Meßwerte einer anderen Arbeitsgruppen Ihres Kurses, die im Gegensatz zu Ihrer Gruppe
NaHCO3 eingesetzt bzw. nicht eingesetzt hat.
• Bitte beantworten Sie in Ihrem Protokoll (je nach Frage in unterschiedlichen Kapiteln) die folgenden
Fragen:
1. Warum wird dem Wasser NaHCO3 zugegeben? (im Methodenteil)
2. Wie hängt die Lichtintensität von der Entfernung ab? (in Einleitung)
3. Wie hängt die Sauerstoffproduktion (Photosyntheserate) von der Lichtintensität ab? (in Einleitung)
4. Wie würde sich die ermittelte Kurve nach beiden Seiten fortsetzen, wenn Sie zusätzliche Abstände
berücksichtigt hätten? (in Diskussion)
5.6. Kurstag: Pflanzliche Gewebe III: Sekundäres Dickenwachstum bei Pflanzen
5.6.1. Ihre Vorbereitung
• Recherchieren Sie das sekundäre Dickenwachstum bei Pflanzen
Stichworte: offen kollaterales Leitbündel, Proto- und Metaxylem, Proto- und Metaphloem, Holz, Bast,
interfasciculäres Kambium, Kambiumzylinder, Markstrahlen,
• Recherchieren Sie die sekundären Abschlussgewebe, z.B. Kork, Periderm,
• Wie verläuft das sekundäre Dickenwachstum in einer Wurzel?
Präparate: Übersichtszeichnungen von Sproßquerschnitten unterschiedlich alter Sprosse von Aristolochia sp.
(Osterluzei)
Material:
• Dauerpräparate (Sprosse unterschiedlichen Alters von Aristolochia sp. in 70% Alkohol)
• Präparation: Rasierklingen, Holundermark, Objektträger, Deckgläser, Pinzetten, Styropor,
• Mikroskop
• 200 ml Becherglas, Pasteur-Pipette,
• alkoholische Phloroglucinlösung, konzentrierte Salzsäure. Phloroglucin-Lösung und konzentrierte Salzsäure
dürfen nicht in die Augen oder auf Schleimhäute gelangen (ätzend!). Wenn die Substanzen auf die Haut
gelangen (Finger), sofort mit Seife abwaschen! Auf Kleidung entstehen durch Salzsäure Löcher. Deshalb
Laborkittel anziehen!
Phloroglucin-HCl darf nicht an Mikroskop-Objektive gelangen! Wenn es doch passiert, muss das Objektiv
einer speziellen Reinigung unterzogen werden, bitte sofort melden!
Durchführung
• analog zu den Schnitten, die im Kurstag „Pflanzl. Gewebe II“ angefertigt wurden.

M. Schessl & T. Hoppe – Skript zur Übung „Experimente zur allgemeinen Biologie“
Version für das WS 2011/12 Nur zum internen Gebrauch im Praktikum bestimmt! Seite 31
Beobachtung 4:
Bei Aristolochia gigantea – eine tropische Liane – liegen im ersten Jahr im jungen Spross offen kollaterale
Leitbündel vor, die über den Sprossquerschnitt ringförmig angeordnet sind (Abb. 2a, unten). Der Terminus „offen“
bezeichnet die Tatsache, dass Xylem und Phloem nicht in direktem Kontakt, sondern durch ein faszikuläres
Kambium getrennt werden. Dieses Kambium bringt sowohl das Xylem als auch das Phloem hervor. Da sich das
faszikuläre Kambium direkt vom Apikalmeristem ableitet, ist es ein primäres Meristem. Die Gewebe, die zwischen
den Leitbündeln liegen, sind die Markstrahlen.
Gegen Ende des ersten Jahres
wird das sekundäre Dicken-
wachstum eingeleitet. Hierbei
entsteht aus dem Markstrahl-
gewebe zwischen den
Leitbündeln ein sekundäres
Meristem, das interfaszikuläre
Kambium. Das faszikuläre und
das interfaszikuläre Kambium
bilden zusammen einen
durchgehenden zusammen-
hängenden Kambiumring. Dieser
Kambiumring gibt nach innen
„Holz“ und nach aussen „Bast“
ab (Abb. 2a, nebenstehend).
Holz und Bast bezeichnen
komplexe Gewebe, die ver-
schiedene Zelltypen enthalten.
Im Gegensatz zur Umgangssprache impliziert der botanische Begriff „Holz“ nicht, dass das Holzgewebe
notwendigerweise „verholzt“, d.h. lignifiziert, ist.
Das Metaphloem besteht aus Siebröhren, Geleitzellen und Parenchym. Außerhalb der Leitbündel befindet sich
ein geschlossener und interzellularenfreier Ring von Sklerenchymfasern, dessen geschichtete Wände verholzt
sind (Sekundärwand). Die Rinde von Aristolochia enthält Chloroplasten und geht nach außen in ein schwach
entwickeltes Kanntenkollenchyn unter der Epidermis über.
4 Aus G. Wanner „Mikroskopisch-Botanisches Praktikum“ (Thieme Verlag 2004).
Phloem; RP = Rindenparenchym; Sk = Sklerenchym; X = Xylem. Aus: G. Wanner „Mikroskopisch-Botanisches Praktikum“ (Thieme Verlag 2004).

M. Schessl & T. Hoppe – Skript zur Übung „Experimente zur allgemeinen Biologie“
Version für das WS 2011/12 Nur zum internen Gebrauch im Praktikum bestimmt! Seite 32
Auswertung
Fertigen Sie je eine Übersichtszeichnung eines sehr jungen Sprosses und eines mehrjährigen Sproßes an. Eine
Übersichtszeichnung meint, daß Sie nicht zellig zeichnen sollen, sondern lediglich die Lage und Ausdehnung der
Gewebe in einem Tortenstück-artigen Ausschnitt aus dem Sprosses zeichnen.
5.7. Kurstag „Mitose“: Beobachten von Mitosestadien bei Zwiebelzellen der Wurzelspitze
5.7.1. Ihre Vorbereitung
• Informieren Sie sich über den Mechanismus, den zeitlichen Ablauf und den Zweck der Mitose.
Stichworte: Doppelhelix, Transportform, Tochterzellen, diploide Zelle, Chromatin, Chromatiden, Abbau der
Kernhülle, Spindelfaserapparat, Nucleoli, Äquatorialebene , Chromosomenkondensation, Karyogramm,
Schwesterchromatiden, Tochterchromosome,
• Was passiert in den Mitosephasen Prophase, Metaphase, Anaphase, Telophase, Cytokinsese, Zellplatte,
Mittellamelle, Primärwand, Sekundärwand
Präparat 7: Mikroskopische Untersuchung verschiedener Mitosestadien
Material:
• Etwa 2 cm lange Wurzeln von Allium cepa (Küchenzwiebel) als Frischmaterial,
• Mikroskop, Wasserbad (98°C)
• Präparierbesteck (Rasierklinge, Präpariernadel, Pinzette)
• Objektträger, Deckgläschen, Pasteur-Pipette,
• 50 % Essigsäure, Karmin-Essigsäure,
• Blockschälchen, Reagenzgläser, Alufolie,
• Tafel mit Mikrophotos (mikroskopische Aufnahmen) verschiedener Mitosestadien.
Präparation:
Zwei Zentimeter der Zwiebelwurzeln werden in einem kleinen Reagenzglas in Karmin-Essigsäure im Wasserbad bei
98 °C ca. 15 Minuten „gekocht“. Achten Sie darauf, dass Sie beim Öffnen des Wasserbades das Gesicht seitlich
wegdrehen, da eine Dampfwolke von fast 100 °C entsteht! Verbrühungsgefahr! Bei Verbrühung sofort mit kaltem
Wasser kühlen und Hilfe herbeiholen. Karminessigsäure darf nicht in die Augen geraten: benutzen Sie Ihre
Schutzbrille!
Die Wurzeln werden anschließend in ein Blockschälchen gegossen, die Karmin-Essigsäure abpipettiert (kann
wiederverwendet werden) und die Wurzeln mit 50 % Essigsäure übergossen (ist farblos!). Anschließend legt man
die Wurzeln auf einen Objektträger in 50 % Essigsäure und schneidet davon etwa 2 mm lange Spitzen ab und
entfernt den Rest. Es ist dabei darauf zu achten, dass es sich tatsächlich um die Wurzelspitzen handelt. Das
Präparat wird mit einem Deckgläschen abgedeckt. Dann drückt man mit der Spitze einer Präpariernadel vorsichtig
auf das Deckgläschen, so dass die Wurzelspitzen auseinanderfließen. Das Deckgläschen darf dabei nicht seitlich
verschoben werden.

M. Schessl & T. Hoppe – Skript zur Übung „Experimente zur allgemeinen Biologie“
Version für das WS 2011/12 Nur zum internen Gebrauch im Praktikum bestimmt! Seite 33
Wenn das Objekt auszutrocknen droht, muss an den Rand des Deckgläschens 50 % Essigsäure zugegeben
werden. Kein Wasser zugeben! Die mikroskopische Untersuchung kann sogleich erfolgen. Zur Erinnerung: Karmin-
Essigsäure und Essigsäure beschädigen u.a. Mikroskop-Objektive: Das Deckgläschen muss auf der Oberseite
trocken sein!
Mikroskopieren
Bei den bislang von Ihnen eingesetzten Objektiven verblieb zwischen der Austrittslinse des Objektivs (seiner
„Unterseite“) und dem Deckgläschen Ihres Präparates immer ein schmaler Spalt, der sozusagen „mit Luft gefüllt“
war.
Aufgabe:
Zeichnen und beschriften Sie die oben beschriebenen Kernteilungsstadien, mit 400-facher Vergrößerung, ggf. mit
Ölimmersion bei 1000x Vergrößerung (dann aber nicht Reinigung des Objektivs mit Pentan vergessen!). Nur das
Objektiv, auf dem „oil“ steht, ist für die Benutzung mit Ölimmersion ausgelegt. Alle anderen Objektive sind so
konstruiert, dass mit Luft als Medium zwischen Austritt Objektiv und Oberseite Deckgläschen
Beobachtungen:
In der Regel findet man in einem Präparat alle Stadien der Mitose. Die in großer Zahl vorhandenen
Interphasekerne lassen das rot angefärbte "Kerngerüst" erkennen. Wie wir heute wissen, handelt es sich hierbei
um die langgestreckten Chromosomen, die im Kernraum zusammengeknäult sind und scheinbar wirr
durcheinander liegen. Im ersten Abschnitt der Kernteilung, der Prophase, erfährt das Kerngerüst eine allmähliche
Auflockerung. Infolge der schraubigen Aufrollung ihrer Längselemente treten die Chromosomen als Individuen
immer deutlicher hervor, da sie sich zunehmend verkürzen.
Bei genauerer Betrachtung erkennt man, dass sie der Länge nach in je zwei Chromatiden gespalten sind. Den
stärksten Grad der Verkürzung erreichen die Chromosomen in der Metaphase. Sie sind hier in der sogenannten
Äquatorialplatte angeordnet, und die Kernspindel, die bei dem gewählten Präparationsverfahren schlecht zu sehen
ist, ist fertig ausgebildet. In der Anaphase weichen die beiden Chromatiden der Chromosomen auseinander und
wandern zu den Spindelpolen, so dass jede Tochterzelle die gleiche Anzahl Chromosomen erhält wie die
Mutterzelle. Schon während des Auseinanderweichens der Chromosomen wird die Zellplatte in der Mitte des
Phragmoplasten angelegt. Sie erhält schließlich Anschluss an die Seitenwände und trennt als neue Querwand die
beiden Tochterzellen voneinander. Im letzten Abschnitt der Kernteilung, der Telophase, strecken sich die
Chromosomen wieder und gehen in die bereits beschriebene Form des Interphasekerns über, der sich durch eine
Kernhülle vom Cytoplasma abgrenzt. Auch die Nucleoli werden neu gebildet.

M. Schessl & T. Hoppe – Skript zur Übung „Experimente zur allgemeinen Biologie“
Version für das WS 2011/12 Nur zum internen Gebrauch im Praktikum bestimmt! Seite 34
5.8. Kurstag „Tierische Gewebe“
5.8.1. Ihre Vorbereitung
• Informieren Sie sich über die Charakteristika der vier hauptsächlichen Gewebetypen der Säugetiere
• Epithelgewebe (Abb.: Hautausschnitt mit Epidermis, Schweiß- (1) und Talgdrüsen (2)).
• Binde- und Stützgewebe (Abb.: lockeres Bindegewebe).
• Muskelgewebe (Abb.: Herzmuskulatur).
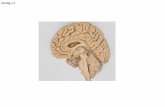
• Nervengewebe (Abb.: Ausschnitt aus der grauen Substanz des Großhirns).
5.8.2. Lokalisation verschiedener Oberflächenepithelien.
Alle nachfolgenden Abbildungsbezüge beziehen sich auf die Zeichnungen in Tafel 2., die - ohne Anspruch auf Vollständigkeit zu erheben - eine
Vorstellung von der Verteilung der Deckepithelien im Organismus gibt.
• Die einschichtigen Plattenepithelien (A) kleiden in erster Linie das Herzinnere, alle Gefäße, Körperhöhlen
(Pleura, Peritoneum) usw. aus.
Tafel 1: Vier Gewebegruppen. aus KRSTIC: "Die Gewebe
des Menschen und der Säugetiere" aus dem Springer-Verlag
entnommen.
Tafel 2: Die verschiedenen Typen von Epithelgewebe. aus
KRSTIC: "Die Gewebe des Menschen und der Säugetiere".

M. Schessl & T. Hoppe – Skript zur Übung „Experimente zur allgemeinen Biologie“
Version für das WS 2011/12 Nur zum internen Gebrauch im Praktikum bestimmt! Seite 35
• Das einschichtige kubische Epithel (B) ist weit weniger verbreitet. Es kommt in verschiedenen Abschnitten
der Nierenkanälchen, im Plexus chorioideus, Pigmentepithel der Netzhaut usw. vor.
• Das einschichtige hochprismatische Epithel mit Kinocilien (C1) findet man in Eileiter und Uterus), vom
Mageneingang bis zum Anus als Auskleidung des Darmrohres (C2), in großen Sammelrohren, in den Ductus
papillares der Niere usw. (C3).
• Im Nebenhodengang und im Ductus deferens gibt es das zweireihige hochprismatische Epithel mit und ohne
Stereocilien (D1, D2), während ein mehrreihiges Epithel mit Kinocilien - das Flimmerepithel (E) - in den
Luftwegen (Nasenhöhle, Trachea, Bronchialbaum) verbreitet ist.
• Für die Harnwege (Nierenbecken, Harnleiter, Harnblase, Anfangsabschnitt der Harnröhre) ist das
Übergangsepithel (F) spezifisch.
• Das mehrschichtige hochprismatische Epithel (G) kommt selten vor: man findet es hauptsächlich an den
Übergängen von geschichtetem Plattenepithel in mehrreihigem prismatischem Epithel (Gaumen,
Kehlkopfdeckel, Fornix conjunctivae) und in einem Teil der Harnröhre.
• An mechanisch stärker beanspruchten Stellen, wie Mundhöhle, Speiseröhre, Anus und Vagina sowie als
vorderes Hornhautepithel usw. findet man das unverhornte geschichtete Plattenepithel (H), das ständig
durch Drüsensekretion befeuchtet werden muss.
• Schließlich ist das verhornte geschichtete Plattenepithel als Epidermis (I) ein Bestandteil der Haut. Dieses
Epithel schützt den Organismus vor physikalischen und chemischen Beschädigungen und bewahrt ihn vor
Austrocknung.
Tafel 4: Typen und Lokalisation der Muskelgewebe. aus KRSTIC: "Die Gewebe des Menschen und der Säugetiere".
Tafel 3: Nervengewebe.

M. Schessl & T. Hoppe – Skript zur Übung „Experimente zur allgemeinen Biologie“
Version für das WS 2011/12 Nur zum internen Gebrauch im Praktikum bestimmt! Seite 36
Präparat 8 a-i: Mikroskopie verschiedener Gewebe
Material:
• Mikroskop, LIEDER-Folien, Histologie.
• Fertigpräparate von:
a) Handfläche quer, Dickdarm quer, Dünndarm quer,
b) Bindegewebe, Knorpel, Knochen,quergestreifte Muskulatur,
c) längsgestreifte Muskulatur,glatte Muskulatur
Tafel 5: Übersicht über die Gewebstypen des Binde- und Stützgewebes. aus KRSTIC: "Die Gewebe des Menschen und der Säugetiere".

M. Schessl & T. Hoppe – Skript zur Übung „Experimente zur allgemeinen Biologie“
Version für das WS 2011/12 Nur zum internen Gebrauch im Praktikum bestimmt! Seite 37
Aufgabe:
• Mikroskopieren Sie die vorliegenden Fertigpräparate, stellen Sie Skizzen her (mit Beschriftung!)
Was für Gewebe haben Pflanzen und Tiere? Tabelle bitte ausfüllen!
Tab. 1: Vergleich zwischen pflanzlichen und tierischen Gewebegruppen
Pflanzliche Gewebegruppen Tierische Gewebegruppen
5.9. Kurstag „Ernährung“
5.9.1. Ihre Vorbereitung
• Suchen Sie eine konsistente Definition von Ernährung; bei welchen Organismen kommt Ernährung vor?
Stichworte: Urphänomen des Lebens; autotroph, heterotroph
• In welche drei Gruppen kann man die Nährstoffe zusammenfassen? Wie werden diese den
Sotoffwechselformen :Energiestoffwechsel, Speicherstoffe, Aufbaustoffwechsel zugeordnet?
• Informieren Sie sich über essentielle Bestandteile der Nahrung
Stichworte: Wasser, Vitamine, Ballaststoffe, Mineralstoffe, Spurenelemente
•
Versuch 2: Nachweis von Zucker und Stärke
Material:
• Haferflocken, Milch, Kartoffel, Wurst, Limonade, Scheibenkäse, hartes Ei, und von Ihnen mitgebrachte
Lebensmittel nach Wahl
• Lugol´sche Lösung,
• Fehling I und II,
• dest. Wasser,
• Kartoffelreibe, Seihtuch,
• Spatel, Reagenzglasständer, Reagenzgläser, Reagenzglashalter, Alufolie, Bunsenbrenner, Schutzbrille.

M. Schessl & T. Hoppe – Skript zur Übung „Experimente zur allgemeinen Biologie“
Version für das WS 2011/12 Nur zum internen Gebrauch im Praktikum bestimmt! Seite 38
Versuchsdurchführung:
• Eine Spatelspitze der zu untersuchenden Lebensmittel (Kartoffelsaft: Kartoffel wird gerieben und abgeseiht,
Wurst und Käse zerdrückt) wird in je zwei Reagenzgläser praktiziert und die trockenen Materialien mit 3-4 cm
destilliertem Wasser überschichtet.
• a) Stärkenachweis: Je eine Probe wird mit einem Spritzer Lugol´scher Lösung versehen und geschüttelt.
• b) Zuckernachweis: Die andere Probe wird mit einem Spritzer Fehling I und II versetzt, mit etwas Alufolie
abgedeckt und unter lockerem Schütteln über der Bunsenbrennerflamme einmal kurz aufgekocht.
Ein Laborspruch sagt: „Wenn Sie lange genug kochen, wird jede Probe positiv“. Was steckt hinter diesem
Spruch?
Die Fehling-Probe ist nur positiv, wenn ein rötlicher-rostbrauner Niederschlag ausfällt. Manchmal ist dieser
sehr schwer zu sehen. Im Zweifelsfall sollten Sie das Reagenzglas vorsichtig dekantieren und nachschauen, ob
Sie winzige rostrote Körnchen entdecken können.
Der von H. Fehling 1848 publizierte Test wurde vor allem zur Blutzuckerbestimmung im Harn bei Verdacht auf
Zuckerkrankheit angewandt und ersetzte die wenig beliebte Geschmacksprüfung des Urins!
• Fehling I ist umweltgefährlich und darf nicht in das Abwasser gelangen: es muss als gefährlicher Abfall
entsorgt werden.
• Das in der Fehling II enthaltene Natriumhydroxid (Natronlauge) verursacht schwere Verätzungen (R35);
Fehling II darf weder eingeatmet noch verschluckt werden und muss ebenfalls als Sondermüll entsorgt
werden.
• Bei diesem Versuch besteht die konkrete Gefahr von Siedeverzügen! Deshalb decken wir die Reagenzgläser
mit Alufolie ab. Aber auch so kommt es regelmäßig zu Siedeverzügen, bei denen die Alufolie schon mehrere
Meter weit geschleudert wurde: halten Sie die „Mündung“ Ihres Reagenzglases nicht auf Kollegen im Labor,
achten Sie darauf, daß um das Reagenzglas keine Gegenstände liegen (Mäppchen, Schals, Hefte), die durch
heiße Fehling-Lösung leiden würden. Setzen Sie unbedingt Ihre Schutzbrille auf!
• Die Gaszufuhr der Bunsenbrenner sollte bei Nichtgebrauch abgestellt werden.
• Tragen Sie die Ergebnisse in die unten stehende Tabelle 1 ein!
• Interpretieren Sie die Ergebnisse der verschiedenen Proben!
Versuch 3: Nachweis von Fetten
Material:
• Lebensmittel wie in Versuch 7.2.1,
• Schreibpapier, Fön.
Versuchsdurchführung:
• Etwas von den Proben wird auf ein Stück Papier aufgerieben bzw. getropft und anschließend getrocknet.
• Tragen Sie die Ergebnisse in die unten stehende Tabelle 1 ein!
Versuch 4: Nachweis von Eiweißen
Der Eiweißnachweis ist etwas problematisch. Exakt lässt er sich nur mit hoch quecksilberhaltigen Reagenzien
durchführen. Eine andere, nicht so exakte Methode ist eine Gelbfärbung durch konzentrierte Salpetersäure, die
nur unter dem Abzug durchgeführt werden kann. Aus diesem Grund, und da Sie für diese Übung sowieso viel Zeit
benötigen, wird auf eine generelle Durchführung von Eiweißnachweisen verzichten. Im Abzug soll einmal für alle
gezeigt werden, wie konzentrierte Salpetersäure auf verschiedene Nahrungsmittel wirkt.

M. Schessl & T. Hoppe – Skript zur Übung „Experimente zur allgemeinen Biologie“
Version für das WS 2011/12 Nur zum internen Gebrauch im Praktikum bestimmt! Seite 39
Rauchende Salpetersäure ist stark ätzend.
Deshalb verwenden wir sie nur zur Demonstration unter dem Abzug. Nicht berühren!
Tab. 2 Ergebnistabelle für die Versuche 4-6
Lugol-Probe Fehling-Probe Fettfleckprobe Salpetersäure
Färbung
Ergeb-
nis
(+/-)
Färbung
Rötl.
Nieder-
schlag
(j/n)
Ergeb-
nis
(+/-)
Intensität
Ergeb-
nis
(++/+/-)
Gelb-
färbung
Ergeb-
nis
(+/-)
Haferflocken
Milch
Kartoffel
(roh)
Wurst
Limonade
Käse
Hart
gekochtes Ei
Rohes Ei

M. Schessl & T. Hoppe – Skript zur Übung „Experimente zur allgemeinen Biologie“
Version für das WS 2011/12 Nur zum internen Gebrauch im Praktikum bestimmt! Seite 40
5.10. Kurstag „Verdauung“
5.10.1. Ihre Vorbereitung
• Formulieren Sie eine gute Definition der Verdauung
• Welche Enzyme sind für die Verdauung der Hauptnährstoffgruppen zuständig?
• Komplettieren Sie die Tab. 3
Tab. 3: Elemente der Verdauung: Mechanik, Anatomie und Chemie
Mechanik Anatomie
(wo findet „Mechanik statt“?)
Chemie
(was findet hier statt“?)
Kauen
Schlucken
Speicherung
Entleerung
Durchknetung und Resorption
Defäkation
Versuch 5: Die Kohlenhydratverdauung mit Hilfe von Speichel
Material:
• Wasserbad ca. 36° C,
• Haferflocken,
• Lugol´sche Lösung, Fehling´sche Lösung I und II, Phosphatpuffer pH 7,
• Reagenzgläser, Reagenzglasständer, Reagenzglashalter,
• Trichter, Filtrierpapier, Messpipette 10 ml, Becherglas, Peleusball
Durchführung:
• Stellen Sie die Versuchsansätze nach der folgenden Tabelle 4 zusammen. Beachten Sie, dass alle Ansätze nach
dem Zusammengeben gut geschüttelt werden müssen.
• Spülen Sie den Mund zunächst sorgfältig aus, damit keine Glucosereste in Ihrem Speichel verbleiben.
• Stellen Sie nun eine Speichellösung her, indem Sie mit 10 ml Wasser den Mund ausspülen.
• Die Spüllösung spucken Sie dann in ein Becherglas und erhöhen die Konzentration durch weiteren
Speichelzusatz.
• Beschriften Sie die Ansätze!

M. Schessl & T. Hoppe – Skript zur Übung „Experimente zur allgemeinen Biologie“
Version für das WS 2011/12 Nur zum internen Gebrauch im Praktikum bestimmt! Seite 41
• Für alle Verdauungsversuche gilt folgende Reihenfolge der Durchführung:
1. Versuchsansatz ins entsprechende Wasserbad,
2. reagieren lassen.
3: Herausnehmen,
4. Nachweismittel hinzufügen, bei Fehling: aufkochen.
Tab. 4: Zusammenstellung der Versuchsansätze
Nr. Versuchsansatz
10
min
. ins W
asse
rbad
!
Nachweisreaktion nach
10 Minuten im
Wasserbad (36°)
Verfärbung des Niederschlages Versuchs-
ergebnis (+ / - )
1 3 ml H2O,
10 Haferflocken Lugol´sche Lösung
2 3 ml H2O,
10 Haferflocken
Fehling´sche Lösungen I
und II, anschließend
aufkochen
3
3 ml
Speichellösung
10 Haferflocken,
1 ml Puffer pH7
Lugol´sche Lösung
4
3 ml
Speichellösung, 10
Haferflocken, 1 ml
Puffer pH7
Fehling´sche Lösungen I
und II, anschließend
aufkochen
5 3 ml
Speichellösung
Fehling´sche Lösungen I
und II, anschließend
aufkochen
6
3 ml
Speichellösung, 10
Haferflocken,
Reagenzglasinhalt
abfiltrieren, Filtrat mit
Fehling´schen Lösungen I
und II versetzen,
anschließend aufkochen
Versuch 6: Verdauung von Fett mittels Lipase
Lipase katalysiert die Spaltung von Fett in Glycerin und Fettsäuren:
H2C-O-C-Fettsäurerest 1 H2C-OH + Fettsäure 1
Lipase HC-O-C-Fettsäurerest 2 -------------------���� H-C-OH + Fettsäure 2
H2O
H2C-O-C-Fettsäurerest 3 H2C-OH + Fettsäure 3
Fettsäuren geben als Säuren H+-
Ionen ab, so dass die Lipasetätigkeit mit Hilfe der Änderung des pH-Wertes gut
verfolgt werden kann. Milch ist eine Emulsion mit den verschiedensten Bestandteilen, die Fett in kleinen
Tröpfchen enthält. Durch diese Tröpfchen erscheint Milch weiß.

M. Schessl & T. Hoppe – Skript zur Übung „Experimente zur allgemeinen Biologie“
Version für das WS 2011/12 Nur zum internen Gebrauch im Praktikum bestimmt! Seite 42
Versuchsaufgabe:
Durch diesen Versuch lässt sich außer der Fettverdauung auch der Einfluss der Temperatur auf enzymatische
Reaktionen beobachten. Die Temperatur spielt für die Reaktionsgeschwindigkeit eine entscheidende Rolle. Nach
der RGT-Regel steigert ein Erwärmen um 10° C die Reaktionsgeschwindigkeit um das 2 – 3-fache. Gilt dies auch
uneingeschränkt für die Enzymaktivität?
Material:
• 30 ml frische Vollmilch,
• 0,7 %ige Natriumcarbonatlösung,
• Phenolphthalein,
• Lipase- bzw. Pankreatinlösung 5% (Enzymgemisch aus der Bauchspeicheldrüse, das Lipase enthält),
• Reagenzgläser, Reagenzglasständer, Messpipetten 10ml und 1ml,
• Laboruhr, Wasserbäder 36° C, 45° C, 55° C mit eingesetzten Edelstahlreagenzglasständern, Peleusball
Versuchsdurchführung:
• In 8 Reagenzgläser werden jeweils 3 ml frische Vollmilch pipettiert.
• Die Milch jedes Glases wird mit 10 Tropfen Phenolphthalein versetzt
• dann mit 3 ml einer 0,7 %igen Natriumcarbonatlösung alkalisch gemacht.
• Danach wird die Emulsion geschüttelt, bis alles gleichmäßig gefärbt erscheint.
• Die Proben im Wasserbad auf die gewünschte Temperatur erhitzen (s. Angaben in Tab. 6).
• Jeweils 1 ml der Lipaselösung ebenfalls auf die gewünschte Temperatur erhitzen (s. Angaben in Tab. 6).
• Nach einigen Minuten die Milch in die Lipaselösung geben.
• Messen Sie die Zeit, die von der Enzymzugabe bis zur Entfärbung vergeht.
Tab. 5: Meßwerte zum Versuch 14
Temperatur Entfärbezeit
10°C
25 °C
36° C
45° C
55° C
• Stellen Sie die Ergebnisse graphisch dar (Temperatur auf der Abszisse, Entfärbezeit auf der Ordinate)!
• Tragen Sie die Ergebnisse auch mit einer gruppenspezifischen Kreidefarbe in den Graphen an der Tafel ein!
• Vergleichen Sie die Ergebnisse mit denen anderer Gruppen! Diskutieren Sie die Ergebnisse und nehmen Sie
Stellung zur Versuchsfrage!

M. Schessl & T. Hoppe – Skript zur Übung „Experimente zur allgemeinen Biologie“
Version für das WS 2011/12 Nur zum internen Gebrauch im Praktikum bestimmt! Seite 43
Versuch 7: Eiweißverdauung
Die Eiweißstoffe gelangen über die Speiseröhre in den Magen. Der Magensaft ist im Gegensatz zum neutralen
Mundspeichel aufgrund der Salzsäureproduktion der Belegzellen in der Magenwand stark sauer. Durch diese pH-
Änderung wird die Struktur vieler Proteine aufgebrochen. Die Proteine werden in eine gestreckte, für die
Hydrolyse und Enzymkatalyse angreifbare Form überführt. Das wichtigste hier wirksame Enzym ist Pepsin.
Pepsin wird in den Hauptzellen der Magenwanddrüsenzellen in einer unwirksamen Vorstufe (sonst
Selbstverdauung!) hergestellt. Das Pepsin ist an einen Hemmstoff gebunden, durch den seine Wirksamkeit
blockiert ist. Gelangt es dann ins Mageninnere, wird es durch die Magensäure in seine wirksame Form überführt.
Aus Zeitgründen wollen wir auf die Versuche in Gruppen verzichten und die Versuche für alle einmal durchführen.
Aufgabe:
• Was bewirkt Pepsin bei Eiweiß und unter welchen pH-Bedingungen liegt das Wirkungsoptimum dieses
Enzyms?
• Quelle für Versuchsanleitung: http://www.seminare-bw.de/servlet/PB/-
s/1ac1rui1vqxro1gx54t8gnjagvzxke1x/show/1216936/nwa-tag-2007-eiweissverdauung.pdf
• Formeln und Zusammensetzung der Chemikalien auflisten
Material:
• Tageslichtprojektor, gekochtes Eiklar (durch Teesieb zerdrückt), 4 Petrischalen, Wasser, 1%ige Pepsin-Lösung,
5%ige Salzsäure, Tageslichtprojektor, Indikatorpapier
Versuchsdurchführung:
• In die 4 Petrischalen wird je eine erbsengroße Menge zerdrücktes Eiklar gegeben. In Schale 1 werden zudem
10 ml Wasser gegeben, in Schale 2 9 ml 1%ige Pepsin-Lösung sowie 1 ml Wasser, in Schale 3 9 ml Wasser und
1 ml 5%ige Salzsäure. In Schale 4 werden 9 ml 1%ige Pepsin-Lösung sowie 1 ml 5%ige Salzsäure zugefügt. Die
Schalen werden für mindestens 2 Stunden auf einen Tageslichtprojektor gestellt.
• Messen Sie die pH-Werte mit Indikatorpapier!
• Tragen Sie die Ergebnisse in die nachfolgende Tabelle ein!
Tab. 6: Ergebnistabelle zum Versuch ph-Optimum von Pepsin
Nr. Versuchsansatz pH-Wert Ergebnis
1 • ca. erbsengroße Menge Eiklarbrei in
Petrischale mit 10 ml Wasser
2 • ca. erbsengroße Menge Eiklarbrei in
Petrischale mit 9 ml 1%iger Pepsin-
Lösung und 1 ml Wasser
3 • ca. erbsengroße Menge Eiklarbrei in
Petrischale mit 9 ml Wasser und 1 ml
5%iger Salzsäure
4 • ca. erbsengroße Menge Eiklarbrei in
Petrischale mit 9 ml 1%iger Pepsin-
Lösung und 1 ml 5%iger Salzsäure

M. Schessl & T. Hoppe – Skript zur Übung „Experimente zur allgemeinen Biologie“
Version für das WS 2011/12 Nur zum internen Gebrauch im Praktikum bestimmt! Seite 44
5.11. Kurstag „Atmung“
5.11.1. Ihre Vorbereitung
• Suchen Sie nach einer Definition für Zellatmung. Wozu brauchen wir diesen Prozess? Welche Organismen
atmen?.... und wann (wieviel)?
Stichworte: Autotrophe, Heterotrophe, Produzente, Konsumenten, Reduzenten, biologische Oxidation;
innere Atmung, äußere Atmung,
Versuch 8: Wie unterscheidet sich die Zusammensetzung der ausgeatmeten Luft von der Zusammensetzung der
eingeatmeten Luft bezüglich der CO2-Konzentration?
Vorbereitung:
• In diesem Versuch arbeiten Sie in Zweier- und Dreiergruppen. Hier muss ein Protokoll angefertigt werden.
• Informieren Sie sich über die stoffliche Zusammensetzung der Luft!
• Wieso setzen wir Kalkwasser ein?
Material:
• 2 Waschflaschen, 1 T-Rohrstück, 3 Schlauchstücke,
• Kalkwasser
Versuchsdurchführung:
• Die beiden Waschflaschen werden mit je ca. 10 cm (Füllhöhe) mit Kalkwasser gefüllt.
• Waschflaschen, T-Rohr und Schlauchverbindungsstücke werden entsprechend der folgenden Zeichnung
zusammengebaut (Abb. 19)
• Dann wird nach vorherigem
Ausatmen die Luft langsam durch das
T-Rohr eingeatmet (durch welche
Flasche?).
• Ohne abzusetzen, wird danach durch
das T-Rohr ausgeatmet.
• Dieser Vorgang wird mehrmals
wiederholt.
• Bitte variieren Sie den Versuch
innerhalb des Kurses dergestalt, daß
einige Probanden vorher Kniebeugen
etc. durchführen.
Aufgaben:
• Wie ändert sich das Kalkwasser in der
"Einatmungsflasche" bzw. in der
"Ausatmungsflasche"?
• Schreiben Sie die Gleichung für die Nachweisreaktion des CO2 auf!
• Deuten Sie das Versuchsergebnis!
Abb. 17: Schematischer Versuchsaufbau zum Atmungsversuch

M. Schessl & T. Hoppe – Skript zur Übung „Experimente zur allgemeinen Biologie“
Version für das WS 2011/12 Nur zum internen Gebrauch im Praktikum bestimmt! Seite 45
Versuch 9: Wie unter scheidet sich die Zusammensetzung der ausgeatmeten Luft von der Zusammensetzung der
eingeatmeten Luft bezüglich der O2-Konzentration?
Material:
• 1 Standzylinder,
• 1 Glasdeckel, 1 Aquarium,
• Waschflasche mit Kalkwasser, 1 Gummiverbindungsstück mit gebogenem Glasrohr,
• 2 Kerzen, Streichhölzer,
• Uhr mit Sekundenzeiger.
Versuchsdurchführung:
• Man senkt über eine brennende Kerze einen Glaszylinder und misst, wie lange die Kerze danach noch ìn
diesem begrenzten Luftraum brennt.
• Aus 5 Versuchen wird ein Mittelwert gebildet.
• Dann wird das Aquarium bis über die Hälfte mit Wasser gefüllt. In die Wanne wird der Glaszylinder
eingetaucht, dabei mit Wasser gefüllt.
• Die Luft wird durch die Waschflasche mit Kalkwasser (Einatmungsflasche aus vorherigem Versuch) über einen
Gummischlauch und das Glasrohr in den Glaszylinder ausgeatmet. Dies ist ein wichtiger Bestandteil des
Versuchsaufbaus, ohne den dieser Versuch keinen Sinn machen würde. Deshalb: warum machen Sie dies?
• Der vollständig mit Atemluft
gefüllte Zylinder wird unter Wasser
mit einem Glasdeckel verschlossen
(evtl. noch vorhandenes Wasser
bei leicht geöffnetem Deckel
ausfließen lassen!).
• Diesen mit ausgeatmeter Luft
gefüllten Zylinder stülpt man, wie
in den Vorversuchen, wieder über
dieselbe brennende Kerze und
stellt die Brenndauer der Kerze
fest.
• Das Aquarium nicht ausleeren! Sie
können es für den anschließenden
Versuch zur Ermittlung des
respiratorischen Quotienten
verwenden!
Auswertung:
• Tragen Sie die Meßwerte in eine Tabelle an der Tafel ein. Nutzen Sie die Daten aller Gruppen Ihres Kurses, um
Ihre Meßwerte vergleichend zu beschreiben.
• Fertigen Sie ein Protokoll zu diesem Versuch an. Folgende Fragen sollten hierin (in welchen Kapiteln?)
besprochen werden
• Schätzen Sie durch Vergleich der Brenndauer der Kerze in den beiden Teilversuchen ab, wieviel Sauerstoff
sich in der Atemluft befinden könnte. (Diskussionsteil)
• Welche Funktion hat die vorgeschaltete Waschflasche mit Kalkwasser (Methodenteil)?
Abb. 18: Versuchsaufbau zum „CO2-Versuch“

M. Schessl & T. Hoppe – Skript zur Übung „Experimente zur allgemeinen Biologie“
Version für das WS 2011/12 Nur zum internen Gebrauch im Praktikum bestimmt! Seite 46
Versuch 10: Atmen auch grüne Pflanzen?
Material:
• 3 Waschflaschen,
• 1 Standzylinder mit doppelt durchbohrtem Stopfen und zwei kurzen, rechtwinklig gebogenen Glasrohren,
• Kalkwasser, Wasserstrahlpumpe, Alufolie,
• Coleus-Pflanze, die in den Standzylinder passt,
• Schlauchstückchen.
Durchführung:
• 2 Stunden reichen meist nicht aus, um das Ergebnis zu zeigen, deshalb wird der Versuch mehrere Stunden vor
dem Übungstermin angesetzt
• Der Versuch wird als Demonstration einmal für das gesamte Praktikum vorgezeigt
• Er hat den in Abb. 9 dargestellten Aufbau: Der Standzylinder mit der Pflanze ist mit Alufolie umwickelt, so
dass kein Licht eindringen kann. Eine Aquarienpumpe belüftet die Apparatur.
Auswertung
Fertigen Sie ein Protokoll zu diesem Versuch an. Folgende Fragen sollten hierin (in welchen Kapiteln?) besprochen
werden
• Wozu dient das Kalkwasser in der 1., 2. und 3. Waschflasche? Ab wann haben wir ein „sicheres“ Ergebnis?
• Warum wird verhindert, dass Licht in den Standzylinder eindringt?
• Wie sieht das Versuchsergebnis aus und was schließen Sie daraus?
Abb. 19: Versuchsaufbau zum Demonstrationsversuch: „atmen Pflanzen?“

M. Schessl & T. Hoppe – Skript zur Übung „Experimente zur allgemeinen Biologie“
Version für das WS 2011/12 Nur zum internen Gebrauch im Praktikum bestimmt! Seite 47
5.11.2. Bestimmung des respiratorischen Quotienten
Einleitung
Nahrungsstoffe werden im Wesentlichen über einen bestimmten Stoffwechselweg zur Energiegewinnung
abgebaut. Wenn man vom Zucker Glucose ausgeht, kann man diesen in 4 verschiedene Abschnitte einteilen:
1. die Glycolyse
2. die oxidative Decarboxylierung
3. den Zitronensäurezyklus
4. die Atmungskette.
Wird Glucose unter Verwendung von Sauerstoff abgebaut, wird der vollständige Weg durchlaufen. Fette werden
zunächst in Glycerin und Fettsäuren gespalten. Anschließend werden von der Fettsäure C2-Körper abgespalten und
in Acetyl-Coenzym A umgewandelt, welches dann in den Zitronensäurezyklus eingeschleust wird. Eiweiße werden
in Aminosäuren zerlegt. Die meisten können dann über Zwischenstufen zu Bernsteinsäure verarbeitet werden,
welche Bestandteil des Zitronensäurezyklus ist.
Nicht nur Kohlenhydrate können über die genannten Abbauwege veratmet werden, sondern auch Aminosäuren
und Fette. Die meisten Aminosäuren lassen sich, wenn man die Aminogruppe abgespalten hat ( → Harnstoff), in
eine der Säuren des Citratzyklus überführen und damit vollständig abbauen. Fette werden zunächst in Glycerin und
Fettsäuren gespalten. Von den Fettsäuren werden C2-Körper abgespalten, an Coenzym A gebunden und dann in
den Citratzyklus eingeschleust.
Als Nährstoffe werden allen Zellen Glukose (auch als Abbauprodukt der anderen Kohlenhydrate), verschiedene
Fettsäuren (Abbauprodukte der Fette) und Spaltprodukte der Eiweißstoffe geliefert. Die für die Lebensvorgänge in
den Zellen notwendige Energie wird dann durch oxydativen Abbau von Glukose, Fettsäuren usw. in den einzelnen
Zellen gewonnen. Die Abbauwege für Glukose, Fettsäuren und Eiweißspaltprodukte sind jeweils verschieden.
Gemeinsam ist den Abbauwegen im sogenannten aeroben Stoffwechsel, dass O2 benötigt wird und CO2 als
Abfallprodukt frei wird. Das Verhältnis von aufgenommenem O2 und freigesetztem CO2 ist beim oxydativen Abbau
von Glukose, Fettsäuren und Eiweißspaltprodukten verschieden. Es hängt davon ab, wie viel O2 das abzubauende
Molekül selbst mit in die Zelle bringt. Kohlenhydrate enthalten relativ viel O2. Für ihren Abbau muss nicht mehr
sehr viel O2 über die äußere Atmung hinzugeliefert werden. Anders ist es bei den Fettsäuren. Das zeigen die
folgenden Bruttogleichungen für den oxydativen Glukose- und Fettsäureabbau (Tab. XX). Den Quotienten aus CO2
und O2 nennt man den Respiratorischen Quotienten (RQ).
Abb. 20: Bruttogleichungen und respiratorische Quotienten für Glucose und Stearin
Stoff Bruttogleichungen Respiratorischen Quotienten (RQ).
Glucose C6H12O6 + 6 O2 → 6 CO2 + 6 H2O + Energie RQ für Glukose: 6/6 = 1
Stearinsäure C17H35COOH + 26 O2 → 18 CO2 + 18 H2O + Energie RQ für Stearinsäure: 18/26 = 0,69
Nach Avogadro gilt nun: Bei gleicher Temperatur und gleichem Druck enthalten gleiche Volumina idealer Gase die
gleiche Zahl von Molekülen. Auf unser Problem angewandt, könnte man auch sagen: den Volumenverhältnissen

M. Schessl & T. Hoppe – Skript zur Übung „Experimente zur allgemeinen Biologie“
Version für das WS 2011/12 Nur zum internen Gebrauch im Praktikum bestimmt! Seite 48
entsprechen unter gleichen Bedingungen die Molekülzahlen. Bestimmt man also die Volumenverhältnisse von
aufgenommenem O2 und abgegebenem CO2, so lässt sich daraus im Idealfall ablesen, ob in den Zellen des
betreffenden Tieres Kohlenhydrate (RQ = 0,9 - 1,0), Fette (RQ = 0,6 - 0,7) oder andere Stoffe abgebaut werden.
Versuch 11: Bestimmung des Respiratorischen Quotienten einer Maus – Alternativdurchführung mit Mehlwürmern
Versuchsfrage:
• Wovon ernährt sich das Ihnen zur Untersuchung ausgegebene Tier?
Material:
• Respirometer, bestehend aus 1 Erlenmeyerkolben 500 ml, 1 doppelt durchbohrtem Stopfen mit Glasspritze
10 ml und NaOH-Gefäß, 1 Glashahn und 1 Manometerrohr,
• Aquarium, 1 Stativ, Kreuzmuffe (nicht drehbar), Klemme für Erlenmeyerkolben, Laboruhr,
• Tiere
Versuchsdurchführung:
• Bauen Sie das Respirometer nach Abb. 11e
zusammen:
• füllen Sie in das Manometer etwas Wasser
• Setzen Sie die Tiere (Gewicht bestimmen) in den
Erlenmeyer-Kolben und verschließen Sie ihn mit
dem Gummistopfen samt Zubehör.
• Im Teilversuch, bei dem NaOH-Plätzchen
zugegeben werden, legen Sie das mit Gaze
verschlossene Schnappdeckelglas in den
Erlenmeyer-Kolben.
• Der Versuch ist höchst temperaturlabil und wird
am besten in einem Wasserbad mit
Raumtemperatur durchgeführt (warum?).
• Wenn der Stopfen aufgesetzt wird, muss der Glashahn geöffnet sein. Sonst werden Sie u.U. duschen!
• Der Kolben der Glasspritze wird auf seine oberste Marke gestellt.
• Zur Überprüfung auf Dichtigkeit wird der Glashahn geschlossen und der Spritzenkolben etwas
heruntergedrückt. Die Wassersäule im Manometerrohr darf jetzt nicht in den ursprünglichen Stand
zurückkehren.
• Nach der Dichteprüfung wird der Glashahn wieder geöffnet, der Spritzenkolben auf die oberste Marke
gebracht und der Manometerstand mit einem Filzschreiber markiert.
• Dann wartet man 5 Minuten, bis die Versuchsbedingungen etwa konstant sind. Dann wird der Glashahn
geschlossen und die Uhr gestartet.
• Alle 2 Minuten wird der Manometerstand wieder mit der Spritze auf die Filzstiftmarke eingestellt und das
Volumen an der Spritze abgelesen.
• Wenn an der Glasspritze die unterste Marke erreicht ist, wird der Versuch spätestens beendet.
• Der Stopfen wird entfernt, damit die Tiere frische Luft bekommen.
• Die Versuchszeit soll der des ersten Versuchs entsprechen. Das Gasvolumen ändert sich jetzt nur
unwesentlich.
• Das an der Spritze abgelesene Volumen entspricht der Differenz aus Sauerstoffverbrauch und CO2-Abgabe.
Abb. 21: Versuchsaufbau zum Respirationsversuch

M. Schessl & T. Hoppe – Skript zur Übung „Experimente zur allgemeinen Biologie“
Version für das WS 2011/12 Nur zum internen Gebrauch im Praktikum bestimmt! Seite 49
Auswertung
• Notieren Sie die Änderungen des Gasvolumens in beiden Versuchen in die nachfolgende Tabelle
• Berechnen Sie den Respiratorischen Quotienten aus den beiden Versuchsserien mithilfe der unten
dargestellten Formel (Tab. 7).
• Notieren Sie das Endvolumen verbrauchter Luft beider Teilversuche in eine Tabelle an der Tafel
• Fertigen Sie ein Protokoll zu diesem Versuch an. Der Versuch ist apparativ sehr heikel, es ist gut möglich, daß
er bei Ihrer Gruppe nicht auf Anhieb funktioniert. Deshalb ist es in diesem Kurstag besonders wichtig, die
Rohdaten verschiedener Arbeitsgruppen Ihres Kurses ebenfalls zu notieren, um ein sinnvolles Protokoll
erstellen zu können.
• Überlegen Sie, welche möglichen Fehler Sie gemacht haben könnten bzw. welche Fehlerquellen die
Messapparatur und Auswertung beinhalten könnten.
• Diskutieren Sie in Ihre Werte vergleichend mit denjenigen, anderer Gruppen.
Tab. 7: Versuchsergebnisse zum Respirationsversuch
mit NaOH ohne NaOH
Zeit Gesamtvolumen Zeit Gesamtvolumen
2' 2'
4' 4'
6' 6'
RQCO Abgabe
O Aufnahme
O O CO
O= −
−=
− −2
2
2 2 2
2
[O2] = Messergebnis des Versuchs mit NaOH
[O2 - CO2] = Messergebnis des Versuchs ohne NaOH
Abb. 22: Formel zur Berechnung des respiratorischen Quotienten

M. Schessl & T. Hoppe – Skript zur Übung „Experimente zur allgemeinen Biologie“
Version für das WS 2011/12 Nur zum internen Gebrauch im Praktikum bestimmt! Seite 50
5.12. Kurstag „Anatomie eines Knochenfisches“
Material:
• Regenbogenforelle, Oncorhynchus mykiss (Teleostei, Salmonidae)
• Teller, Präparierschere, Pinzette, Sonde,
• Herzmodell des Hechts, Modell eines Karpfens
Durchführung:
• Sie arbeiten in Zweiergruppen
• Führen Sie zuerst eine äußere Inspektion vor, d.h. begutachten Sie Ihren Fisch von außen; gehen Sie hierzu
das unten anschließende Kapitel Schritt für Schritt durch.
• Führen Sie dann erst die Präparation durch. Arbeiten Sie hierzu die Punkte im entsprechenden unten
anschließenden Kapitel ab.
• Zeichnen Sie das Gesehene
Präparat 9: Äußere Inspektion des Fisches
Die Forelle ist als Knochenfisch in drei Abschnitte gegliedert: den Kopf mit den Hauptsinnesorganen (Augen, Nase,
Gleichgewichtssinn), dem Gehirn und der Mundöffnung; den Rumpf mit den Eingeweiden und den Schwanz, der
hinter der Afteröffnung beginnt, als Hauptfortbewegungsorgan.
• Sehen Sie sich die Augen, die Nasenöffnungen und die Mundöffnung mit ihrer Bezahnung an!
• Sondieren Sie die Nasenöffnungen! Ist eine Verbindung zum Mund vorhanden?
• Betrachten Sie die Kiemen (Kammkiemen) durch Anheben eines Kiemendeckels!
• Was für Flossen hat die Forelle (paarige-, unpaare Flossen)?
• Sehen Sie sich das Seitenliniensystem als Ferntastsinn an!
• Wo liegen die Öffnungen für den Darmausgang, die Harnwege und die Geschlechtsorgane?
• Sehen Sie sich die Beschuppung an!
Präparat 10: Präparation der Forelle (Situspräparation)
Durchführung:
• Sehen Sie sich zunächst das OHP-Bild an, damit Sie wissen, wie Ihr Präparat aussehen soll.
• Durchstechen Sie mit der kleinen Schere die Bauchdecke vor der Kloake und schneiden Sie diese bis zum Kinn
auf.
• Legen Sie die Forelle o auf den Teller, dass der Kopf nach rechts zeigt.
• Während Sie die Bauchdecke anheben, schneiden Sie die Seiten bis an die Schwimmblase auf und entfernen
dann durch einen Schnitt entlang der Schwimmblase auf einer Seite die Muskulatur;
Vorsicht: Schwimmblase nicht verletzen!
• Versuchen Sie, die jetzt sichtbaren Organe zu identifizieren.
• Legen Sie den Magen-Darm-Trakt heraus (wie in der Video-Aufzeichnung zu sehen ist) und zeichnen Sie den
Situs.
• Achten Sie darauf, dass das Papier (DIN A4) gut ausgenutzt ist! Beachten Sie, dass die Forelle einen anderen
Habitus hat als die Plötze auf der Abb. 18.

M. Schessl & T. Hoppe – Skript zur Übung „Experimente zur allgemeinen Biologie“
Version für das WS 2011/12 Nur zum internen Gebrauch im Praktikum bestimmt! Seite 51
Beschriftung:
• Oncorhynchus mykiss (Regenbogenforelle), Teleostei, Salmonidae, Situs.
• Fam. Salmonidae (Lachsartige) O. Salmoniformes (Karpfenartige) Kl. Teleostei (Knochenfische).
Dies sollten Sie sehen und zeichnen:
• Darmtrakt: Mundöffnung mit Mundzähnen, Magen, Pylorus-Anhänge (Merkmal für Salmoniden u. a.), Darm,
Kloake, Leber, Milz.
• Extremitäten: paarig: Brustflossen, Bauchflossen; unpaar: Rücken-, After-, Schwanzflosse. Die unpaare
Fettflosse (ohne Flossenstrahlen) ist ein Merkmal der Salmoniden.
• Sinnesorgane: Nase, Augen, Seitenlinie.
• Atmungsorgane: Kammkiemen, Kiemendeckel (ein Stück davon mit der Schere abschneiden, damit man die
Kammkiemen sehen kann!).
• Ausscheidungsorgane: Opistonephros, Harnleiter.
• Geschlechtsorgane: Testis / Ovar, Samenleiter / Eileiter.
• Schwimmblase.
Wenn Sie Ihr Situspräparat der Forelle mit der Abbildung des Plötzensitus (Rutilus rutilus, Abb. 18) vergleichen, fällt
sofort auf, dass der Forellensitus viel übersichtlicher ist. Das liegt daran, dass die Plötze einen sehr viel längeren
Darm besitzt. Die Plötze zeichnet sich außerdem durch ein Fehlen der Mundbezahnung (Schlundzähne!) aus.
Ursache für diesen Unterschied ist die Anpassung an verschiedene Nahrung: Die Forelle ernährt sich als Räuber
von tierischer Kost. Diese ist relativ leicht zu verdauen. Die Plötze hingegen ernährt sich von pflanzlicher Nahrung.
Pflanzliche Nahrung besteht jedoch zum überwiegenden Teil aus Zellulose (Zellwände), die von Tieren selbst nicht
abgebaut werden kann. In dem langen Darm erhalten Darmbakterien Gelegenheit, einen Teil der Zellulose
abzubauen und für den Fisch verfügbar zu machen.
Noch extremer sind jedoch die Unterschiede im Verdauungssystem von Säugetieren: Räuber wie Hund oder Katze
sind nicht in der Lage, mit pflanzlicher Kost auszukommen. Auch bei Mensch und Schwein, die über einen
verlängerten Darm verfügen, findet keine geregelte Zelluloseverdauung statt. Dagegen haben Pflanzenfresser
spezielle Organe für die Zelluloseverdauung mit Bakterien ausgebildet: Hasenartige, Nager und Pferde besitzen zu
diesem Zweck einen vergrößerten Blinddarm, in dem die Nahrung länger verbleiben kann. Wiederkäuer haben
ihren Magen aufgeteilt, so dass hier die Zellulose aufgeschlossen werden kann.

M. Schessl & T. Hoppe – Skript zur Übung „Experimente zur allgemeinen Biologie“
Version für das WS 2011/12 Nur zum internen Gebrauch im Praktikum bestimmt! Seite 52
1. Mundöffnung
2. Zunge
3. Kiemen
4. Bulbus arteriosus
5. Herzkammer
6. Vorkammer, darunter Sinus
venosus
7. Vordere Bauchfellwand
8. Darm
9. 1. Leberlappen
10. 2. Leberlappen
11. Hoden
12. 3. Leberlappen
13. Bauchflosse
14. After
15. Geschlechtsöffnung
16. ?
17. ?
18. Afterflosse
19. Rückenflosse
20. Bulbus olfactorius
21. Auge
22. Mittelhirn
23. Schlundkopf
24. Kopfniere
25. Schwimmblase
26. Niere
27. Rippen
28. Schwimmblase
29. Rückenflosse
Abb. 23: Anatomie von Rutilus rutilus (Plötze oder Rotauge)

M. Schessl & T. Hoppe – Skript zur Übung „Experimente zur allgemeinen Biologie“
Version für das WS 2011/12 Nur zum internen Gebrauch im Praktikum bestimmt! Seite 53
Präparat 11: Präparation des Herzens:
• Sehen Sie sich das OHP-Bild an!
• Zwischen den Kiemen liegt im Herzbeutel das Herz. Meist ist das Perikard (der Herzbeutel) schon beim
Aufschneiden der Bauchhöhle verletzt worden. Nun werden die Reste vorsichtig mit der Pinzette weggezupft.
• Jetzt können die verschiedenen Teile des Fischherzens identifiziert werden. Nehmen Sie die Literatur und das
Modell zu Hilfe!
• Skizzieren Sie das Herz mit den abführenden Gefäßen!
• Beschriftung:
Sinus venosus, Vorkammer,
Ventrikel, Bulbus arteriosus,
Truncus arteriosus,
Kiemenarterienstamm.
Anmerkung:
Bei den ursprünglichen Wirbeltieren, z. B. Neunauge (Agnatha, Rundmäuler), liegen je 3 paarige Kiemenarterien
vor. Kopfwärts bilden sich in der Evolution die ersten beiden Paare zurück, so dass bei den höheren Fischen (den
Knochenfischen) nur noch 4 Kiemenarterienpaare vorliegen (Abb. 19, links). Bis zu den Säugetieren (Abb. 19,
rechts) werden dann von diesen 4 weitere Arterien zurück- und umgebildet: die 1. werden zu den Kopfarterien
(mit Abzweigen zu den Armarterien), die linke 2. wird zur Aorta, die rechte 2. und die beiden 3. werden
zurückgebildet und die beiden 4. werden zu den Lungenarterien.
Schematischer Aufbau des Herzens eines
Knochenfisches
Schematischer Aufbau des Herzens eines Säugers
Abb. 24: Aufbau des Herzens von Fisch und Säugetier








![Untersuchungen zum Wert der Sputumzytologie bei … · der von den Oberflächenepithelien der Bronchial- oder Bronchiolenwand herleiten oder vom bronchialen APUD-System ausgehen [76].](https://static.fdokument.com/doc/165x107/5b9f99de09d3f2857a8b5e77/untersuchungen-zum-wert-der-sputumzytologie-bei-der-von-den-oberflaechenepithelien.jpg)