Effekte der neuromuskulären Stimulation des distalen N. … · - 2 - Angenommen vom Fachbereich...
Transcript of Effekte der neuromuskulären Stimulation des distalen N. … · - 2 - Angenommen vom Fachbereich...

Aus der Klinik für Innere Medizin, Schwerpunkt Pneumologie
Geschäftsführender Direktor: Prof. Dr. C. Vogelmeier
des Fachbereichs Medizin der Philipps-Universität Marburg
in Zusammenarbeit mit dem Universitätsklinikum Gießen und Marburg GmbH,
Standort Marburg
Effekte der neuromuskulären Stimulation
des distalen N. hypoglossus auf die
Funktion der oberen Atemwege und den
inspiratorischen Atemfluss
Inaugural-Dissertation zur Erlangung des
Doktorgrades der gesamten Humanmedizin
dem Fachbereich Medizin der Philipps-Universität
vorgelegt von
Gerald Kalmus
aus Karlsruhe
Marburg, 2008

- 2 -
Angenommen vom Fachbereich Medizin der Philipps-Universität Marburg
am 03.07.2008.
Gedruckt mit Genehmigung des Fachbereichs.
Dekan: Prof. Dr. M. Rothmund
Referent: Prof. Dr. T. Penzel
Korreferent: Prof. Dr. F. L. Welter

- 3 -
Inhaltsverzeichnis Seite
1. Einleitung 6
1.1 Schlafbezogene Atmungsstörungen 6
1.1.1 Obstruktives Schlafapnoe-Syndrom (OSAS) 6
1.1.2 Physiologie der Atmung im Schlaf 7
1.1.2.1 Koordination der oberen Atemwege im Schlaf 8
1.1.3 Definitionen und Klassifikationen von schlafbezogenen
Atmungsstörungen 11
1.1.4 Epidemiologie 12
1.1.5 Pathophysiologische Veränderungen bei obstruktiven,
schlafbezogenen Atmungsstörungen 12
1.1.6 Anatomische Charakteristika der Obstruktiven Schlafapnoe 13
1.1.7 Neurologische Charakteristika der Obstruktiven Schlafapnoe 13
1.1.8 Symptome bei schlafbezogenen Atmungsstörungen 15
1.2 Diagnostik schlafbezogener Atmungsstörungen 16
1.3 Quantifizierung der pharyngealen Kollapsibilität im Schlaf
(kritischer pharyngealer Verschlussdruck = Pcrit) 16
1.3.1 Der Starling Resistor 18
1.3.2 Klinische Untersuchungen zum kritischen pharyngealen
Verschlussdruck 20
1.3.3 Determinanten der pharyngealen Kollapsibilität 21
1.4 Therapie schlafbezogener Atmungsstörungen 23
1.4.1 Nicht-operative Verfahren 24
1.4.2 Operative Verfahren 25
1.5. Innovative Behandlungsansätze: Elektrische Stimulation der
oberen Atemwege 26
2. Fragestellung 29
3. Methoden 30
3.1. Auswahl des Patientenkollektivs 30
3.2. Datenerhebung 31

- 4 -
3.2.1. Polysomnographie 31
3.2.2. Ermittlung des dynamischen Widerstands der oberen
Atemwege 32
3.2.3. Messung des kritischen pharyngealen Verschlussdruckes (Pcrit) 33
3.3. Auswertung 35
3.3.1. Auswertung der Polysomnographie 35
3.3.2. Berechnung des kritischen pharyngealen Verschlussdruckes
und des pharyngealen Widerstandes 36
3.4. Das Schrittmacher-System zur atmungsgetriggerten
neuromuskulären Stimulation des N. Hypoglossus 38
3.4.1. Die Komponenten 38
3.5. Operatives Procedere 39
3.6. Patientenkollektiv 41
3.7. Statistische Auswertung 42
4. Ergebnisse 43
4.1. Operativer und postoperativer Verlauf 43
4.2. Effekte der unilateralen elektrischen Stimulation des
N. Hypoglossus auf die respiratorischen Parameter 43
4.2.1. Unmittelbare Effekte während einzelner Atemzyklen 43
4.2.2. Langzeiteffekte aller gemessenen Patienten 45
4.2.2.1. Schlafbezogene Atmungsstörungen 45
4.2.2.2. Schlafparameter 46
4.3. Funktionen des Schrittmachers 47
4.3.1. Technische Parameter im Verlauf 47
4.3.2. Elektrodenbruch/Haltbarkeit der Hardware 48
4.4. Sub-Set-Analyse mit Messung der pharyngealen Kollapsibilität
und des Widerstandes der oberen Atemwege bei n=4 Patienten 48
4.4.1. Pressure-Flow-Analyse mit und ohne Stimulation bei Rückenlage 50
4.4.2. Tabellen und Zusammenstellung des kritischen pharyngealen
Verschlussdruckes und des oberen Atemwiderstandes 51

- 5 -
5. Diskussion 53
5.1. Methodische Diskussion 54
5.2. Klinische Diskussion 55
5.3. Mechanik der oberen Atemwege unter elektrischer Stimulation 56
5.4. Effekte der elektrischen Stimulation auf den Schlaf 59
5.5. Implikationen 60
6. Zusammenfassung 61
7. Literaturverzeichnis 63
8. Anhang 78
8.1. Abkürzungsverzeichnis 78
8.2. Verzeichnis der Abbildungen 79
8.3. Verzeichnis der Tabellen 80
8.4. Danksagung 80
8.5. Akademische Lehrer 81
8.6. Lebenslauf 82
8.7. Ehrenwörtliche Erklärung 84

- 6 -
1. Einleitung
1.1. Schlafbezogene Atmungsstörungen
1.1.1. Obstruktives Schlafapnoe-Syndrom (OSAS)
Charakteristisch für die obstruktive Schlafapnoe sind phasenweise
Einengungen der pharyngealen Atemwege während des Schlafs mit
anschließenden Atmungsstörungen in Form von Atemstillständen und
Hypopnoen. Jede Phase wird ihrerseits durch eine Weckreaktion, ein Arousal,
terminiert. Diese wiederholt auftretenden Arousals führen zu einer Störung der
Schlafstruktur mit den dazugehörenden Symptomen des nicht erholsamen
Schlafes wie zum Beispiel vermehrte Tagesmüdigkeit. Zudem lässt sich eine
über längere Zeit bestehende obstruktive Schlafapnoe mit schwerwiegenden
internistischen Erkrankungen (Herzrhythmusstörungen, Hypertonie, Herzinfarkt,
Schlaganfall, etc.) in Verbindung bringen18,82,97,98,100. Über die Häufigkeit der
Atmungsstörungen während des Schlafes sowie einer vorhandenen
Tagessymptomatik wird das Vorliegen eines obstruktiven Schlafapnoe-
Syndroms definiert. Nach den Kriterien der Internationalen Klassifikation der
Schlafstörungen (ICSD-2) spricht man von einem Obstruktiven Schlafapnoe-
Syndrom wenn mindestens 5 Atmungsstörungen pro Stunde Schlaf bei
Patienten mit Tagessymptomatik oder mindestens 15 Atmungsstörungen pro
Stunde Schlaf bei Patienten ohne Tagessymptomatik vorliegen.
In den „S2“-Leitlinien der Deutschen Gesellschaft für Schlafforschung und
Schlafmedizin (DGSM) für „Nicht-erholsamen Schlaf“ findet man ein großes
Spektrum an Krankheiten deren Charakteristika die oberen
Atemwegsobstruktionen sind und durch die unterschiedliche Beeinträchtigung
der Ventilation zu unterschiedlichen Schweregraden führen können.24

- 7 -
1.1.2. Physiologie der Atmung im Schlaf
Der Schlaf wird anhand der Hirnstromaktivität durch Differenzierung von
Frequenz und Amplitude beurteilt. Zusätzlich dienen morphologische
Charakteristika der enzephalographischen Wellenformen zur Identifizierung
unterschiedlicher Schlafstadien.
Zur Zeit der Durchführung der Untersuchung erfolgte die Schlaf- EEG-
Auswertung nach den Richtlinien des 1968 herausgegebenen Manuals von
Rechtschaffen und Kales. Zur Schlafstadienanalyse werden
Elektroenzephalogramm (EEG), Elektroocculogramm (EOG) und
Elektromyogramm (EMG) abgeleitet 104 und Gesamtschlaf in REM- (Rapid Eye
Movement) und NREM-Schlaf (Non Rapid Eye Movement) unterteilt. Der
NREM-Schlaf wird weiterhin in Leichtschlaf, mit den Schlafstadien 1 und 2,
sowie in Tiefschlaf, mit den Schlafstadien 3 und 4, eingeteilt. In der Abfolge der
Schlafstadien kommt es zu einer kontinuierlichen Abnahme des Muskeltonus
und der Verlangsamung der Hirnstromaktivität. Man bezeichnet den NREM-
Schlaf auch als orthodoxen Schlaf.
In der REM- Schlafphase treten schnelle horizontale Augenbewegungen auf,
die ihm seinen Namen gaben. Dieser REM-Schlaf verzeichnet die niedrigste
Muskelaktivität, aber auch zugleich die höchste Aktivität im EEG, weshalb man
auch vom paradoxen Schlaf spricht 33. Darüber hinaus hat der REM-Schlaf
weitere Charakteristika, wie ausgeprägte Variabilitäten der Herzfrequenz, des
Blutdrucks, der Atemfrequenz, der Atemtiefe sowie Schwankungen bei dem
Sauerstoffgehalt des Blutes 138,145. Eine verminderte Ansprechbarkeit auf
hyperkapnische und hypoxische Reize ist ebenso beschrieben worden9,81,136.
Bei gesunden Probanden findet man diese Ereignisse im NREM-Schlaf nicht.
Das Atmungsmuster und die Atemfrequenz sind gleichförmig, so dass keine
Sättigungsschwankungen oder Blutgasveränderungen auftreten63,88,128.
Im Laufe einer Nacht werden die unterschiedlichen Schlafstadien in der
gleichen Reihenfolge 3-5-mal durchlaufen. Ein solcher Schlafzyklus dauert
zwischen 70-90 Minuten und beginnt mit einer kurzen NREM-
Leichtschlafphase, die von einer NREM-Tiefschlafphase gefolgt wird. Danach
folgt eine REM-Schlafphase, die jeweils den Zyklus beendet. Insgesamt ergibt
sich eine durchschnittliche Schlafdauer von 7-8 Stunden 33. Mit zunehmender
Schlafdauer nehmen der Anteil des NREM-Tiefschlafs ab und der Anteil des

- 8 -
NREM-Leichtschlafs zu. Ebenso verlängern sich auch die REM-Schlafphasen 60.
Die Regulation der Atmung ist ein komplexes System mit sehr vielen
Einflussgrößen, das für eine perfekte Funktion auf hoch entwickelte
Regelmechanismen angewiesen ist.
In der Medulla Oblongata liegen inspiratorische und exspiratorische autonome
Neurone, durch deren rhythmische Aktivierung die an der Atmung beteiligten
Muskelgruppen stimuliert werden, um somit die Atmung zu gewährleisten 21.
Afferenzen aus dem kardiovaskulären System, periphere und zentrale
Chemorezeptoren, zum Beispiel Informationen über den Säure-Basen-Haushalt
sowie die arterielle Blutgase liefern beeinflussen die Frequenz und die Tiefe der
Atmung 33. Gegenüber dem Wachzustand ist im Schlaf sowohl die Atemtiefe als
auch die Frequenz erniedrigt und das Atemminutenvolumen sinkt
durchschnittlich um 10-15 %. Der Tonus der quergestreiften Muskulatur nimmt,
mit zunehmender Schlaftiefe und damit sinkender Vigilanz, stetig ab und führt,
bei Tonusverlust, zu einem erhöhten Widerstand der oberen Atemwege 14,32.
1.1.2.1.Koordination der oberen Atemwege im Schlaf
Die muskuläre Koordination und Synchronisation der an der Atmung beteiligten
nasalen, pharyngealen, laryngealen und tracheobronchialen Segmente
erfordert eine hohe zeitliche Präzision in Bezug auf die Intensität der
neuromuskulären Innervationen. Die Zeitverzögerung von proximal nach distal,
innerhalb derer die Aktivierung der benötigten Muskelgruppen abläuft, liegt im
Millisekundenbereich. Störungen der Synchronisation der an der Atmung
beteiligten Muskelgruppen im Schlaf können zu einer Beeinträchtigung der
Atmung im Schlaf bis hin zu Hypopnoen und Apnoen führen56. So ist zum
Beispiel eine auftretende Desynchronisation zwischen thorakaler und
abdomineller Atmung für die Obstruktive Schlafapnoe charakteristisch.
Die neuromuskulären Aktivierungen zu Beginn der Inspiration, die entlang des
Atemweges auftreten, entsprechen einer relativen Koordination. So erfolgt 92
msec vor dem Einsetzen der nasalen Strömung eine Nasenflügelerweiterung.
Der M. Genioglossus wird 70 msec vor Innervation des Zwerchfells aktiviert. Die
Laufzeitdifferenz zwischen alveolärer Entfaltung und der nasalen
Strömungsänderung beträgt ca. 43 msec, wobei die Nervenleitgeschwindigkeit

- 9 -
des N. phrenicus nur 8 bis 14 msec beträgt. Diese unterschiedlichen Latenzen
verdeutlichen die physiologische zeitliche Innervationsfolge der an der Atmung
beteiligten Muskeln. Im Schlaf wurden Änderungen der zeitlichen Beziehungen
in Form von Verzögerungen, einem Auseinanderlaufen oder einer Straffung der
Koordination beobachtet, was ebenfalls einen Einfluss auf die oberen
Atemwege hat56.
Die Weite der oberen Atemwege wird durch die Aktivität der oberen
Atmungsmuskulatur bestimmt. Sie kontrahierten sich während der Inspiration,
bewirkten so eine Protrusion des Unterkiefers, des Zungenbeins, der Zunge,
des Gaumens und öffneten so den Pharynx52,114. Die Aktivität dieser Muskeln
nimmt physiologischer Weise während des Schlafs ab.
Die folgende Tabelle zeigt welche Muskeln bei Inspiration und Exspiration
beteiligt sind:

- 10 -
Tabelle 1: Funktionsweise der an Inspiration und Exspiration beteiligten
Muskeln
Name und
Lokalisation
vermutete
Atmungsfunktion
Innervation Atmungs-
funktion
Schlaf Atemantwort auf
negative Drücke
Nase und Gaumen
Alae nasi Dilatation der Nase Facialis (VII) I ↓ ↑
Tensor veli palatini Versteift den Gaumen (?) Trigeminus (V) I oder
tonisch
↓ ↑
Levator veli palatini hebt den Gaumen Pharyngealer Plexus
(IX,X)
I ↑
Palatoglossus Öffnet retropalat. Raum
(?)
Pharyngealer Plexus
(IX,X)
I ↑
Palatopharyngeus Öffnet retropalat. Raum Pharyngealer Plexus
(IX,X)
?
Oraler Pharynx
Genioglossus Zungenprotrusion Hypoglossus (XII) I ↓ ↑
Hyoglossus Zungenkontraktion Hypoglossus (XII) ?
Styloglossus Zungenkontraktion Hypoglossus (XII) I?
Stylopharyngeus hebt die Zunge Glossopharyngeus (IX) I?
Constriktor kontrahiert den Pharynx Pharyngealer Plexus
(IX,X)
E? ↓
Digastric -anterior Öffnet den Pharynx Trigeminus (V) ?
Digastric - posterior Öffnet den Pharynx Facialis (VII) ?
Zungenbein
oben fixiert
Geniohyoideus Öffnet den Pharynx ? Hypoglossus (XII) I ↑
Mylohyoideus ? Trigeminus (V) ?
Stylohyoideus ? Facialis (VII) ?
unten fixiert
Thyrohyoideus ? Hypoglossus(XII) / C1 I
Sternohyoideus Öffnet den Pharynx ? Ansa cervicalis (C1-C3) I? oder
tonisch
↑
Sternothyroideus Öffnet den Pharynx ? Ansa cervicalis (C1-C3) I? ↑
Larynx
Cricoarytenoideus
post.
Abduziert die
Stimmbänder
Laryngeus reccurens (X) I ↓ ↑
Thyroarytenoideus Abduziert die
Stimmbänder
Laryngeus reccurens (X) E ↓
Cricoarytenoideus
lat.
Abduziert die
Stimmbänder
Laryngeus reccurens (X) ?
Arytenoideus Abduziert Stimmbänder Laryngeus reccurens (X) ?
Cricothyroideus spannt die Stimbänder externer Ast des I/E ↓ ↑
Laryngeus superior (X)
E – Expiration; I – Inspiration; I/E – In- und Expiration;
Horner et al.49

- 11 -
1.1.3. Definitionen und Klassifikationen von schlaf bezogenen
Atmungsstörungen
Atmungsstörungen, die aus einer pathologischen Wechselwirkung von Atmung,
Kreislauf sowie Schlaf entstehen, wurden 1976 wurde von Guilleminault et al.40
erstmals als Schnarch- Apnoe- Syndrom und später als schlafbezogene
Atmungsstörungen (SBAS) bezeichnet. Peter et al. belegte in seinen Studien,
dass man nach klinischen Gesichtspunkten zwischen SBAS mit Obstruktion der
oberen Atemwege und SBAS ohne Obstruktion der oberen Atemwege
unterscheiden kann 88,89. Die American Sleep Disorders Association (ASDA)
legt die derzeit gültige internationale Klassifikation der Schlafstörungen
(International Classification of Sleep Disorders, ICSD-2)2 fest und unterscheidet
bei Schlafbezogenen Atmungsstörungen das obstruktive Schlafapnoe-Syndrom
(OSAS), das zentrale Schlafapnoe-Syndrom (ZSAS) sowie das,
Schlafbezogene Hypoventilations- und Hypoxämie-Syndrom.
Als Maß für den Schweregrades der Atmungsstörung wird die durchschnittliche
Anzahl der Apnoen und Hypopnoen pro Schlafstunde, der Apnoe- Hypopnoe-
Index (AHI), angegeben.
Als Apnoe wird das Sistieren des oronasalen Luftflusses für eine Dauer von
mindestens 10 Sekunden bezeichnet 37,96. Auch im Schlaf gesunder Personen
können Apnoen auftreten. Diese, meistens im REM Schlaf oder beim
Einschlafen 64,140 auftretenden vereinzelte Apnoen, haben laut Guilleminault
keinen Krankheitswert, solange die Häufigkeit der Atmungsstörungen unter 5
Apnoephasen pro Stunde Schlafzeit beträgt 36. Als sicher pathologisch sind,
nach Lavie et al. 67, mehr als 10 Apnoen pro Stunde Schlafzeit.
Nach Durchführung einer Schlaflabormessung (Polysomnographie) wird der
Apnoe- Hypopnoe-Index (AHI) berechnet. Dieser ergibt sich aus der Summe
der Hypopnoen pro Stunde Schlafzeit (HI) und den Apnoen pro Stunde
Schlafzeit (AI), also AHI= HI+AI. Als normal einzustufen ist ein AHI unter 5, als
grenzwertig einzustufen ist ein AHI zwischen 5 und 10 und ein AHI >10 wird als
pathologisch betrachtet 32,88.
Tritt während des Schlafes eine Weckreaktion mit einer Mindestlänge von 3
Sekunden, verbunden mit einem Frequenzanstieg im EEG und einer
Aktivitätszunahme im EMG auf, wird dies als ein Arousal klassifiziert 1. Ein

- 12 -
Arousal terminiert nicht nur die verschiedenen Apnoen sondern kann auch
physiologischerweise während des Schlafes gesunder Patienten auftreten33.
1.1.4. Epidemiologie
In Studien zur Prävalenz der schlafbezogenen Atmungsstörungen variiert diese
erheblich. Die Prävalenz der schlafbezogenen Atmungsstörungen in der
gesamten US-Amerikanischen Bevölkerung betrug 1997 nach einer Schätzung
der American Disorder Sleep Association 1-2 % 2. Bei einer Studie von Lavie
an 1502 Industriearbeitern betrug die Prävalenz 1,3 % 67,68, allerdings unter der
Voraussetzung, dass der AHI > 10 war. In einer Arbeit von Peter et al. welche
das Vorliegen von pathologischen Atmungsmustern untersuchte wurde bei
männlichen Industriearbeitern eine Prävalenz von 10 % ermittelt 87,94. Young et.
al. fand bei ihrer Untersuchung heraus, dass schätzungsweise 2% der
weiblichen und 4% der männlichen Bevölkerung unter der schwersten
Ausprägung der OSA leiden, wobei das Auftreten von leichten Formen der
oberen Atemwegsobstruktion und Hypoventilation im Schlaf viel höher liegt.144
1.1.5. Pathophysiologische Veränderungen bei obstru ktiven
schlafbezogenen Atmungsstörungen
Bei obstruktiven schlafbezogenen Atmungsstörungen (OSAS) kommt es zu
einer kompletten oder inkompletten Verlegung der oberen Atemwege. Da ein
Aktivitätsverlust der pharyngealen Muskeln während des Schlafs physiologisch
ist, müssen weitere Faktoren hinzukommen, um eine nächtliche
Atmungsstörungen zu verursachen. Es konnte gezeigt werden, dass sowohl
morphologische als auch koordinative Faktoren bei der Pathogenese der OSAS
eine Rolle spielen. Anatomische Engen im Bereich der oberen Atemwege
können in Verbindung mit dem im Schlaf abnehmenden Muskeltonus
Obstruktionen verursachen. Ebenso kann eine erhöhte Kollapsneigung der
Muskulatur der oberen Atemwege für die Entstehung obstruktiver
Atemstörungen verantwortlich sein. Schneider et al. konnten zeigen, dass
sowohl jeder Faktor allein aber auch eine gegenseitige Beeinflussung der
Faktoren zu obstruktiven Schlafstörungen führt.115

- 13 -
1.1.6. Anatomische Charakteristika des Obstruktiven Schlafapnoe
Syndroms
Mehrere Studien konnten einen Zusammenhang zwischen anatomischen
Weichteil-charakteristika sowie skelettalen Dimensionen und obstruktiver
Schlafapnoe belegen 4,43,58,70,108,134,146. Welche Parameter welchen Einfluss auf
die Genese der obstruktiven Schlafapnoe haben, ist jedoch noch nicht sicher
belegt worden. Man kann bei anatomischen Dysmorphien zwischen knöchernen
und weichteil-betreffenden Veränderungen unterscheiden:
Weichteilcharakteristika:
° Zungenveränderungen (Makroglossie)
° Weichteilhyperplasie des Pharynx, usw.
° Verlängertes und verdicktes Gaumensegel
° Adenoid- und Tonsillenhyperplasie
Skelettale Charakteristika:
° Veränderungen der Schädelbasis
° Inferiore Stellung des Zungenbeins
° Maxilläre und /oder mandibuläre Retrognathie/Mikrognathie
1.1.7. Neurologische Charakteristika des Obstruktiv en Schlafapnoe
Syndroms
Zusätzlich zu anatomischen Charakteristika ist die Durchgängigkeit der oberen
Atemwege auch von neuromuskulären Faktoren abhängig. Zahlreiche
neuromuskulären Reflexe, die bei einer oberen Atemwegsobstruktion ausgelöst
werden, stimulieren die dilatierenden Muskeln der oberen Atemwege und
stellen einen offenen Zustand wieder her75.
Es wurde im Tierexperiment gezeigt dass Reflexe, pulmonale Rezeptoren,
neuromuskuläre Kontrolle, obere Atemwegsrezeptoren sowie auch
Chemorezeptoren einzeln wie auch in Kombination die Aktivität der
dilatatorischen Muskulatur der oberen Atemwege beeinflussen.
An isolierten oberen Atemwegen von Tieren wurden Studien durchgeführt um
die Funktion der oberen Atemwege zu erklären. Es konnte gezeigt werden,

- 14 -
dass die Kollapsneigung der oberen Atemwege durch eine komplexe Interaktion
von neuromuskulären und anatomischen Faktoren beeinflusst wird. Diese
Experimente verdeutlichten den Effekt von Veränderung einer neuromuskulären
Aktivität auf die pharyngeale Kollapsneigung und die Dynamik des
pharyngealen Luftflusses. 110,111,125
Werden Schlafapnoepatienten und gesunde Kontrollpersonen nach einem
standardisiertem Protokoll unterschiedlichen Druckwerten im Pharynx während
des Schlafes ausgesetzt (positive und negative Druckwerte), kommt es bei
OSAS-Patienten vergleichsweise zu einem rascheren Kollaps der oberen
Atemwege. Im Detail kollabieren die oberen Atemwege bei OSAS-Patienten
bereits bei positiven oder gering negativen Druckwerten, während gesunden
Kontrollpersonen erst bei deutlichen Unterdruckwerten einen pharyngealen
Kollaps im Schlaf aufweisen86.
Verschiedene andere Untersuchungen zeigten, dass dem M. genioglossus eine
große Bedeutung in der Genese der schlafbezogenen Atmungsstörungen
zukommt 53,75,106,113. Es wurde bei einer Aktivitätsmessung des Muskels
festgestellt, dass bei OSAS-Patienten der Muskeltonus im Schlaf verringert ist.
Paradoxerweise werden am Tage vergleichsweise höhere EMG-Aktivitäten
gemessen, welche als kompensatorische Überaktivität interpretiert
werden.53,75,95.
In verschiedenen Studien konnte festgestellt werden, dass bei Patienten mit
obstruktiven Atmungsstörungen das kollabile Segment in unterschiedlichen
Abschnitten des Pharynx lokalisiert ist 50,52,106,127. Außerdem wurde
nachgewiesen, dass eine Schlafstadienvariabilität des kollabilen Segments
vorliegt. Shepard et al. und Boudewyns et al. konnten nachweisen, dass im
REM-Schlaf gegenüber dem NREM-Schlaf eine Tendenz zu einem mehr kaudal
lokalisierten Kollaps vorhanden ist 13,127. Häufig befindet sich der Kollaps an
einer Stelle mit einer anatomischen Veränderung, beispielsweise ist der Ort des
Atemweg-Kollapses bei Patienten mit vergrößerter Zunge oder einem
kaudalwärts verlagerten Zungenbein vermehrt im Oropharynx und/oder im
Hypopharynx lokalisiert, während bei Patienten mit einem verdicktem
Gaumensegel der Kollaps im Bereich des Nasopharynx auftritt52,85.

- 15 -
1.1.8. Symptome bei schlafbezogenen Atmungsstörunge n
Im vorangegangen Text wurde deutlich, dass die Apnoephasen mit der
anschließenden Weckreaktion (Arousal) zu einer Fragmentation des Schlafes
führen. Kommt es zu einer deutlichen Erhöhung von Arousals (>100/Nacht),
führt die Schlaffragmentation und die Störung der Schlafarchitektur zu einer für
Schlafapnoepatienten typischen Symptomatik 33,147.
Die Hypersomnie (Tagesschläfrigkeit) und die Monotonie-Intoleranz sind
Kardinalsymptome. Die Ausprägungen reichen von leichten
Konzentrationsmängeln bis hin zu imperativem Einschlafzwang bei einer
deutlich gesteigerten Monotonieintoleranz 18. Die Arbeitsgruppe von Cassel et
al. konnte zeigen, dass bei Schlafapnoepatienten ein signifikant erhöhtes
Unfallrisiko besteht 16. Als weitere Beschwerden werden trockener Rachen,
allgemeine Leistungsminderung, Libido- und Potenzverlust, morgendliche
Unausgeschlafenheit bis hin zu Persönlichkeitsveränderungen und
Stimmungsschwankungen angegeben 89,93,132.
Bei der obstruktiven Form der schlafbezogenen Atmungsstörungen ist das
unregelmäßige laute Schnarchen das Hauptsymptom während der Nacht. Dies
wird zumeist fremdanamnestisch durch den Ehepartner oder Dritte
beschrieben. Der Patient selbst berichtet von Durchschlafstörungen, häufigen
Schlafunterbrechungen, Nykturie sowie vermehrter Neigung zu nächtlicher
Hyperhidrose 89,93.
Eine Reihe von internistischen Krankheiten lassen sich mit schlafbezogenen
Atmungsstörungen in Verbindung bringen. Dazu zählen
Herzrhythmusstörungen, arterielle und/oder pulmonale Hypertonie,
Herzinsuffizienz und respiratorische Insuffizienz18,82,97,98,100. Hung et al. fanden
zudem heraus, dass die Erhöhung des Myocardinfarktrisikos für Patienten mit
einem Apnoeindex über 5,3 um das dreiundzwanzig fache höher liegt als bei
Gesunden 51. Diese Erkrankungen sind meist langfristige Auswirkungen von
schlafbezogenen Atmungsstörungen, da bei diesen Krankheitsbildern
Veränderungen in den arteriellen Blutgasen und der Hämodynamik des Blutes
auftreten 10,39,97,101,129.
Tachykarde Rhythmusstörungen wurden bei 57 bis 70 % 10,39,76, bradykarde
Herzrhythmusstörungen jeglicher Art bei 5 – 10 % 25,35,48,61 der Patienten mit
schlafbezogenen Atmungsstörungen beschrieben. Ein pulmonaler Hochdruck

- 16 -
wurde bei 20 %, ein systemarterieller Hochdruck wurde bei 50 % der Patienten
beobachtet 3,91,98.
Anatomische Charakteristika spielen eine wichtige Rolle in der Entstehung von
obstruktiven Schlafstörungen. Hierzu gehören eine charakteristisch veränderte
Fettverteilung bei Übergewicht, eine Zunahme des Halsumfangs, eine
veränderte pharyngeale Querschnittsform, eine Zunahme des
parapharyngealen Fettgewebes sowie knöcherne Charakteristika des
Gesichtsschädels (z.B. Retrognathie und Mikrognathie). Somit muss nicht nur in
der Fachrichtung der Inneren Medizin (Pneumologie, Kardiologie,
Endokrinologie, etc.), sondern auch in der Neurologie, Hals- Nasen-
Ohrenheilkunde oder Mund- Kiefer- und Gesichtschirurgie auf Symptome von
schlafbezogenen Atmungsstörungen geachtet werden. 41,77,82,89,92.
1.2. Diagnostik schlafbezogener Atmungsstörungen
Bei Verdacht auf das Vorliegen schlafbezogener Atmungsstörungen werden
gegenwärtig zunächst ambulante Screeningverfahren eingesetzt 31,84.
Sollte sich nach deren Auswertung ein Verdacht auf das Vorliegen
schlafbezogener Atmungsstörungen ergeben, erfolgt eine standardisierte
polysomnographische Diagnostik in einem akkreditierten Schlaflabor.83 Um
internistische Begleiterkrankungen auszuschließen oder zu diagnostizieren
sollte zudem eine Lungenfunktionsprüfung, ein Langzeit-EKG, eine Langzeit-
Blutdruckmessung sowie eine Blutgasanalyse durchgeführt werden. Zur
Abklärung von anatomischen Besonderheiten sollte im Verdachtsfall außerdem
eine konsiliarische Untersuchung in der Abteilung für Mund- Kiefer- und
Gesichtschirurgie und in der Abteilung für Hals- Nasen- und Ohrenheilkunde
erfolgen 44,90.
1.3. Quantifizierung der pharyngealen Kollapsibilit ät im Schlaf
(kritischer pharyngealer Verschlussdruck = P crit )
Bisher werden Methoden zur Engstellendiagnostik und Erfassung anatomischer
Determinanten des obstruktiven Schlafapnoe Syndroms im Wachzustand im

- 17 -
klinischen Alltag eingesetzt (Bronchoskopie, Kernspintomographie, etc.). Im
Schlaf ergibt sich hingegen die Schwierigkeit, dass nur die Bestimmung des
AHI und der Sauerstoffentsättigungen die Krankheitsschwere beurteilt, aber
keine quantitative Methode zur Erfassung der Funktionsstörung der oberen
Atemwege existiert. Eine praktikable Meßmethode zur Erfassung der
Kollapsneigung der Atemwege im Schlaf wurde von Schwartz et. al. an der
Johns Hopkins Universität in Baltimore entwickelt und stellt einen wichtigen
Bestandteil dieser Untersuchung dar30,122,124. Es handelt sich um die Messung
des so genannten kritischen pharyngealen Verschlussdruckes (Pcrit). Diese
Methode basiert auf der Messung der Druck-Flussbeziehungen der oberen
Atemwege. Als entscheidender methodischer Unterschied zu herkömmlichen
Druckflussmessungen, werden nicht die Gesetzmäßigkeiten eines starren
Röhrensystems verwendet. Es werden die Druckflussbedingungen in flexible
Röhren nach den Kriterien des Starling Resistors berechnet, wobei der Luftfluss
durch den Quotienten zwischen Druckabfall und Widerstand bestimmt wird. Die
Druckverhältnisse im Pharynx und dessen Kollapsibilität kann mit dem Prinzip
des so genannten Starling Resistors (Knowlton und Starling 1912) beschrieben
werden.

- 18 -
1.3.1. Der Starling-Resistor
Die Beobachtungen bei den Tierexperimenten haben zur Entwicklung des
Starling-Resistor Modells geführt, mit dem die Funktion der oberen Atemwege
unter verschiedenen Bedingungen im Schlaf auch beim Menschen erklärt
werden kann. 28,30 Hierbei wird der Pharynx als ein zum Kollaps neigendes
Segment modelliert, das vom Gewebedruck der Umgebung und zwei starren
Segmenten begrenzt wird, ein kraniales Segment im Bereich von Mund und
Nase, auch oberes Segment (OS) genannt, sowie ein distales Segment in den
Bereichen von Trachea und Lunge, auch unteres Segment (US) genannt. Ob
die Atemwege nun komplett offen, partiell offen oder komplett verschlossen sind
wird durch die Druckverhältnisse zwischen dem oberen und unteren Segment
und dem Gewebedruck der Umgebung Pcrit bestimmt.
Abhängig von unterschiedlichen Drücken kann es nun drei Zustände geben, die
den Luftfluss und die dazugehörige Klinik erklären.
Zustand 1 (POS >PUS> Pcrit), Zustand 2 (POS >Pcrit >PUS) und Zustand 3 (Pcrit
>POS> PUS).
Abbildung 1: Das Starling-Resistor Modell

- 19 -
Die Normalatmung ohne reduzierten Atemfluss wird durch Zustand 1 erklärt, bei
dem der Luftfluss durch das Ohm’sche Gesetz bestimmt werden kann: V=(POS -
Pcrit) / RRS.
Der Druck des oberen Segments (POS) entspricht dabei dem der Umgebung, ist
damit Null und der Widerstand des respiratorischen Systems ( RRS ) setzt sich
aus dem Widerstand der Lunge und dem der Nase zusammen.
Es ist möglich mehr Atemfluss zu erzeugen wenn der Patient aufgrund eines
höheren Atemantriebs mehr Atemfluss benötigt, was eine Abnahme von PUS
bedeutet und somit einen höheren Druckgradienten (POS-PUS).
In Zustand 2 und 3 kann der Atemfluss nicht mehr durch eine Zunahme des
Atemantriebs, welches sich in einer Abnahme von PUS zeigt, gesteigert werden.
Beim Zustand 2, der Schnarchen beinhaltet, ist der maximale Atemfluss Vimax
abhängig vom Druckgradienten zwischen POS und Pcrit (VIMAX=(POS- Pcrit)/RUA)
wobei RUA sich durch den nasalen Widerstand und dem dynamischen Kollaps
der oberen Atemwege RUA aufbaut.
Eine wesentliche Erhöhung des Atemflusses kann entsprechend der Gleichung:
V=(POS - Pcrit) / RRS nur durch eine Erhöhung des POS oder durch eine
Verminderung des Pcrit infolge neuraler Aktivierung erreicht werden. Eine
Erhöhung des POS wird therapeutisch durch eine Überdruckbeatmung mittels
Nasenmaske (CPAP) erreicht, während eine Verminderung des Pcrit durch
Gewichtsreduktion und chirurgische Verfahren zu erzielen ist.
Im Zustand 3, der obstruktiven Apnoe, bei der die Atemwege komplett
verschlossen sind, sind Veränderungen des POS und PUS irrelevant.
Wie bereits angedeutet entsteht durch den oben beschriebenen Kollaps der
pharyngealen Muskulatur das Schnarchen. Die Kollapsneigung der beteiligten
Muskulatur kann gemessen werden und wie oben erläutert als kritischer
Verschlussdruck (Pcrit) angegeben.
Der Pcrit ist definiert als der intraluminale Druck der aufgewendet werden muss,
um eine pharyngeale Okklusion durch kompletten Kollaps und damit eine
obstruktive Apnoe zu verursachen.
Bei wachen Patienten müssen starke subatmosphärische Drücke von -50
cmH2O und weniger erzeugt werden um den Pharynx zum Kollaps zu bringen.
Negative Drücke führen im Wachzustand zu einer reflektorischen neuronalen
Aktivierung der pharyngealen Muskulatur und somit zu einer

- 20 -
Muskelanspannung. Im Schlaf reichen leichte subatmosphärische Drücke aus
um die Atemwege zum Kollaps zu bringen, da diese Aktivierung abgeschwächt
ist oder gänzlich fehlt. Bei Nichtschnarchern liegt der Pcrit in der Regel bei -10
cmH2O und erhöht sich mit dem Schweregrad der Kollapsneigung.
Gemäß diesen Überlegungen kann man somit den kritischen pharyngealen
Verschlussdruck Pcrit als quantitatives Maß für die Kollapsneigung des Pharynx
benutzen52,56,124.
1.3.2. Klinische Untersuchungen zum kritischen phar yngealen
Verschlussdruck
Schwarz et al. (1988) untersuchten das Verhalten des kritischen pharyngealen
Verschlussdruckes Pcrit bei 7 Personen, die anamnestisch und klinisch keine
Anzeichen für das Vorliegen schlafbezogener Atmungsstörungen zeigten 124.
Experimentell wurden im NREM-Schlaf über eine Nasenmaske verschiedene
subatmosphärische Drücke appliziert und mittels eines Pneumotachographen
die Flussvariationen aufgezeichnet 124. Hierbei ergab sich bei Normalpersonen
ein Pcrit von -13,3 ± 3,2 cm H2O. In Untersuchungen von Smith et al. an 6
Patienten mit Schlafapnoe wurde dagegen ein Pcrit von +3,3 ±3,3 cm H2O
beschrieben, d.h. bei diesen Patienten kam es schon bei positiven
intraluminalen Drücken zu einem Kollaps der oberen Atemwege. Gleadhill et al.
und Gold et al. konnten außerdem bei ihren Untersuchungen zeigen, dass
signifikante Unterschiede in der Kollapsibilität von Schlafapnoepatienten,
habituellen Schnarchern und Normalpersonen bestehen 28,30.

- 21 -
Abb2. Das Ausmaß der pharyngealen Kollapsibilität korreliert mit der Ausprägung der
schlafbezogenen Atmungsstörungen
Schwartz AR, Smith PL, Kashima HK, et al. Respiratory function of the upper airways. In Murray
JF, Nadel JA, Textbook of respiratory medicine. 2nd edition Philadelphia: WB Saunders, 1994;
1451-70
Die Ergebnisse dieser Untersuchungen lassen den Schluss zu, dass die
Kollapsneigung des Pharynx, die über den kritischen pharyngealen
Verschlussdruck Pcrit ermittelt wurde, den Schweregrad der SBAS wiedergibt28.
Diesbezüglich konnten Gold et al. nachweisen, dass bei Schlafapnoepatienten
der Pcrit im positiven Bereich liegt und sich bei Hypopnoen und Schnarchen eine
Abnahme des Pcrit auf 0 bis -4 cm H2O zeigt. Bei Normalpersonen liegt er
bereits in eine subatmosphärischen Bereich zwischen -8 und -10 cm H2O 30. Ein
ansteigender Pcrit korreliert somit mit einem zunehmenden Schweregrad der
pharyngealen Obstruktion.
Durch die unterschiedlichen Funktionszustände der oberen Atemwege,
quantitativ bestimmt durch die Pcrit-Messung, können Normalpersonen,
Schnarcher, Hypopnoiker und Apnoiker, voneinander differenziert werden.
1.3.3. Determinanten der pharyngealen Kollapsibilit ät
Verschieden Einflussgrößen können die Kollapsibilität des Pharynx
beeinflussen. Neben schon genannten mechanischen Einflussgrößen,

- 22 -
Vigilanzabhängigkeit, neuronalen Faktoren und anatomischen Faktoren, ist
auch an eine Körperlageabhängigkeit des pharyngealen Kollapses zu denken.
Es ist bekannt, dass pharyngeale Obstruktionen häufiger in Rücken- als in
Seitenlage beobachtet werden, was sich oft durch einen geringeren Apnoe-
Hypopnoe-Index in Seitenlage dokumentieren lässt 15,143. McKenzie et al.
beschrieben bei OSAS-Patienten in Rückenlage einen höheren Pcrit als in
Seitenlage. Boudewyns et al. konnten dies mit ihrer Arbeit bestätigen, wobei die
Differenz des Pcrit zwischen Rücken- und Seitenlage etwa 3 cm H2O betrug 12.
Dabei wird bei einem Wechsel von Rücken- auf die Seitenlage eine
Verlängerung des Muskelschlauchs der oberen Atemwege festgestellt, der eine
Tonuserhöhung der Atemwegsmuskulatur bewirkt 74. Die Straffung der oberen
Atemwegsmuskulatur hat eindeutig eine Reduktion der pharyngealen
Kollapsneigung zur Folge.
In tierexperimentellen Untersuchungen an isolierten oberen Atemwegen wurde
ein signifikanter Abfall des Pcrit beschrieben, wenn der Muskelschlauch der
oberen Atemwege verlängert wurde 80,110,120,131. Mechanische Faktoren
scheinen also die Kollapsibilität des Pharynx nicht unerheblich zu beeinflussen.
Ebenso wird dem Körpergewicht und der Körperfettverteilung ein negativer
Einfluss auf die Kollapsibilität und den damit verbundenen Atmungsstörungen
zugeschrieben 69,78,119,137. Der Body Mass Index (BMI) setzt das Körpergewicht
in Relation zur Körpergröße. Ein vergrößerter Halsumfang geht oft mit einer
Vermehrung des Weichteilgewebes einher und kann so zu einem erhöhten
Umgebungsdruck auf die oberen Atemwege führen und somit den Pcrit erhöhen 112,119. Bei einem Gewichtsverlust kommt es zu einer Abnahme des Pcrit und
dies führt zu einer entscheidenden Senkung der Kollapsibilität 119.
Studien von Schwartz et al. zeigten, dass durch die Stimulation von
verschiedenen Muskeln des Pharynx es zu einer Zunahme des inspiratorischen
Luftflusses und zu einer Abnahme des Pcrit kommt 118,125,130. Besonders eine
Aktivierung des M. genioglossus, der eine Protrusion der Zunge bewirkt, führt
zu einer Kollapsibilitätsabnahme118. Diese tierexperimentelle Studie eröffnet
eine neue Therapiemöglichkeit zur Behandlung der obstruktiven Schlafapnoe,
welche Grundlage dieser Arbeit ist.

- 23 -
Abb.3: Mögliche Einflussgrößen der pharyngealen Kollapsibilität
Neuromuskuläre Anatomische Mechanische
Faktoren Charakteristika Faktoren
Pharyngeale Kollapsibilität
Körperfett- Vigilanz Blutgase
Verteilung
1.4. Therapie schlafbezogener Atmungsstörungen
Das therapeutische Vorgehen beinhaltet nichtoperative und operative
Maßnahmen. Die Goldstandardbehandlung stellt die nasale nächtliches
Druckluftschienung der oberen Atemwege im Schlaf dar (Continuous Positive
Airway Pressure – CPAP). Die Therapieentscheidung wird in Abhängigkeit von
der Art und der Ausprägung der schlafbezogenen Atmungsstörung getroffen.
Außerdem müssen das Risikoprofil und die subjektiven Beschwerden des
Patienten einbezogen werden. Erst dann sollte die Therapie, konservativ oder
chirurgisch, individuell auf den Patienten abgestimmt werden.

- 24 -
1.4.1. Nicht-operative Verfahren
Mechanische Überdruckbeatmung:
Die wohl am meisten verbreitete Therapieform für obstruktive Schlafapnoe ist
die von Sullivan 1981 eingeführte kontinuierliche nasale Überdruckbeatmung
(nasal Continuous Positive Airway Pressure, nCPAP) 134,135.Der über eine
Nasenmaske applizierte Luftstrom bewirkt eine pneumatische Schienung und
verhindert somit den Kollaps der oberen Atemwege 7,134. Der therapeutisch
notwendige Druck wird allgemein in einem Schlaflabor unter
polysomnographischer Überwachung individuell für jeden Patienten ermittelt.
Ziel dieser Druckeinstellung ist die vollständige Reduktion der schlafbezogenen
Atmungsstörungen.
Dass die nCPAP-Therapie derzeit auch als „Goldstandard“ bezeichnet wird,
belegt die Effektivität in Bezug auf eine vollständige Beseitigung der
Atemwegsverschlüsse 8,62. Die Anwendungsdauer dieser Therapieform ist in
der Regel lebenslang und eine Langzeitakteptanz besteht bei 65-80 %
angegeben 6,62,103,105,109.
Benötigen Patienten mit obstruktiver Schlafapnoe sehr hohe therapeutische
Drücke oder liegen schwere Herz- oder Lungenerkrankungen vor so kann man
auch ein nBIPAP-Gerät (nasal Bilevel Positive Airway Pressure, nBIPAP)
einsetzen 7, das mit unterschiedlichen in- und expiratorischen Druckniveaus
arbeitet. Ebenso wird die nBIPAP Beatmung auch bei primären und sekundären
Hypoventilationen und zentralen Apnoen im Schlaf verwendet. Alternativ wird
auch eine volumenkontrollierte intermittierende positive Druckbeatmung
(Intermittent Positive Pressure Ventilation, IPPV) durchgeführt.
Die Compliance der Patienten die Überdruckbeatmung zu akzeptieren liegt bei
50 – 80 %. Das bedeutet, dass bis zu 50 % therapiebedürftiger schlafbezogener
Atmungsstörungen mangelhaft oder gar nicht behandelt werden. Daher sind
auch alternative Behandlungsformen notwendig86.
Orale Prothesen:
Eine weitere Therapie von schlafbezogenen Atmungsstörungen ist die
Benutzung von intraoralen Prothesen (Esmarchprothese, Zungenextensoren),
die eine Unter-kiefervorverlagerung bewirken sollen. Es kommt bei Orthodesen
vermehrt zu prothesenspezifischen Komplikationen (Schmerzen,

- 25 -
Schwierigkeiten im Mandibular-gelenk, Hypersalivation), so dass nur 25 - 40 %
der so behandelten Patienten diese Therapie dauerhaft tolerieren 17,34,116.
Leichte schlafbezogene Atmungsstörungen kann man mit dieser Therapie
behandeln, wobei es in 50 % der Fälle es zu einer Reduktion kommt, aber keine
vollständige Behebung schlafbezogener Atmungsstörungen zu erwarten ist 34,116. Bei schweren obstruktive schlafbezogenen Atmungsstörungen sind
Orthodesen meist ohne ausreichenden therapeutischen Effekt.
1.4.2. Operative Verfahren:
Tracheotomie:
Als Ultima ratio bei lebensbedrohlichen Zuständen (Hypoventilation,
Herzinsuffizienz, nicht therapierbare Adipositas per magna, etc.) wenn andere
Beatmungsformen oder Therapiemöglichkeiten versagen, wird eine
Tracheotomie durchgeführt, 34,45,65,139.
Umstellungsosteotomien:
Die Oberkiefer/Unterkieferosteotomie oder isolierte Unterkieferosteotomie
zeigen, bei strenger Indikationsstellung (z.B. bei Retrognathie oder
Mikrognathie bei Fehlen ausgeprägter Adipositas), Erfolgsraten von 90 % 19,34,45-47,73,102,107,133. Neben der routinemäßigen Polysomnographie müssen sich
die Patienten auch einer Untersuchung in der Mund- Kiefer- und
Gesichtschirurgie unterziehen, bei der die Bisslage sowie die Skelett- und
Weichteilstrukturen mittels eines Fernröntgenseitenbildes 71,72 beurteilt werden.
Wird eine Enge des Pharynx oder eine Retroposition der Kiefer nachgewiesen,
kann die Indikation zur Korrekturosteotomie gestellt werden 44,45,71. Die
Retroposition kann im sagittalen Schnitt durch verschiedene kephalometrische
Parameter bestimmt werden.
Die sog. retromolare sagittale Osteotomie ist das OP-Standardverfahren. Das
Ziel der Operation ist nicht nur die durch die Vorverlagerung des Unterkiefers
resultierende Vorverlagerung der daran befestigten Weichteile mit
mechanischer Erweiterung des Pharynx, sondern auch die funktionelle
Beeinflussung der daran ansetzenden Atemmuskulatur und die Herstellung
einer neutralen Bisslage 45,47.

- 26 -
Uvulopalatopharyngoplastik (UPPP):
Wegen der geringen Erfolgsrate von 50 % ist die Indikation zur Uvulopalato-
pharyngoplastik sehr sorgfältig zu stellen 89,121. Welche individuelle Parameter
für einen Erfolg oder Misserfolg der Operation verantwortlich sind, ist noch nicht
abschließend geklärt 11,102,142. Um überhaupt einen Therapieerfolg belegen zu
können, ist eine prä- und postoperative polysomnographische Untersuchung 88,89 erforderlich.
Eine effektive Therapie führt zur Beseitigung der Beschwerden sowie zur
Normalisierung der Atmung im Schlaf. Veränderungen, die durch das
Krankheitsbild schlafbezogener Atmungsstörungen entstanden sind (arterielle
und pulmonale Hypertonie, Herzrhythmusstörungen, respiratorische
Insuffizienz, Herzinsuffizienz) können sich ebenso normalisieren.5,99,131,141. Bei
konsequenter Anwendung der nächtlichen Überdrucktherapie kann die
Mortalität und die Morbidität bei Schlafapnoe-Patienten wieder auf die
Altersnorm gesenkt werden 41,82.
1.5. Innovative Behandlungsansätze: Elektrische Sti mulation der oberen
Atemwege
In ersten Studien wurde untersucht, inwieweit die muskuläre Stimulation
oropharyngealer Muskeln zur Beseitung oberer Atemwegsobstruktionen
beitragen kann. Es wurde insbesondere untersucht, welche Muskeln aktiv am
Offenhalten der oberen Atemwege insbesondere im Schlaf beteiligt sind. Im
Weiteren wurde experimentell eine Stimulation isolierter Muskelgruppen
untersucht125. Es wurde beabsichtigt eine Beseitigung des oberen
Atemwegkollapses bei ungestörten Schlafbedingungen zu erreichen. Dabei
konzentrierte sich das Interesse zunehmend auf die neuromuskuläre
Stimulation des M. genioglossus, dem anatomisch und funktionell eine
Schlüsselrolle bei der Genese obstruktiver schlafbezogener Atmungsstörungen
zukommt. Initial erfolgte in ersten Untersuchungen die elektrische Stimulation
des M. genioglossus über transkutan-perkutane und intraoral platzierte
Elektroden. Hierbei traten methodische Probleme in Bezug auf die selektive
Stimulation des M. genioglossus auf. Zum einen konnte transkutan der
Genioglossus nicht selektiv stimuliert werden, zum anderen kam es durch die

- 27 -
kutane Stimulation zusätzlich zur ungewollten muskulären Aktivierung
antagonistisch arbeitender Muskelgruppen (Musculus hyoglossus und
styloglossus). Dieser unselektive Summationseffekt einer kombinierten,
unilateralen Innervation der Mm. styloglossus, hyoglossus und genioglossus
bewirkte insgesamt eine Verkleinerung des pharyngealen Durchmessers, der
Folge einer Retraktion der Zunge war. Pneumotachographisch zeigte sich eine
Atemflussverminderung im Vergleich zum unstimulierten Zustand. Des
Weiteren traten bei transkutaner Reizung vermehrt Weckreaktionen (Arousal)
auf. Um eine effektive elektrische Stimulation zu erzielen wurden hohe
Stimulationsparameter (Amplitude, Frequenz, Impulsdauer etc.) benötigt.
Hierdurch kam es unerwünscht zur Erregung sensibler afferenter
Schmerzfasern, die zu kortikalen Aktivierungsreaktionen (Arousal) führten.
Die beobachtete Erhöhung des Atemflusses war Folge einer nicht-spezifischen
Aktivierung und Tonisierung der oropharyngealen Muskulatur, wie sie
physiologischerweise beim Übergang vom Schlaf- zum Wachzustand auftritt.
Die elektrophysiologischen Ableitungen im EEG bestätigten die Arousal im
Rahmen der neuromuskulären Stimulation.
In einer Untersuchung von Schwarz et al. gelang es durch methodische
Verbesserungen, selektiv antagonistisch kontrahierende Muskelgruppen
abwechselnd zu stimulieren. Experimentell gelang es durch die Anwendung
intraoral-intramuskulärer Elektroden, selektiv einerseits die Mm. hyoglossus und
styloglossus (Zungenretraktion) und andererseits den M. genioglossus
(Zungenprotrusion) zu stimulieren.118 Durch niedrigere
Stimulationsschwellenwerte (Spannung, Frequenz, Impulsdauer) war dies ohne
eine polysomnographisch nachweisbare Beeinträchtigung der Schlafqualität
möglich. Die elektrische Stimulation erfolgte mittels dünner, teflonbeschichteter
Elektroden, die intraoral-intramuskulär platziert wurden. Im Wachzustand wurde
über eine Modifikation der Spannung, Impulsdauer und Frequenz eine effektive
“Titration” des elektrischen Stimulus erreicht. Hierbei wurde der niedrigste,
effektive Schwellenwert sämtlicher Stimulationsparameter ermittelt, der ohne
Angabe subjektiver Beschwerden zu einer maximalen Zungenprotrusion führte.
Durch Stimulation unterschiedlich lokalisierter Elektroden ermöglichte im
Wachzustand die Kontrolle der Muskelkontraktion differenter Muskelgruppen.
Auf diese Weise konnte ein Stimulationsmuster im Schlaf geprüft und sein

- 28 -
Effekt auf die Zungenbewegung und den pharyngealen Querschnitt kontrolliert
werden. Eine Stimulation der im posterioren gingivolabialen Sulcus platzierten
Elektroden, führte zu einer Kontraktion des Mm. hyoglossus und styloglossus.
Als Folge konnte eine ipsilaterale Retraktion der Zunge beobachtet werden.
Nach Stimulation von lateral des Frenulums platzierten Elektroden ließ sich der
M. genioglossus selektiv kontrahieren, wodurch eine kontralaterale Protrusion
resultierte. 54,55
Die bisher durchgeführten Grundlagenuntersuchungen konnten zeigen, dass
die direkte Stimulation des M. genioglossus und die neurale Stimulation des
Nervus hypoglossus zu einer Abnahme der pharyngealen Kollapsibilität und
einer konsekutiven inspiratorischen Flussverbesserung führen kann, ohne
Weckreaktionen herbeizuführen.
Ziel dieser Arbeit ist es, die Effektivität eines neukonstruierten inspiratorisch-
gesteuerten Schrittmachersystems zur Behandlung der OSA zu untersuchen 117. Hierfür wurden die NREM-Schlafstadien gewählt, da sie über einen
längeren Zeitraum mit ihren verschiedenen Ausprägungen anzutreffen sind um
die notwendigen Messversuche zu absolvieren.

- 29 -
2. Fragestellung
In dieser Arbeit wird der therapeutische Effekt der unilateralen elektrischen
Stimulation des M. genioglossus durch einen Hypoglossus - Schrittmacher bei 8
Patienten einer Multi-Center-Studie untersucht. An der Philipps-Universität
Marburg wurde aus diesem Kollektiv einem Patienten ein Schrittmachersystem
implantiert.
Im Weiteren sollen folgende Fragestellungen beantwortet werden:
1. Welche Effekte hat die unilaterale elektrische Stimulation des N.
hypoglossus auf die polysomnographischen Parameter im Schlaf: Apnoe-
Hypopnoe-Index (AHI), mittlere basale Sauerstoffsättigung (O2 Basis),
niedrigste Sauerstoffsättigung (O2 Tief)
2. Welche Effekte hat die unilaterale elektrische Stimulation des N.
hypoglossus auf die Schlafparameter: Schlafstadienanteile (NREM 1 bis 4
und REM), Totale Schlafzeit, Schlafeffizienz
3. Welche technischen Aspekte ergaben sich während des
Schrittmacherprojektes: Veränderung der Stimulationsparameter
(Impulsweite, Frequenz, Amplitude), Hardware bzw. Materialfehler
Außerdem wurde eine Subsetanalyse bei 4 Patienten durchgeführt, die im
Rahmen eines neuen Schrittmacher-Modells und einem erweiterten
Studienprotokoll untersucht wurden:
4. Welche Effekte hat die unilaterale elektrische Stimulation des N.
hypoglossus auf den Pcrit und den dynamischen Widerstand der oberen
Atemwege (Rus)

- 30 -
3. Methoden
3.1. Auswahl des Patientenkollektivs
Die Teilnehmer der Studie leiden an einer obstruktiven Schlafapnoe
(AHI>20/Std) und wurden über einen Zeitraum von mindestens sechs Monaten
mit einer nCPAP-Therapie behandelt. Die Patienten lehnten allerdings aus
medizinischen oder persönlichen Gründen dauerhaft diese Therapieform sowie
Alternativtherapien ab. Daraufhin wurde eine Studienteilnahme erörtert, wobei
nach unterschriebener Einverständniserklärung die Aufnahme in die Studie
erfolgte.
Es wurden folgende Ausschlusskriterien festgelegt:
1. schwere Herzrhythmusstörungen, bradykarde Arrhythmien; Asystolien
bei SA- oder AV-Blockierungen im Rahmen der Schlafapnoe,
ausgeprägte ventrikuläre Herzrhythmusstörungen
2. Chronische obstruktive Atemwegserkrankungen bzw. Asthma bronchiale
3. Akute Atemwegserkrankungen (z.B. Asthma, Pneumonien, interstitielle
Lungenerkrankung)
4. Aktive kardiale Erkrankungen: stabile Angina pectoris bei KHK,
Myokardinfarkt in den letzten 3 Monaten, dekompensierte
Herzinsuffizienz, entzündliche Herzmuskel-Herzbeutelerkrankungen
5. Maligne arterielle Hypertonie (diastolische Werte > 110 mmHg)
6. Hinweis auf psychiatrische Erkrankungen (akute Psychose, Suizidalität)
7. Narkolepsie, schlafbezogener Myoklonus
8. Patienten , die unter einer Medikation von offensichtlich
schlafstrukturbeeinflussenden Medikamenten stehen (z.B.
Benzodiazepine, Neuroleptika, Stimulanzien, Phenothiazine etc.)
9. Patienten mit Langzeit-Sauerstofftherapie
10. Patienten mit Herzschrittmacher bzw. anderen elektrisch betriebenen
Behandlungsgeräten (interner Defibrillator)
11. Patienten mit Zungen- und neuromuskulären Erkrankungen
12. Jede therapeutische Behandlung, die vom behandelnden Arzt als
kontraindiziert angesehen wird

- 31 -
3.2 Datenerhebung
3.2.1. Polysomnographie
Alle Patienten wurden einer standardisierten Polysomnographie unterzogen um
ihren Schlaf und ihre Atmung zu analysieren (siehe Abbildung 4). Dabei wurden
Daten des Elektroenzephalogramms (EEG) mit den Ableitungen C4A1 und
C3A2, des rechten und linken Elektrookulogramms (EOG), des EMG des M.
Genioglossus mit Hilfe von Nadelelektroden (bezeichnet als EMGment), des
EKG, der Atembewegungen an Brust und Bauch, der peripheren arteriellen
Sauerstoffsättigung (SpO2) und des EMG des M. tibialis anterior aufgezeichnet.
Zur Messung der Brust- und Bauchbewegungen wurde das System Respitrace
(Ambulatory Monitoring Inc., Ardsley, NY, USA) und zur Messung der arteriellen
Sauerstoffsättigung das Pulsoximeter Biox 3740 (Ohmeda, Louisville, CO, USA)
verwendet. Das Luftfluss-Signal wurde sowohl von einer Nasenkanüle als auch
von einem oronasalen Thermistor aufgezeichnet. Sämtliche Signale wurden im
Marburger Schlaflabor kontinuierlich auf einem 16-Kanal-Papierschreiber (UD
32, Firma Schwarzer, München) sowie auf einem lokalen Rechner digital
aufgezeichnet (Sandman Software, Melville NPB, Inc.). Die Probanden wurden
zudem während der gesamten Nacht mit Hilfe von Infrarotkameras durch einen
medizin-technischen Assistenten überwacht.
Abbildung 4: Beispielabbildung einer polysomnographischen Registrierung mit den
Elektrodenpositionen für deren Ableitung
Video
EEGC3-A2
EEGC4-A1
EMGment.
EOGROC
EOGLOC
EKG
EMGtib.
Schnarchen
SpO2
Atemfluss
Thorax
Abdomen
Video
EEGC3-A2
EEGC4-A1
EMGment.
EOGROC
EOGLOC
EKG
EMGtib.
Schnarchen
SpO2
Atemfluss
Thorax
Abdomen

- 32 -
3.2.2. Ermittlung des dynamischen Widerstandes der oberen Atmwege
(Rus) unter der P crit -Gleichung
In den oberen Atemwegen gibt es, resultierend aus dem Starling Resistor,
unterschiedliche Flussvolumina. Jedoch ist die Größe des Luftflusses nicht
allein von applizierten Drücken abhängig, sondern auch von anderen Faktoren
wie z.B. der Widerstand der oberen Atemwege oder die Art der Strömung 30,123.
Hierzu muss man zwischen folgenden Drücken und Widerständen in den
oberen Atemwegen unterscheiden:
Pcrit kritischer pharyngealer Verschlussdruck, Druck im kollabilen Segment
POS Druck des sog. „upstream“ Segments; das Segment, das oberhalb des
kollabilen Segments liegt
PUS Druck des sog. „downstream“ Segments; das Segment, das unterhalb
des kollabilen Segments liegt
ROS oberer Atemwegswiderstand, Widerstand des „upstream“- Segmentes
RUS untere Atemwegswiderstand, Widerstand des „downstream“-Segmentes
RRS pharyngealer Widerstand als Summe der Einzelwiderstände
V Volumenfluss
Analog des ersten Zustandes des Starling Resistors ist der maximale Luftfluss
von der Druckdifferenz vor und hinter dem kollabilen Segment abhängig (siehe
Kapitel 1.3.1.Der Starling-Resistor, Seite 17ff).
Mathematisch wird dieser Sachverhalt durch folgende Formel beschrieben:
RS
critOS
R
PPV
−=
Ebenso lässt sich der Luftfluss durch das kollabile Segment berechnen, der von
dem Druckgradienten zwischen POS und Pcrit Segment abhängig ist.
Ist der Druck oberhalb des kollabierenden Segmentes kleiner gleich dem
kritischen Gewebedruckes im Bereich des kollabierenden Pharynxabschnittes,
ist kein Atemfluss mehr registrierbar(POS - Pcrit = 0)
Unter der Annahme, dass bei konstanten Bedingungen (Körperlage, stabiler
Schlaf ect.) der Pcrit eine Konstante ist, welche durch Übergewicht,
anatomische Charakteristika und neuromuskuläre Faktoren definiert ist, lässt
sich durch eine schrittweise Variation des POS (Maskendruck) eine lineare
Beziehung zwischen den unterschiedlichen POS- Werten und dem Atemfluss

- 33 -
feststellen. Die Druck- Fluss- Beziehung lassen sich somit mathematisch in
Form einer linearen Regression darstellen. Die berechenbare
Geradengleichung definiert mit dem Schnittpunkt der Abszisse den kritischen
Verschlussdruck Pcrit.
3.2.3. Messtechnik zur Bestimmung des Pcrit
Zusätzlich zu den in der Methodik aufgeführten polysomnographischen
Messwerten werden bei der Pcrit- Messung folgende messtechnische
Ergänzungen vorgenommen. Um den kritischen pharyngealen Verschlussdruck
Pcrit sowie den pharyngealen Widerstand Rph zu bestimmen, musste der
Versuchsaufbau wie folgt verändert werden.
Analog einer routinemäßigen nasalen Ventilationstherapie wurden die Patienten
über eine Nasenmaske und einen Beatmungsschlauch mit einem
angeschlossenen nCPAP-Gerät verbunden, welches eine Druckluftschienung
der oberen Atemwege bewirken soll. Zwei kleine Plastikschläuche werden von
der Nasenmaske abgeleitet. Zum einen wird hier eine digitale zum anderen eine
mechanische Druckmessung durchgeführt. Das verwendete und modifizierte
Gerät ist in der Lage unterschiedliche positive und auch negative Druckwerte zu
erzeugen.
Die Patienten erhielten zunächst den therapeutisch notwendigen nCPAP-Druck,
der bereits in den vorangegangenen Nächten ermittelt wurde. Der zweite
Drucklevel, den das modifizierte Gerät liefern konnte diente zur Vorwahl
niedrigerer Maskendrücke, die manuell auf einer Fernbedienung (Respironics
ST/D 30, Respironics, Wendelstein) eingestellt werden konnten. Um auch
negative Drücke zu erzeugen, wurde ein weiteres Gerät (Beatmungsgerät
Somnotron, Weinmann, Hamburg) in den Versuch einbezogen. Mittels
manueller Einstellung, konnten mit Hilfe einer Wasserwaage verschiedene
negative Drücke vorgegeben werden.
Die Bereitstellung eines verringerten positiven Maskendrucks erfolgte durch
Umschalten auf den zweiten Drucklevel des Gerätes. Ein Wechsel vom
therapeutisch notwendigen Maskendruck in den negativen Druckbereich
erfolgte durch ein zwischen das Schlauchsystem zwischengeschaltetes
Umschaltventil (Zentrales Entwicklungslabor für Elektronik, Universität
Marburg).

- 34 -
Dieses Umschaltventil diente zur Regulation des Beatmungsdruckes, wobei
dem Patienten entweder Raumluft in verschiedenen positiven Druckniveaus
durch das nCPAP-Gerät zugeführt oder durch das negative Druck-Gerät Luft
entzogen wurde.
Um den Luftfluss zu messen, wurde ein aus drei Komponenten bestehendes
System eingesetzt: Im Beatmungssystem des Patienten wurde zwischen
Nasenmaske und Beatmungsschlauch ein Röhrenpneumotachograph
(Rudolph, inc., Kansas City, USA) integriert, der indirekt über die Druckdifferenz
vor und hinter dem Sensor über einen Messschlauch die zugehörigen
Differenzen eines jeden Atemzuges an einen Atemflussmesser (Rudolph inc.,
Kansas City, USA) übermittelte.
Mittels eines Drucktransducers (Föhr Medical Instruments GmbH, Seeheim),
der die eingegangenen Signale in Spannung umwandelte, und einer
abschließenden Verstärkung und Filterung (Föhr Medical Instruments GmbH,
Seeheim) der Signale war es möglich, sowohl zwischen Expiration und
Inspiration zu unterscheiden als auch die dazu gehörigen quantitativen
Flusswerte in ml/s zu erfassen.
Abb.5: Schematische Zeichnung des Versuchsaufbaus zur Messung des
kritischen pharyngealen Verschlussdruckes
:

- 35 -
Messprocedere und Protokoll:
Im Laufe der Nacht wurde unter videometrischer Überwachung sowie unter
kontinuierlicher Sicht auf einen 16-Kanal-Schreiber der Maskendruck vom
therapeutisch notwendigen Niveau für maximal 6 Atemzüge auf verschiedene
positive und negative Druckniveaus in absteigender Größe abgesenkt. Die
Druckveränderung erfolgte nur endexpiratorisch und am schlafenden Patienten.
Während der Druckabsenkungen wurde das Schlafstadium nach Rechtschaffen
und Kales dokumentiert. Ein Erwachen des Patienten während des Versuches
wurde ebenso festgehalten104) wie die Lageposition des Patienten, die einen
großen Einfluss auf die Kollapsneigung der oberen Atemwege hat 12,74. Im
Rahmen der späteren Auswertung erfolgte eine Einteilung der Schlafstadien
über die ganze Nacht gemäß Rechtschaffen und Kales 104.
3.3. Auswertung
3.3.1. Auswertung der Polysomnographie
Die Einteilung der Schlafstadien, nach den internationalen Kriterien von
Rechtschaffen und Kales 104 erfolgte auf dem Papierausschrieb an Hand der
Aufzeichnungen des Elektrookulogramms, des Elektromyogramms und des
Elektroenzephalogramms. Auch wurde notiert, ob es während der
Druckabsenkungen zu einem Arousal (Erwecken) des Patienten 1 gekommen
war. Versuche, bei denen es zu einem solchen Arousal unmittelbar oder bis zu
3 Sekunden nach Versuchende gekommen war, wurden nicht mit in die
Berechnung des kritischen pharyngealen Verschlussdrucks Pcrit einbezogen.
Aufgrund der Weckreaktion, die den Tonus der Pharynxmuskulatur steigert und
somit die Kollapsneigung vermindert, können Episoden trotz verringertem
Maskendruck einen dem Wachzustand ähnlichen Luftfluss aufweisen124.
Die respiratorischen Parameter wurden anhand der Atemgurte und des
Larynxmikrophons ausgewertet und zwischen obstruktiven und zentralen
Atmungsstörungen unterschieden. Bei den unterschiedlichen
Druckabsenkungsmanövern, die zu kompletten und inkompletten pharyngealen
Obstruktionen führten, konnten polysomnographisch zentrale SBAS
ausgeschlossen werden.

- 36 -
Eine Quantifizierung der Atmungsstörungen mittels des Apnoe-Hypopnoe-Index
(AHI) wurde nicht vorgenommen. Es wurde allerdings darauf geachtet, dass die
mit den Versuchen verbundenen Druckabfälle nicht mit zentralen
Atmungsereignissen zusammenfielen, beispielsweise während des REM-
Schlafs.
3.3.2 Berechnung des kritischen pharyngealen Versch lussdruckes P crit
und des pharyngealen Widerstandes R ph
Nach der polysomnographischen Auswertung wurde in computerunterstützer
Analyse die Bestimmung des kritischen pharyngealen Verschlussdruckes
vorgenommen. Mit Hilfe der Software Windaq (Dataq Instruments, Akron, Ohio,
USA) wurde erst der therapeutische Druck und dann der während des
Versuches vorgegebene Testdruck des 2. bis 4. Atemzugs endexspiratorisch
bestimmt. Die Erfassung der Druckwerte erfolgte immer endexpiratorisch.
Anhand des letzten Atemzugs vor der Drucksenkung wurde der therapeutisch
notwendig bezeichnete Ausgangsdruck erfasst. Nach Kalibrierung des
Pneumotachographensignals erfolgte die Ermittlung des Luftflusses in ml/s.
Abb.6 : Registrierbeispiel einer Kardiorespiratorischen Polysomnographie mit zusätzlicher Messung des kritischen pharyngealen Verschlussdruckes Pcrit. Dargestellt sind von oben nach unten eine 1 -Kanal Elektrokardiographie (EKG), je eine Ableitungen eines Elektroenzephalogramm (EEG), Elektroocculogramm (EOG) und Elektromyogramm (EMG), Luftfluss, applizierter Druck, thorakale und abdominale Atembewegungen, und Sauerstoffsättigung (SaO2) über eine Aufzeichnungsdauer von 1 Minute. Weiterhin ist eine Drucksenkung für 4 Atemzüge sowie die konsekutiven Luftflussveränderungen zu erkennen.

- 37 -
In der folgenden Abbildung wird ein einzelner Atemzug näher betrachtet. Man
kann genau zwischen den inspiratorischen und expiratorischen Phasen
unterscheiden. Als Umschlagpunkt zwischen Inspiration und Expiration kann
der Wendepunkt des Luftsignals angesehen werden, bei dem es zu keinem
nennenswerten Volumenfluss kommt. Im Drucksignal findet man diesen
Umschlagpunkt am Druckabfall am Ende der Expiration bzw. zu Beginn der
Inspiration.
Mit Hilfe eines Druck-Fluss-Diagramms mit Auftragung des maximalen
Flussvolumen auf der Ordinate und der Zeit auf der Abszisse kann durch die
Strecke zwischen der Nulllinie am Umschlagpunkt (zwischen Expiration zur
Inspiration) und dem tiefsten Punkt des Mess-Signals der maximale
Inspirationsfluss für jeden der drei Atemzüge bestimmt werden.
Abb.7: Darstellung von Maskendruck und Flusskurve im Verlauf eines Atemzyklus,
Vimax = maximaler inspiratorischer Fluss
Druck in
cm H20
Luftfluss
in ml/s
Endexpiratorischer
Druckpunkt zur
Bestimmung des
Umschlagpunkt
zwischen Expiration
und Inspiration Luftfluß = 0 ml/s
Maximaler
inspiratorischer
Luftfluss (Vimax)
Inspiration Exspiration
Zeit in s
Expiration

- 38 -
Zur späteren Berechnung der Fluss-Volumen-Kurve wurden nur
Drucksenkungen verwendet, bei denen sich der Patient in den Schlafstadien
NREM 2-4 und REM befand. Außerdem durfte es zu keiner Änderung des
Schlafstadiums des Patienten vor, während und nach dem Versuch (weniger
als 3 Sekunden) kommen.
Um den kritischen pharyngealen Verschlussdruck Pcrit graphisch darzustellen
wurden nur Episoden mit Absenkungen des Maskendrucks berücksichtigt, bei
denen es zu einer Limitation des Luftflusses kam. Abschließend wurden diese
ermittelten Werte des kritischen pharyngealen Verschlussdrucks und die Werte
des pharyngealen Widerstandes Rph in NREM 2-4 Schlaf tabellarisch
zusammengestellt.
3.4. Das Schrittmacher-System zur atmungsgetriggert en
neuromuskulären Stimulation des N. Hypoglossus
3.4.1. Die Komponenten
Das verwendete Schrittmachersystem besteht aus 3 Komponenten: der
Elektrode, dem Drucksensor und dem eigentlichen Schrittmacheraggregat.
Die tripolare Elektrode hat einen halbseitig geöffneten Cuff (Half-Cuff-Elektrode;
Medtronic Model 3990A Lead) bestehend aus Platinum/Iridium, wobei die Cuff-
Öffnung 3-4 mm misst. Der Cuff wird um den Nerv gelegt ohne diesen zu
beschädigen. Die gesamte Elektrode ist mit Silikon bzw. Polypropylene isoliert.
Die Gesamtlänge des Elektrodenkabels beträgt 45 cm und hat einen
Durchmesser von 1 mm.
Der Drucksensor (Medtronic Model 4322T) ist in der Lage kleinste
Druckschwankungen zu messen, die im Brustraum durch die atmungsbedingten
Druckschwankungen hervorgerufen werden. Der Piezo-Kristall-Drucksensor
wird transsternal fixiert und durch ein subkutan verlaufendes Kabel mit dem
Schrittmacheraggregat verbunden.
Das Schrittmacheraggregat (Medtronic© Model 3024 Stimulator) ist mit 2
Verbindungssteckern/Zugängen ausgerüstet. Einer ist für die
Stimulationselektrode und der zweite für den Drucksensor reserviert. Das
Schrittmacheraggregat wird subkutan über den M. pectoralis implantiert.

- 39 -
Der Drucksensor übermittelt die Werte der thorakalen Druckschwankungen an
den Impulsgenerator. Dieser kann aufgrund der programmierten
Druckschwellenwerte Inspiration und Expiration unterscheiden. Es wird für jede
Inspiration ein Impuls zur Elektrode abgegeben, die diesen an den Nerv
übermittelt. Dies hat eine Muskelkontraktion zur Folge.
Die Reizung des Nerven kann in der Stimulusamplitude, der Frequenz und der
Impulsdauer verändert werden. Diese Parameter beschreiben die benötigte
Stromstärke, Frequenz und Impulsdauer, mit der der Nerv gereizt wird um eine
Reizantwort zu erhalten.
3.5. Operatives Procedere
Die operative Implantation des Schrittmachersystems erfolgte in Marburg in der
Klinik für Gesichts-, Mund- und Kieferchirurgie in Zusammenarbeit mit dem
Departement für Head and Neck-Surgery der Johns Hopkins Universität
Baltimore. Um die Protrusion der Zunge (M. genioglossus-Aktivierung), bei
intraoperativer Stimulation, beurteilen zu können erfolgt die Operation in nasaler
Intubationstechnik. In einem ersten Schritt wird der distale Ast des N.
hypoglossus über eine kleine Inzision an der Halsseite freigelegt. Die Elektrode
wird vorsichtig um den freipräparierten Nerv gelegt, wobei anschließend über
elektrische Stimulation der motorische Schwellenwert geprüft wird, bei der die
Zunge eine suffiziente Vorwärtsbewegung durchführt. Bei wiederholter
Protrusion der Zunge (klinische Beobachtung) wird die Elektrode in Position
belassen. Der Impulsgenerator, der auch gleichzeitig Empfänger ist, wird über
eine weitere Inzision subkutan implantiert, an die Elektrode angeschlossen und
die Operationswunde verschlossen. Nach intraoperativer Verifizierung der
Funktionen des Schrittmachers wird ein Drucksensor transsternal platziert
(dritte Inzision). Bei diesem Drucksensor handelt es sich um einen mit
Piezokristallen ausgestatteten Sensor, der sehr empfindliche thorakale
Druckschwankungen messen kann. Nach Funktionsprüfung der einzelnen
Elemente erfolgen Wundverschluss und eine prophylaktische
Antibiotikatherapie. Nach steriler Wundversorgung erfolgt die radiologische
Positionskontrolle und Dokumentation direkt postoperativ. Dem Protokoll
entsprechend erfolgt nach Wundheilung 4 Wochen postoperativ die erste
Schlaflabormessung mit Schrittmachereinstellung in zwei aufeinander
folgenden Nächten.

- 40 -
Abb.8 Implantierbares N. Hypoglossus Stimulationssystem zur Behandlung der obstruktiven
Schlafapnoe (Medtronic, Inc., Maastricht, The Netherlands)
Sensor Lead = Sensor Kabel
Stimulation Lead = Stimulationskabel
IPG = Schrittmacher (Impulsgenerator)
Hypoglossal Nerve = N. Hypoglossus
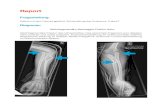
Abb. 9: Schnittführung und Kabelverlauf des N. Hypoglossus-Stimulationssystems am Patienten.
Die Inzisionsstellen (schwarz mit Endpunkten) befinden sich an der Halsseite
(Elektrodenlokalisation), pektoral (Impulsgenerator) und sternal (Piezodrucksensor). Die anderen
Linien stellen zum einen den Sitz und die Größe des Impulsgenerators und die subkutan
getunnelten Schrittmacher-Kabel dar. Die Intubation erfolgte nasal.
Stimulationselektrode
Piezodrucksensor
Impulsgenerator

- 41 -
3.6. Patientenkollektiv
In Zusammenarbeit mit dem Johns Hopkins Sleep Disorder Center, Baltimore
(USA), dem Sleep Center der Ziekenhuis Universität, Antwerpen (Belgien), dem
Sleep Center der Sahlgrenska Universität, Göteborg (Schweden) und dem
Hennepin County Medical Center der Universität von Minnesota (USA) wurde
eine Pilotstudie mit 8 Patienten durchgeführt, die man mit dem oben
beschriebenen voll implantierbaren Schrittmachersystems versorgte.
Tabelle 2 zeigt die anthropometrischen Daten aller Patienten. Zwei dieser
Patienten unterzogen sich bereits einer Uvulopalato-Pharyngoplastik, die
jedoch keinen therapeutischen Erfolg erzielte (RS und JT). Alle Patienten
benutzen ein CPAP –Gerät über einen Zeitraum von mindestens 6 Monaten,
beendeten diese Therapieform jedoch vor Behandlungsbeginn.
Tabelle 2: Anthropometrische Daten sowie Ausgangsbefunde aller Patienten
NREM REM
Patient Geschlec
ht
Alter Nacken BMI AHI O2 Basis O2 Tief AHI O2 Basis O2 Tief
(Jahre)
)
(cm) Kg/m2 (#/Std) (%) (%) (#/Std) (%) (%)
DF M 57 43,5 31,4 65,6 91,9 90,1 45,7 94,6 88,4
JT M 54 46,5 34,4 17,1 92,4 91,7 8,0 95,0 92,4
HL M 55 41,0 25,8 57,8 91,4 88,7 66,7 88,9 85,9
SH M 52 45,7 34,9 58 97,3 86,6 60,0 96,8 75,7
RS M 36 41,3 24,5 60,7 93,0 87,6 69,7 93,3 89,9
CB M 38 39,4 27,2 80,8 97,4 93,6 88,4 97,0 93,7
LK M 54 39,5 23,1 46,5 98,1 93,1 47,1 98,0 94,7
HW M 53 40,0 26,0 29,7 91,2 85,9 0,0* - -
Mittel 49 41,9 28 50,1 94,4 89,6 48,6 94,8 88,7
SD 8 3 4,7 21,2 3,1 3,2 32,9 3,4 7,1
Min-Max 36 - 57 39,4 - 46,5 23,1 - 34,9 17,1 - 80,8 91,2 - 98,1 85,9 - 91,7 8,0 - 88,4 98,0 - 88,9 94,7 –
75,7
BMI, body mass index; NREM ( non-rapid eye movement) – NREM-Schlaf ;
REM ( rapid eye movement) – REM-Schlaf; AHI, Apnea-Hypopnoe Index;
O2 Basis, Ausgangs-Sauerstoffsättigung; O2 Tief, Durchschnitllich niedrigste
Sauerstoffsättigung bei Ereignissen; SD Standard deviation,
Standardabweichung;
Mittel, Mittelwert
* REM-Schlaf aus technischen Gründen nicht auswertbar

- 42 -
3.7. Statistische Auswertung
Bei dieser Untersuchung handelt es sich um eine Pilotstudie. Vergleichsdaten
aus anderen Untersuchungen liegen nur in sehr begrenzten Umfang vor.
Aufgrund der daraus resultierenden Fallzahl wird auf eine inferenzstatistische
Absicherung der Daten verzichtet. Die Darstellung der Ergebnisse erfolgt rein
deskriptiv.

- 43 -
4. Ergebnisse
4.1. Operativer und postoperativer Verlauf:
Intraoperativ traten keine Komplikationen, keine nennenswerten Blutungen oder
Narkoseschwierigkeiten auf. Auch postoperativ kam es zu keinen Infektionen
des Operationsgebiets, ebenso nicht zu verzögerten Blutungen oder
Schmerzen.
Es traten auch keine späteren Nebenwirkungen durch den eingeschalteten
Schrittmacher, wie Missempfindungen, Schluck- oder Sprachstörungen auf.
4.2. Effekte der unilateralen elektrischen Stimulat ion des N.
Hypoglossus auf die respiratorischen Parameter
4.2.1. Unmittelbare Effekte während einzelner Atmun gszyklen
Unter inspirationsgetriggerten Stimulation des N. hypoglossus während des
Schlafes zeigte sich zusammenfassend eine deutliche Reduktion der
Schnarchphasen und eine verbesserte Synchronizität der thorakalen und
abdominalen Atemexkursionen, was zusammenfassend durch eine
Verringerung der Obstruktionen der oberen Atemwege gewertet werden kann.
Während bei 3 Patienten sowohl eine Verbesserung des inspiratorischen
Atemflusses in Rücken- und Seitenlage festgestellt werde konnte, zeigte ein
Patient lediglich in Seitenlage eine Verbesserung der Atmungsbefundes.
Die Abbildung 10 zeigt eine nächtliche Aufzeichnung mit folgenden Ableitungen:
Ein Elektroocculogramm (EOG), ein submentales Elektromyogramm (EMG),
das die Zungenbewegung anzeigt, eine Elektroenzephalogramm (EEG), den
Luftfluss(Airflow), einen ösophagealen Drucksensor (Pes), der die thorakalen
Druckschwankungen während der In- und Expiration misst und die
Sauerstoffsättigung (SaO2).
Die polysomnographischen Aufzeichnung zeigt die Veränderungen der
Atmungs- und Schlafparameter, wenn der Schrittmacher eingeschaltet wird. In
Abbildung 10 sieht man während einer kontinuierlichen NREM-Schlafphase
links der Trennlinie Atemzüge ohne Hypoglossus-Stimulation, rechts der
Trennlinie Atemzüge mit Hypoglossus-Stimulation.

- 44 -
Bevor die elektrische Stimulation des N. hypoglossus einsetzt, erkennt man 3
obstruktive Atmungsstörungen. Während dieser Obstruktionen nehmen der
Luftfluss und der Druck im Ösophagus ab. Etwas verzögert fällt später auch die
Sauerstoffsättigung ab. Eine obstruktive Atmungsstörung wird durch eine
Weckreaktion (Arousal) beendet, welches sich in einer Veränderung des EEGs
und EOGs zeigt. Außerdem sieht man einen vermehrten kompensierenden
Luftfluss und eine Normalisierung der Sauerstoffsättigung.
Mit Beginn der Stimulation des N. hypoglossus stabilisiert sich der Luftfluss und
somit die Atmung. Das Schlafstadium verändert sich nicht und es kommt zu
keinen Entsättigungsphasen und Weckreaktionen (Arousals).
Abb.10: Polysomnographische Aufzeichnung mit und ohne Schrittmacherfunktion

- 45 -
4.2.2. Langzeiteffekte aller gemessenen Patienten
4.2.2.1.Schlafbezogene Atmungsstörungen
Tabelle 3 zeigt den mittleren Apnoe-Hypopnoe-Index (AHI) des gesamten
Studienkollektivs unter bestimmten Auswertekriterien. Dabei werden 3
Aufzeichnungszeitpunkte unterschieden.
In der Baseline-Nacht werden die Ausgangswerte erhoben.
Die „Komplette Nacht“ zeichnet den ganzen Zeitraum einer Nacht auf, inklusive
Einschlafzeit, bei der der Schrittmacher noch deaktiviert ist.
Die kontinuierliche Stimulation bezieht sich nur auf den Zeitraum einer Nacht,
bei der der Schrittmacher permanent aktiviert ist.
Man erkennt in der kompletten Nacht und dem Zeitraum unter Stimulation einen
Rückgang des AHI sowohl während der NREM- als auch während der REM-
Schlafphasen. Des Weiteren verbessern sich der Sauerstoffmittelwert und der
Sauerstofftiefstwert.
Tabelle3: Schlafbezogene
Atmungsstörungen der Studienpatienten
NREM REM
Zeitpunkt AHI % Apnoen O 2 Basis O 2 Tief AHI % Apnoen O2 Basis O 2 Tief
Baseline Mittel 52,0 38,8 94,1 89,7 48,2 26,2 94,4 89,0
Nacht SD 20,4 36,5 3,0 2,9 30,5 32,6 3,1 6,1
Komplette Mittel 22,6 28,2 95,2 91,7 16,6 17,9 94,8 91,6
Nacht SD 12,1 23,4 2,2 2,0 17,1 19,3 2,4 2,2
Kontinuierli
che Mittel 15,5 34,7 95,4 92,4 12,0 3,7 94,3 92,6
Stimulation SD 15,2 33,4 1,9 2,9 17,6 6,3 3,0 3,0
% Apnoen, Apnoen in Prozent (Anzahl der Apneoen /Anzahl der Apnoen
+ Hypopnoen
O2 Basis, Ausgangs-Sauerstoffsättigung;
O2 Tief Durchschnitllich niedrigste Sauerstoffsättigung bei Ereignissen;
SD, Standard deviation, Standardabweichung; Mittel, Mittelwert
Komplette Nacht – Messdauer über die ganze Nacht
Kontinuierliche Stimulation – Messdauer nur bei Stimulation

- 46 -
In Abbildung 11 wurden die Veränderungen des AHI nach
Schrittmacherimplantation graphisch dargestellt.
Bei 6 Patienten zeigt sich unter Schrittmacherstimulation eine deutliche
Reduktion des AHIs.
Abb. 11: Veränderung des Apnoe/Hypopnoe-Index bei den Studienpatienten
0
10
20
30
40
50
60
70
80
90
Baseline Komplette Nacht KontinuierlicheStimulation
NREM AHI (#/Std)
DF
JT
HL
SH
RS
CB
LK
HW
4.2.2.2.Schlaf-Parameter
Die Schlafqualität hat sich durch die Funktion des Schrittmachers erheblich
verbessert. In der Baseline Nacht überwogen vor allem die Schlafstadien 1 und
2 während der Tiefschlaf, Schlafstadium 3 und 4 (SWS), anteilsmäßig geringer
war. Bei der „Continous-Night“, bei der nur die Zeit erfasst wird, in welcher der
Schrittmacher eingeschaltet wurde, lässt sich eine Normalisierung der
Schlafstruktur feststellen. Der Anteil des SWS steigt im Mittel von 8,7% wieder
auf 12,7% (siehe Tabelle 4).
Bei einer Messdauer über eine gesamte Nacht, unabhängig wie oft der
Schrittmacher ausgeschaltet wurde, ist sogar ein Tiefschlafanteil mit 15,9 %
ermittelt worden.

- 47 -
Tabelle 4 : Veränderung der Schlaf-Architektur der Studienpatienten
TST SE % S1 % S2 % SWS % REM
Baseline Mittel 307,8 76,3 33,9 46,6 8,7 11,1
Nacht SD 97 23,2 20,2 14,5 8,4 7,7
Komplette Mittel 259,8 70,8 21,1 51,7 12,7 14,5
Nacht SD 66 14,5 9,4 10,1 11,3 5,7
Kontinuierliche Mittel 227,4 88,4 20,2 49,5 15,9 15,3
Stimulation SD 113,7 13,5 19,5 14,2 16,2 9,3
TST, total sleep time, totale Schlafzeit (in Minuten); SE, sleep efficiency, Schlafeffizienz (%
TST/Zeit im Bett);
%S1,Prozent Sclafstadium 1 (Zeit in Schlafstadium 1 sleep/TST); %S2, Prozent Schlafstadium2 (time in
stage2/TST);
% SWS, percent slow wave sleep, Prozent Tiefschlafzeit (Zeit im Tiefschlafstadium/TST);
% REM, percent REM sleep, Prozent im REM-Schlaf (Zeit im REM-Schlaf/TST)
SD, Standard deviation, Standardabweichung; Mittel, Mittelwert
Komplette Nacht – Messdauer über die ganze Nacht
Kontinuierliche Stimulation – Messdauer nur bei Stimulation
4.3. Funktionen des Schrittmachers
4.3.1. Technische Parameter im Verlauf
In Tabelle 5 werden die Stimulationsparameter der Patienten über den
Behandlungszeitraum aufgeführt. Es zeigte sich ein signifikanter Anstieg der
Stimulationsstärke und der Frequenz über den Zeitraum der Studie, allerdings
zeigen sich keine klinisch relevanten Änderungen der Impulsdauer.
Änderungen der Stimulationsparameter wurden nach 1 Monat (38 ± 15 Tage,
n=8), nach 3 Monaten (103 ± 16 Tage, n=7), nach 6 Monaten (219 ± 31 Tagen,
n=8) sowie beim letzten Follow-up (345 ± 97 Tage, n=6) durchgeführt.
Tabelle 5: Veränderung der Schrittmacher-Stimulationsparameter während des
Studienzeitraums
Stimulus Amplitude (Volt) Frequenz in Hz Impulsdauer (µs) Monat (nach Implantation)
Mittel SD Mittel SD Mittel SD
1 2.2 0.5 33.9 2.5 94.3 9.2
3 2.6 0.4 35.0 3.4 107.7 24.6
6 2.7 0.7 35.6 3.6 105.6 23.5
Abschlussuntersuchung 3.0 1.0 37.7 3.6 110.5 25.7
SD - Standardabweichung Mittel - Mittelwert

- 48 -
4.3.2. Elektrodenbruch/Haltbarkeit der Hardware
Während des Beobachtungszeitraums wurden bei einem Patienten
Verwachsungen im Bereich des transsternalen Drucksensors registriert, so
dass dieser die Druckveränderungen zwischen Inspiration und Exspiration nicht
mehr detektieren konnte und während einer erneuten Operation ausgetauscht
werden musste. Bei einem Patienten kam es durch einen Verkehrsunfall zu
einem Bruch einer Elektrode so dass diese ebenfalls operativ gewechselt
werden musste.
4.4. Sub-Set-Analyse mit Messung der pharyngealen Kollapsibilität und
des Widerstandes der oberen Atemwege bei n=4 Patien ten
Aus dem Patienten-Pool der Multicenter-Studie wurden 4 Patienten mit dem
speziellen Protokoll dieser Arbeit gemessen.
Zusätzlich zu den routinemäßigen Parametern, wie zum Beispiel dem Apnoe-
Hypopnoe-Index (AHI), wurde in den Zentren Baltimore und Marburg zusätzlich
der kritische Verschlussdruck Pcrit und der obere Atemwiderstand Rus ermittelt.
Zur Ermittlung dieser Parameter wurde der Versuchsaufbau, der in Kapiteln
3.2.3. beschrieben wurde, verwendet.
Im Kapitel 3.2. (Datenerhebung) wurde bereits ein Registrierbeispiel einer
Polysomnographie gezeigt. Die folgenden Beispiele zeigen Pressure Drops
während einer Pcrit-Untersuchung vor und nach einer Schrittmacherimplantation.
Zum Zeitpunkt beider Drucksenkungsversuche (Pressure Drop) lag der Patient
auf dem Rücken und befand sich in einem Leicht-Schlaf Stadium (NREM 2).

- 49 -
Abb. 12: Registrierbeispiele von Drucksenkungsversuchen in NREM-Schlaf in Rückenlage, linke
Abbildung vor und rechte Abbildung nach Schrittmacherimplantation
Man erkennt in der linken Abbildung, dass es während der Drucksenkung zu
einem Null-Fluss im Flow-Kanal kommt und dass das Ende des Druckversuchs
mit einem Arousal, Schnarchen und kompensatorischer Hyperventilation
einhergeht.
Die rechte Abbildung zeigt eine Messung unter Stimulation des N. hypoglossus.
Die permanente Stimulation durch den Schrittmacher erkennt man in Kanal 5,
der die Muskelaktivität der mimischen Muskulatur aufzeichnet.
In beiden Abbildungen ist der nCPAP-Druck (Testing Pressure) gleich, doch
kommt es im User/Flow-Kanal ohne Stimulation zu einem Nullfluss, also
kompletten Verschluss des kollabilen Segments während sich unter Stimulation
eine verbesserte, jedoch noch flusslimitierte Atmung darstellt.

- 50 -
REM
0
50
100
150
200
250
300
350
400
450
500
-3 -2 -1 0 1 2 3 4 5 6 7 8
Test Druck in cm H2O
Flu
ss in
ml/s
HW 28.11.1997
HW 08.04.1998 stimuliert
NREM
0
50
100
150
200
250
300
350
400
450
500
-3 -2 -1 0 1 2 3 4 5 6 7 8
Testdruck in cm H2O
HW 28.11.1997
HW 05.03.1998
stimuliert
4.4.1. Pressure-Flow-Plot mit und ohne Stimulation bei Rückenlage
Die Abbildungen 13a und 13b zeigen beispielhaft die Druck-Fluss-Beziehungen
eines Patienten welche 4 Monate nach Schrittmacherimplantation gemessen
wurden. Die Messungen erfolgten jeweils in Rückenlage.
Abb.13: Pressure-Plots für Druck-Fluss-Beziehung bei Patienten in NREM- und REM-Schlaf
mit und ohne Schrittmachereffekt
Es ist zu sehen, dass sich der Pcrit im NREM- und REM-Schlaf unter
Stimulation in den subatmosphärischen Bereich verschiebt, was darauf
hindeutet dass komplette in partielle Obstruktionen umgewandelt werden
konnten. Hierdurch erklärt sich unter anderem auch die Abnahme des AHI in
der Subset-Analyse, die auch schon in der Analyse aller Patientendaten
gezeigt wurde (siehe auch Kap. 4.2.2.1).

- 51 -
4.4.2. Tabellen und Zusammenstellung des kritischen pharyngealen
Verschlussdruckes und des oberen Atemwiderstandes
Tabellarisch werden von den 4 Patienten die Veränderungen der untersuchten
Parameter in Tabelle 6 dargestellt.
Tabelle 6: Veränderung des kritischen Verschlussdruckes und des Widerstands der oberen
Atemwege im gemessenen Patientenkollektiv
Patient
Pcrit (cm H2O)
S- S+
Rus (cm H2O/l/s)
S- S+
1.SH +0,5 -2,0 14,0 12,2
2.RS +3,1 -1,5 22,0 23,9
3.CB -0,4 -2,4 22,0 23,9
4.HW -0,8 -1,6 37,9 19,9
S - = ohne Stimulation
S+ = mit Stimulation
Auch die Veränderung der pharyngealen Kollapsibilität (Pcrit) lässt sich
graphisch darstellen.
Deutlich ist bei jedem Patienten die Abnahme der Kollapsibilität unter
Schrittmacher-Stimulation zu erkennen(siehe Abbildung 14).
Abb. 14: Veränderung des Pcrit unter Stimulation
Pcrit -Veränderungen unter Stimulation
-4
-3
-2
-1
0
1
2
3
4
- S + S
Pcr
it in
cm
H2O SH
CB
RS
HW
S - = ohne Stimulation
S+ = mit Stimulation

- 52 -
Abbildung 15 zeigt die Veränderung im Widerstand der oberen Atemwege. Eine
Verringerung des oberen Atemwegswiderstands zeigte sich bei 2 Patienten,
während er bei 2 Patienten anstieg.
Abb. 15: Veränderung des Rus unter Stimulation
Veränderung des Rus unter Stimulation
0
5
10
15
20
25
30
35
40
- S + S
Rus
(cm
H2O
/l/s)
SH
CB
RS
HW
S - = ohne Stimulation
S+ = mit Stimulation

- 53 -
5. Diskussion
Ziel der zugrunde liegenden Untersuchung war es, die Ergebnisse der
Nervenschrittmacher-Implantation, die technische Durchführbarkeit und die
Effekte der elektrischen Stimulation des N. hypoglossus auf die Funktion der
oberen Atemwege zu untersuchen. Hierzu wurden in einer multizentrischen
Pilotstudie Patienten nach einem standardisiertem Protokoll eingeschlossen,
welches jeweils pro Patient eine präoperative Ausgangsmessung und
zahlreiche postoperative Kontrollmessungen beinhaltete. Nach entsprechender
postoperativer Erholung und Wundheilung wurde eine Polysomnographie zur
Einstellung der elektrischen Stimulationsparameter durchgeführt, in der die
Patienten an die nächtliche elektrische Stimulation während des Schlafes
adaptiert wurden.
Als Hauptergebnis dieser Untersuchung ist festzuhalten, dass die nächtliche
unilaterale Stimulation des N. hypoglossus bei Patienten mit obstruktiver
Schlafapnoe zu einer Reduktion schlafbezogener Atmungsstörungen führt,
ohne dass durch diese Methode störende Weckreaktionen im Schlaf (Arousal)
hervorgerufen wurden. Insbesondere kam es zu einer relevanten Abnahme der
Frequenz von Apnoen und Hypopnoen im Schlaf, wodurch auch der
Schweregrad der nächtlichen Sauerstoffdesaturationen im Schlaf verbessert
werden konnte. Mit der Reduktion schlafbezogener Atmungsstörungen durch
die nächtliche elektrische Stimulation des N. hypoglossus zeigte sich ein Trend
zu einem Anstieg des Tiefschlafanteils. Darüber hinaus tolerierten alle
Patienten die nächtliche elektrische Stimulation während des Schafes, ohne
dass unerwünschte Nebenwirkungen dokumentiert werden konnten.
Folglich konnte die Durchführbarkeit der elektrischen Stimulation des N.
hypoglossus zur Behandlung der obstruktiven Schlafapnoe demonstriert und
das therapeutische Potential dieser Methode verdeutlicht werden, wobei die
Aspekte Technik, klinische Ergebnisse, sowie die dieser Arbeit zugrunde
liegenden Untersuchungen zur Mechanik der oberen Atemweg im Schlaf im
Detail diskutiert werden.

- 54 -
5.1. Technische Diskussion
Zusammenfassend zeigten die ersten Untersuchungen 4 Wochen postoperativ
ein gutes respiratorisches „Sensing“ (Aufzeichnung der atemsynchronen
intrathorakalen Druckschwankungen), sowie eine unproblematische
Impulsgebung und Fortleitung der elektrischen Impulse auf den Nerven, was die
praktische Umsetzbarkeit der Methode bestätigte. Die telemetrisch
übermittelten respiratorischen Atemkurven zeigten überwiegend eine gute
Signalqualität. In einigen Fällen zeigte das durch den Drucksensor
aufgezeichnete Signal gelegentlich Störungen der atemsynchronen Wellenform,
die zu einer Dissoziation der elektrischen Impulse mit dem Inspirationsbeginn
führten (Patienten SH und CB). In diesen Fällen führte die inspiratorische
Desynchronisation zu einer fehlenden Stimulation aufgrund des fehlenden
Atemsignals.
Wiederum wurden in einigen Fällen Atemkurvenartefakte aufgezeichnet, die zu
einem Ausbleiben einzelner atemsynchroner elektrischer Impulse führte.
Abb. 16: Registrierbeispiel für Artefakte, die zu keinem therapeutischen Effekt führten
Zum Teil wurden diese oben genannten Signalstörungen durch die
Schlafposition, ein schlafstadien-spezifisches Atmungsmuster (z.B. periodische
Atmung im REM-Schlaf) oder pulssynchrone kardiale Artefakte hervorgerufen.
Die weiteren Follow-up Untersuchungen zeigten, dass die elektrischen
Parameter modifiziert und adjustiert werden mussten. Dabei erhöhte sich

- 55 -
insbesondere der motorische Schwellenwert, bei dem eine M. genioglossus -
Aktivierung erreicht werden konnten (Bandbreite von 2,8 bis 3,2 Volt) bei allen
Patienten.
Als mögliche Erklärung wurde ein Bindegewebswachstum zwischen Nerv und
Elektrode bzw. im Bereich des Piezodrucksensors oder eine strukturelle
Schädigung der Elektrode angenommen. In tierexperimentellen Studien der
Johns Hopkins Universität/Baltimore/USA wurde in einem Fall ein
Bindegewebswachstum zwischen dem Nerv und der U-förmig konzipierten
Elektrode festgestellt, welches den Nerv aus der Ummantelung der Elektrode
drängte. Aufgrund der höheren Widerstände wurden höhere motorische
Schwellenwerte für die elektrische Stimulation benötigt. Obgleich nahezu bei
allen Patienten ein moderater Anstieg der elektrischen Schwellenwerte
beobachtet wurde, konnte ein Bindegewebswachstum zwischen Nerv und
Elektrode beim Menschen bisher nicht dokumentiert werden. Eine strukturelle
Schädigung der Elektrode des Marburger Patienten konnte nach Explantation,
bei vorheriger Fehlfunktion, nachgewiesen werden, wobei sich kein
Bindegewebe zwischen Nerv und Elektrode darstellte. Die Multizentrische
Studie (n=8) zeigte bei zwei Generatoren Fehlfunktionen. Insgesamt wurden
eine Sensorfehlfunktion und ein Elektrodenbruch festgestellt.
Durch eine Verbesserung der Elektrode und Konzipierens eines größeren
Sensors könnten die oben beschriebenen Probleme beseitigt werden.
5.2. Klinische Diskussion
Intraoperative Komplikationen (Verletzungen größere Blutgefäße,
Nervenschädigungen) traten nicht auf. Obgleich eine Implantation
körperfremden Gewebes erfolgte, wurde das Infektionsrisiko durch strengste
hygienische Vorsichtsmaßnahmen reduziert (Trennung der Operationsfelder
durch separate Abdeckung von Gesicht und Mund). Aufgrund einer
anatomischen Verbindung zum Mediastinum, welche durch die Bohrung durch
das Brustbein künstlich geschaffen wurde, um den Piezzo-Drucksensor zu
verankern, wurde unter höchsten aseptischen Bedingungen operiert. Eine
Mediastinitis als gefürchtete Komplikation (Letalität bei ca. 50%) trat in keinem
der Fälle auf. Es sollte aber überlegt werden ob dieses Risiko nicht reduziert

- 56 -
werden könnte, indem man zum Beispiel eine intrapleurale Lokalisation des
Drucksensors vorzieht.
Als Hauptergebnis dieser Pilotstudie ist festzustellen, dass die unilaterale
Stimulation des distalen Astes des Nervus Hypoglossus zu einer Reduktion
schlafbezogener Atmungsstörungen während des NREM-Schlafes bei
Patienten mit Obstruktivem Schlafapnoe Syndrom führt. Weder die
mechanische Bewegung (Protrusion) der Zunge, noch die elektrischen Impulse
beeinflussten die Schlafqualität in relevantem Ausmaß. Es ließ sich unter der
atemsynchronen elektrischen Stimulation eine Verbesserung der Schlafqualität
bei Patienten feststellen (Zunahme des Tiefschlafanteils unter Stimulation im
Vergleich zu Ausgangsmessung ohne Schrittmacheraktivität). Die elektrischen
Parameter (Amplitude, Impulsfrequenz, Impulsdauer) während er nächtlichen
Stimulation beeinflussten in allen Fällen weder die motorische noch
sensorische Funktion der Zunge am Tage (Essen, Sprechen etc.). Eine
unerwünschte Hypertrophie des M. genioglossus durch die intermittierende
nächtliche Stimulation (ausgeschlossen durch klinische Untersuchung und
MRT) wurde in keinem der Fälle beobachtet.
5.3. Mechanik der oberen Atemwege unter elektrische r Stimulation
Obgleich die klinischen Ergebnisse der unilateralen Stimulation des N.
hypoglossus Effekte auf die Mechanik der oberen Atemwege zeigten, wurden
unerwartete Störgrößen bei den einzelnen Studienpatienten festgestellt.
Der in Marburg betreute Patient entwickelte im Schlaf ausschließlich in
Rückenlage weiterhin obstruktive Apnoen, während in Seitenlage keine klinisch
relevanten schlafbezogenen Atmungsstörungen mehr auftraten. Im Vergleich
zur Ausgangsmessung (Baseline) präsentierte dieser Patient unterschiedliche,
körperlageabhängige Effekte unter elektrischer Stimulation in allen weiteren
Nachfolgeuntersuchungen. Im Detail zeigte sich in der
pneumotachographischen Messung einer Verbesserung des maximalen
inspiratorischen Spitzenflusses (Vimax) in Seitenlage von 100-250 ml/sec,
während in Rückenlage eine Verbesserung von weniger als 50 ml/sec
aufgezeichnet wurde. Dies deutet auf eine weiterhin vorhandene partielle
Obstruktion der oberen Atemwege trotz Stimulation des M. genioglossus hin.

- 57 -
Die Ergebnisse der Studie lassen den Schluss zu, dass die Reduktion
schlafbezogener Atmungsstörungen durch eine Aktivierung des M.
genioglossus hervorgerufen wird, der über eine elektrische Reizung des N.
hypoglossus erfolgt. Bei unilateraler Aktivierung dieses Muskels kommt es zu
einer Protrusion und Deviation der Zunge zur kontralateralen Seite. Dieser
Effekt wurde intraoperativ und während sämtlicher Nachfolgeuntersuchungen
geprüft. Darüber hinaus konnte bei einer entsprechenden Protrusion der Zunge
im Schlaf eine Verbesserung des Luftflusses aufgezeichnet werden, die bei
einer Deaktivierung des Impulsgebers (jeweils für einen Atemzug) nicht mehr
beobachtet werden konnte.
Eine Verbesserung des inspiratorischen Luftflusses ist am ehesten Folge einer
Abnahme der pharyngealen Kollapsibilität zu interpretieren 79,125. Es konnte
gezeigt werden, dass eine derartige Abnahme der pharyngealen Kollapsibilität
sowohl zu einer Zunahme des inspiratorischen Luftflusses als auch eine
Reduktion des Apnoeindex bewirkt 28,119,121,124. Zusammenfassend ist davon
auszugehen, dass die Verbesserungen der Apnoe-Hypopnoe-Indices während
der elektrischen Stimulation des N. hypoglossus auf eine Kontraktion des M.
genioglossus und einer damit verbunden Abnahme der pharyngealen
Kollapsneigung zurückzuführen ist.
Die Kollapsibilität der oberen Atemwege kann durch den kritischen
Gewebsdruck definiert werden, bei dem die oberen Atemwege komplett
kollabieren (Pcrit). Es existieren mehrere Ansätze den kritischen
Verschlussdruck bei Patienten mit schlafbezogenen Atmungsstörungen zu
bestimmen. Dabei werden zum einen Protokolle zur Erfassung der Druck-
Querschnittsbeziehungen im Pharynx beschrieben52 und zum anderen werden
die Druck-Flussbeziehungen im oberen Atemwegssystem analysiert. Während
die erstgenannte Methode einen erheblichen apparativen Aufwand darstellt,
sind Druck-Flussbeziehungen unter Verwendung eines Pneumotachographen
und Maske relativ einfach durchführbar. Das in dieser Untersuchung
angewendete Untersuchungsprotokoll zur Messung des „Pcrit“ wurde
ausgewählt, da es eine sehr praktikable Methode ist, die die Mechanik der
oberen Atemwege im Schlaf misst.
Gold et al. konnten zeigen, dass die Pcrit-Messung sowohl bei Normalpersonen,
Schnarchern, Patienten mit moderatem Schlafapnoe-Hypopnoe-Syndrom als

- 58 -
auch Patienten mit dem Vollbild einer obstruktiven Schlafapnoe durchgeführt
werden kann. Weiterhin konnte gezeigt werden, dass die pharyngeale
Kollapsibilität im Schlaf von Normalpersonen bis zu Patienten mit Obstruktiven
Schlafapnoe-Syndrom durch eine Zunahme des Pcrit charakterisiert ist.
Die Beobachtungen, dass interventionelle Eingriffe an den oberen Atemwegen
häufig die Qualität, jedoch nicht die Quantität schlafbezogener
Atmungsstörungen verändert, führte zu einer verbreiterten Akzeptanz der
Methode und zur weiterführenden Untersuchung der pharyngealen
Kollapsneigung26,29,126.
Die Pcrit-Messungen in dieser Untersuchung konnten zeigen, dass die
elektrische Stimulation des M. hypoglossus zu einer Verringerung des Pcrit um
bis zu 5 cm H2O führt 79,118,123. Die erreichte Reduktion des Pcrit führte jedoch
nicht komplett zu Eliminierung der schlafbezogenen Atmungsstörungen. So
zeigten alle Patienten noch Schnarchen und inspiratorische Flusslimitation
unter elektrischer Stimulation, während obstruktive Apnoen nicht mehr
festgestellt werden konnten 23,118.
Im Vergleich zu anderen Studien bei obstruktiver Schlafapnoe, bei denen eine
Pcrit-Messung vor und nach einer Intervention erfolgte, zeigten sich folgende,
mit dieser Untersuchung vergleichbare Ergebnisse. Sowohl bei operativer
Oberkiefer-Unterkiefervorverlagerung (MMO), die Uvulopalatopharyngeoplastie
(UPPP) oder eine Gewichtsabnahme zeigten sich bei bestimmten Patienten
Reduktionen des Pcrit um 3-5 cm H2O 57,59.
Diese Ergebnisse lassen den Schluss zu, dass eher Patienten mit einer
moderat gesteigerten pharyngealen Kollapsneigung von einer M. hypoglossus-
Stimulation profitieren, als Patienten die überwiegend Apnoen mit eine stark
gesteigerten pharyngealen Kollapsibilität aufweisen. Patienten mit einem Pcrit
zwischen –2 bis –5 cmH2O würden dann im Falle einer Reduktion des Pcrit um 5
cmH2O eine nahezu normale pharyngeale Kollapsneigung entwickeln 30.
Der Effekt der Hypoglossus-Stimulation ist außerdem durch den Kollapsort im
Pharynx beeinflusst, der durchaus variabel sein kann.
Die zusätzlich durchgeführten Messungen zur Feststellung des Kollapsortes
mittels Multilumenkatheter und Endoskopie während des Schlaf zeigten bei den
Patienten DF, JT und HL eine schlafassoziierte Obstruktion am Zungengrund
(so genannter retroglossaler Kollaps), wie er sich bei ca. 50% aller

- 59 -
Schlafapnoepatienten darstellt. Obstruktionen, die an diesem Ort im Pharynx
lokalisiert sind, würde am ehesten durch Manöver beseitigt werden, welche die
Zunge nach vorne bewegen. Es konnte gezeigt werden, dass die distale
Hypoglossus-Stimulation eine vergleichbare Zungenbewegung bewirkt, was die
verbessernden Effekte bei einigen Patienten zu erklären vermag.
Es bleibt jedoch anzumerken, dass bei der relativ kleinen Patientenzahl dieser
Studie keine sichere Aussage getroffen werden kann, ob der Therapieerfolg
eher durch den Kollapsort oder den Ausgangswert der Pcrit-Messung (Baseline-
Pcrit) determiniert wird.
5.4. Effekte der elektrischen Stimulation auf den S chlaf
In früheren Untersuchungen konnten gezeigt werden, dass z.B. die transkutane
elektrische Stimulation der oberen Atemwegsmuskulatur häufig zu
Weckreaktionen (sog. Mikroarousal) führt und so die Schlafstruktur der
Patienten stören kann.20,22,27,38,106,118. Die dabei erzielten Verbesserungen des
pneumotachographisch gemessenen Atemflusses im Schlaf wurde durch eine
allgemeine Tonuserhöhung der oberen Atemwegsmuskulatur induziert, ohne
dass eine selektive Stimulation einzelner ausgewählter Muskelgruppen unter
Beibehaltung der physiologischen Schlafstruktur erreicht werden konnte. Bei
der transkutanen Stimulation ergab sich das Problem höherer motorischer
Schwellenwerte, die unter anderem durch die hohen Hautwiderstände bedingt
waren. Die dabei notwendigen Amplitudenerhöhungen führten bei der
elektrischen Impulsgebung zu häufigen Weckreaktionen. Durch die unmittelbare
Nähe von Nerv und Elektrode konnte bei dem Schrittmacher-System von
niedrigeren motorischen Schwellenwerten ausgegangen werden. Mikroarousal
durch elektrische Stimulation und somit eine artifizielle Schlafstrukturstörung
konnten ausgeschlossen werden. Zum einen konnten im Schlaf-EEG relevante
Weckreaktionen (Alpha-Aktivierungen) während und nach der elektrischen
Impulsgebung bei allen Patienten ausgeschlossen werden. Zum anderen
zeigten sich keine typische Erhöhungen des Atemzugvolumens, welche nach
Weckreaktionen beobachtet werden.20,22,118
Außerdem hätten häufige Arousal durch die elektrische Stimulation zu
Störungen der Schlafarchitektur im Sinne einer Zunahme des instabilen

- 60 -
Schlafstadiums I und eine Abnahme der stabilen Schlafstadien II-IV und des
REM-Schlafes geführt. Die polysomnographischen Messungen während
kontinuierlicher elektrischer Stimulation im Schlaf zeigten jedoch eine Zunahme
vor allem der Tiefschlafstadien III-IV und eine Erhöhung der Weckreaktionen im
Vergleich zu den jeweiligen Ausgangsmessungen konnte ausgeschlossen
werden.
5.5. Implikationen
Zusammenfassend zeigen die gegenwärtigen Studienergebnisse, dass die
elektrische Stimulation des N. hypoglossus eine Behandlungsmöglichkeit zur
Therapie der obstruktiven Schlafapnoe darstellt. Weitere Studien sind jedoch
notwendig, um Selektionskriterien für geeignete Patienten zu definieren. Hierzu
müssen weitere Erkenntnisse aus den Baseline-Daten der Patienten gewonnen
werden, die insbesondere den Schweregrad des Schlafapnoesyndroms und
den pharyngealen Kollapsort mit einbeziehen. Es sollte zudem diskutiert
werden, ob eine weitere Optimierung des Therapieeffektes durch eine bilaterale
Stimulation beider Nn. hypoglossi erreicht werden könnte. Tierexperimentelle
Daten unterstützen diese These 42,66. Eine weitere Option stellte die simultane
Stimulation weiterer pharyngealer Muskeln dar, die einen stabilisierenden
Einfluss auf den Hypopharynx im Schlaf haben können (siehe Tabelle aus
Horner et. al., Kap.1.1.2.1. Koordination der oberen Atemwege im Schlaf).
Außerdem muss sich die elektrische Stimulation einer kritischen Evaluation
wichtiger klinischer Messgrößen unterziehen. Hierzu gehören objektivierbare
Maße die Müdigkeit, Leistungsfähigkeit, Schläfrigkeit und Effekte auf das
kardiovaskuläre System (z.B. arterielle Blutdruckmessung) umfassen.
Letztendlich müssen entsprechende Ergebnisse mit der Goldstandardtherapie-
Therapie, der CPAP-Therapie, verglichen werden und hier zumindest eine
Äquivalenz aufweisen.

- 61 -
6. Zusammenfassung
Alternative Therapiemöglichkeiten der obstruktiven Schlafapnoe neben der
CPAP-Therapie sind eher begrenzt. Die operative Oberkiefer-
Unterkiefervorverlagerung (MMO), Uvulopalatopharyngeoplastie (UPPP) oder
die Gewichtsabnahme können alleine nur unwesentlich die obstruktive
Schlafapnoe beeinflussen. Somit dominiert als Goldstandard die kontinuierliche
Überdruckbeatmung mittels einer Maske (CPAP/BiPAP). Voraussetzung dieser
Therapie ist jedoch, dass sich der Patient an das Tragen der Gesichtsmaske
gewöhnt und den applizierten Druck tolerieren kann. Eine berichtete
Langzeitcompliance von 50-80% bei der CPAP-Therapie zeigt jedoch, dass
eine klinische Evaluation von Therapiealternativen notwendig ist.
In dieser Arbeit konnte gezeigt werden, dass bei Patienten mit mäßiger
Kollapsneigung der oberen Atemwege, bestimmt durch die Messung des
kritischen pharyngealen Verschlussdruckes (Pcrit), die Implantation eines
Schrittmacher-System zur atmungsgetriggerten neuromuskulären Stimulation
des N. hypoglossus eine effiziente Therapie der obstruktiven Schlafapnoe sein
kann.
Sowohl im NREM- wie auch im REM-Schlaf führte die unilaterale Stimulation
des N. hypoglossus bei allen untersuchten Patienten (n=8) im Mittel zu einer
Reduktion der schlafbezogener Atmungsstörungen (Apnoe/Hypopnoe-Index).
Auch die Schlafqualität der Patienten konnte im Sinne einer Zunahme der
Tiefschlaf-Anteile während der elektrischen Stimulation verbessert werden.
In der speziell untersuchten Sub-Set-Gruppe (n=4) konnte zudem eine
Verringerung des Pcrit um bis zu 5 cm H2O Wassersäule verzeichnet werden.
Bei 2 Patienten kam es durch Verringerung des oberen Atemwegswiderstands
(Rus) zu einer Zunahme des inspiratorischen Luftflusses.
Darüber hinaus konnte gezeigt werden, dass die nächtliche Aktivität des
Schrittmachers weder die mechanische Bewegung (Protrusion) der Zunge,
noch die Schlafqualität in relevantem Ausmaß beeinflusst.
Auch wenn das nervale Schrittmacher-System eine Alternative zur Behandlung
der obstruktiven Schlafapnoe darstellt, so sind die qualitativen Ergebnisse
letztendlich nur mit der operativen Oberkiefer-Unterkiefervorverlagerung (MMO)
oder Uvulopalatopharyngeoplastie (UPPP) vergleichbar. Um die erzielten
Ergebnisse weiter zu verbessern, könnte eine beidseitige nervale Stimulation in

- 62 -
Erwägung gezogen werden. Letztlich muss der Effekt der nächtlichen
Stimulation gemessen an der täglichen Leistungsfähigkeit, Müdigkeit und der
kardiovaskulären Funktion eingeschätzt werden, damit sich die nervale
Stimulation des N. hypoglossus als eine therapeutische Option zur Behandlung
der Obstruktiven Schlafapnoe etablieren kann.

- 63 -
7. Literaturverzeichnis
1. American Sleep Disorders Association: EEG Arousals: Scoring Rules and Examples
Sleep 15, 173-184 (1992)
2. American Sleep Disorders Association: ICDS - International Classification of Sleep Disorders: Diagnostic and Coding Manual
Kansas, Allen Press (1997)
3. Auchincloss, J. j.; Cooke, E. und Ronzetti, A. D.: Clinica and Physiological Aspects of a Case of Obesity, Polycethemia and Alveolar Hypoventilation
J Clin Invest 34, 1537-1545 (1955)
4. Battagel, J. M. und L'Estrange, P. R.: The cephalometric morphology of patients with obstructive sleep apnoea (OSA)
Eur.J.Orthod. 18, 557-569 (1996)
5. Becker, H.; Brandenburg, U.; Peter, J. H. und von Wichert, P.: Reversal of Sinus Arrest and Atrioventricular Conduction Block in Patients with Sleep Apnea during Nasal Continuous Positive Airway Pressure
Am.J.Respir.Crit.Care Med. 151, 215-218 (1995)
6. Becker, H.; Faust, M.; Fett, I.; Kublik, A.; Peter, J. H.; Riess, M. und von Wichert, P.: Langzeitakzeptanz der nCPAP-Therapie bei 70 Patienten mit Schlafapnoe über eine Behandlungsdauer von mehr als 6 Monaten
Pneumol. 43, 643-646 (1989)
7. Becker, H.; Fett, I.; Riess, M.; Schneider, H.; Stammnitz, A.; Weber, K.; Peter, J. H. und von Wichert, P.: Mechanical Ventilation in the Treatment os Sleep-Related Breathing Disorders
In: Peter, J. H.; Penzel, T.; Podszus, T. und von Wichert, P.(eds.): Sleep and Health Risk
Berlin Heidelberg New York, Springer Verlag, 220-228 (1991)
8. Becker, H.; Stammnitz, A.; Schneider, H.; Peter, J. H. und von Wichert, P.: Die nasale continuous airway pressure (nCPAP) Therapie in der Behandlung von obstruktiven schlafbezogenen Atmungsstörungen (SBAS)
Dtsch.Med.Wschr. 129, 783-789 (1995)
9. Berthon-Jones, M. und Sullivan, C. E.: Ventilatory and arousal responses to hypoxia in sleeping humans
Am.Rev.Respir.Dis. 125, 632-639 (1982)

- 64 -
10. Bolm Audorff, U.; Köhler, U.; Becker, H.; Fuchs, E.; Mainzer, K.; Peter, J. H. und von Wichert, P.: Nächtliche Herzrhythmusstörungen bei Schlafapnoe-Syndrom
Dtsch.Med.Wschr. 109, 853-856 (1984)
11. Boot, H.; Poublon, R. M.; Van Wegen, R.; Bogaard, J. M.; Schmitz, P. I.; Ginai, A. Z. und Van der Meche, F. G.: Uvulopalatopharyngoplasty for the obstructive sleep apnoea syndrome: value of polysomnography, Mueller manoeuvre and cephalometry in predicting surgical outcome
Clin.Otolaryngol. 22 Suppl. 6, 504-510 (1997)
12. Boudewyns, A. N.; Punjabi, N.; Van de Heyning, P. H.; De Backer, W. A.; O'Donell, C. P.; Schneider, H.; Smith, P. L. und Schwartz, A. R.: An Abbreviated Method for Assessing Upper Airway Function in Obstructive Sleep Apnea
Chest 118(4), 1031-41 (2000)
13. Boudewyns, A. N.; Van de Heyning, P. H. und De Backer, W. A.: Site of upper airway obstruction in obstructive apnoea and influence of sleep stage
Eur.Respir.J. 10, 2566-2572 (1997)
14. Bristow, J. D.; Honour, A. J.; Pickering, T. G. und Sleight, P.: Cardiovascular and respiratory changes during sleep in normal and hypertensive subjects
Cardiovasc.Res. 3, 476-485 (1969)
15. Cartwright, R. D.; Diaz, F. und Lloyd, S.: The effects of sleep posture and sleep stage on apnea frequency
Sleep 14, 351-353 (1991)
16. Cassel, W. und Ploch, T.: Sleep Apnea and Accidents: Health Risk for Healthy People?
In: Peter, J. H.; Penzel, T.; Podszus, T. und von Wichert, P.(eds.): Sleep and Health Risk
Berlin Heidelberg New York, Springer Verlag, 297-285 (1991)
17. Clark, G. T.; Arand, D.; Chung, E. und Tong, D.: Effect of Anterior Mandibular Positioning on Obstructive Sleep Apnea
Am.Rev.Respir.Dis. 147, 624-629 (1993)
18. Coccagna, G.; Mantovani, M.; Brigani, F.; Parchi, C. und Lugaresi, E.: Continuous recording of the pulmonary and systemic arterial pressure during sleep in syndromes of hypersomnia with periodic breathing
Bull.Eur.Physiopathol.Respir. 8, 1159-1172 (1972)

- 65 -
19. Conradt, R.; Hochban, W.; Brandenburg, U.; Heitmann, J. und Peter, J. H.: Long-term follow-up after surgical treatment of obstructive sleep apnoea by maxillomandibular advancement
Eur.Respir.J. 10, 123-128 (1997)
20. Decker, M.; Haaga, J.; Arnold, J.; Atzberger, D. und Strohl, K.: Functional electrical stimulation and respiration during sleep
J.Appl.Physiol. 75, 1053-1061 (1993)
21. Douglas, N. J.: Control of Ventilation During Sleep In: Kryger, M. H.; Roth, T. und Dement, W. C.(eds.): Principles and
Practice of Sleep Medicine London Toronto Montreal Sydney Tokyo, W.B. Saunders Company, 204-
211 (1994)
22. Edmonds, L.; Daniels, B.; Stanson, A.; Sheedy, P. und Shepard, J. W., Jr.: The effects of transcutaneous electrical stimulation during wakefulness and sleep in patients with obstructive sleep apnea
Am.Rev.Respir.Dis. 146, 1030-1036 (1992)
23. Eisele, D.; Smith, P. L.; Alam, D. und Schwartz, A. R.: Direct hypoglossal nerv stimulation in obstructive sleep apnea
Arch.Otolaryngol Head Neck Surg 123, 57-61 (1997)
24. Fischer, J.; Mayer, G.; Peter, J. H.; Riemann, D. und Sitter, H.: Nicht-erholsamer Schlaf - Leitlinie "S2" der deutschen Gesellschaft für Schlafforschung und Schlafmedizin (DGSM)
Somnologie 5. Jahrgang (2002).
25. Flemons, W. W.; Remmers, J. E. und Gillis, A. M.: Sleep Apnea and Cardiac Arrhythmias - Is There a Relatiohship?
Am.Rev.Respir.Dis. 148, 618-621 (1993)
26. Fregosi, R. F.; Quan, S. F.; Morgan, W. L.; Goodwin, J. L.; Cabrera, R.; Shareif, I.; Fridel, K. W. und Bootzin, R. R.: Pharyngeal critical pressure in children with mild sleep-disordered breathing
J Appl Physiol 101, 734-739 (2006).
27. Gastaut, H.; Tassinari, C. und Duron, B.: Etude polygraphique des Manifestations episodiques (hypopniques et respiratoires) diurnes et nocturnes du Syndrome de Pickwick
Rev.Neurol. 112, 573-579 (1965)
28. Gleadhill, I. C.; Schwartz, A. R.; Schubert, N. M.; Wise, R. A.; Permutt, S. und Smith, P. L.: Upper Airway Collapsibility in Snorers and in patients with Obstructive Hypopnea and Apnea
Am.Rev.Respir.Dis. 143, 1300-1303 (1991)

- 66 -
29. Gold, A. R.; Marcus, C. L.; Dipalo, F. und Gold, M. S.: Upper Airway Collapsibility During Sleep in Upper Airway Resistance Syndrome
Chest 121, 1531-1540 (2002).
30. Gold, A. R. und Schwartz, A. R.: The Pharyngeal Critical Pressure: The Whys and Hows of Using Nasal Continuous Positive Airway Pressure Diagnostically
Chest 110, 1077-1088 (1996)
31. Grote, L. und Schneider, H.: Diagnostische Verfahren Schlafapnoe und kardiovaskuläre Erkrankungen Stuttgart New York, Georg Thieme Verlag, 22-39 (1996)
32. Grote, L. und Schneider, H.: Schlafbezogene Atmungsstörungen (SBAS) Schlafapnoe und kardiovaskuläre Erkrankungen Stuttgart New York, Georg Thieme Verlag, 40-64 (1996)
33. Grote, L. und Schneider, H.: Schlafmedizinische Grundlagen Schlafapnoe und kardiovaskuläre Erkrankungen Stuttgart New York, Georg Thieme Verlag, 8-21 (1996)
34. Grote, L. und Schneider, H.: Therapie schlafbezogener Atmungsstörungen
Schlafapnoe und kardiovaskuläre Erkrankungen Stuttgart New York, Georg Thieme Verlag, 87-104 (1996)
35. Guilleminault, C.; Connolly, S.; Winkle, R. A. und Melvin, K.: Cyclical Variation of the Heart Rate in Sleeep Apnoea Syndrome
Lancet I, 126-131 (1984)
36. Guilleminault, C.; Eldrigde, F. L. und Dement, W. C.: Insomnia with sleep apnea. A new syndrome
Science 181, 856-858 (1973)
37. Guilleminault, C.; Eldrigde, F. L.; Simmon, F. B. und Dement, W. C.: Sleep Apnea Syndrome: Can It Induce Haemodynamic Changes?
West.J.Med. 123, 7-16 (1975)
38. Guilleminault, C.; Powell, N. B.; Bowman, B. und Stoohs, R.: The effect of electrical stimulation on obstructive sleep apnea syndrome
Chest 107, 67-73 (1995)
39. Guilleminault, C.; Stuart, J.; Connolly, S. und Winkle, R. A.: Cardiac Arrhythmia and Conduction Disturbances During Sleep in 400 Patients with Sleep Apnea Syndrome
Am.J.Cardiol. 52, 490-494 (1983)

- 67 -
40. Guilleminault, C.; Tilkian, A. und Dement, W. C.: The sleep apnea syndromes
Ann.Rev.Med. 465-484 (1976)
41. He, J.; Kryger, M. H.; Zorick, F. J.; Conway, W. und Roth, T.: Mortality and Apnea Index in Obstructive Sleep Apnea
Chest 94, 9-14 (1988)
42. Hida, W.; Kurosawa, H.; Okabe, S.; Kikuchi, Y.; Midorikawa, J.; Chung, Y.; Takishima, T. und Shirato, K.: Hypoglossal nerv stimulation affects the pressure behavior of the upper airway
Am.J.Respir.Crit.Care Med. 151, 455-60 (1995).
43. Hierl, T.; Humpfner-Hierl, H.; Frerich, B.; Heisgen, U.; Hemprich, A. und Bosse-Henck, A.: Severity of obstructive sleep apnea syndrome - correlation with cephalometric parameters
Wien.Med.Wochenschr. 146, 361-363 (1996)
44. Hochban, W.: Das Obstruktive Schlafapnoesyndrom - Diagnostik und Therapie unter besonderer Berücksichtigung craniofazialer Anomalien
Berlin, Blackwell Verlag (1995)
45. Hochban, W. und Brandenburg, U.: Gesichtsskelettverlagernde Eingriffe beim OSAS: Mund- und kieferchirurgische Aspekte
In: Peter, J. H.; Penzel, T.; Cassel, W. und von Wichert, P.(eds.): Schlaf - Atmung - Kreislauf
Berlin Heidelberg New York, Springer Verlag, 250-269 (1993)
46. Hochban, W.; Brandenburg, U. und Kunkel, M.: Die chirurgische Behandlung des obstruktiven Schlafapnoesyndroms durch Gesichtsskelettosteotomien
Pneumol. 47 Suppl 4, 761-765 (1993)
47. Hochban, W.; Brandenburg, U. und Peter, J. H.: Die operative Behandlung von Patienten mit obstruktivem Schlaf-Apnoe-Syndrom durch Gesichtsskelettosteotomien
In: Meier-Ewert, K. und Rüther, E.(eds.): Schlafmedizin Stuttgart, G. Fischer Verlag, 316-320 (1993)
48. Hoffstein, V. und Mateika, S.: Cardiac Arrhythmia, Snoring, and Sleep Apnea
Chest 106, 466-471 (1994)
49. Horner, R. L.: Motor Control of the Pharyngeal Musculature and Implications for the Pathogenesis of Obstructive Sleep Apnea
Sleep 19, 827-853 (1996)

- 68 -
50. Hudgel, D. W.: Variable site of airway narrowing among obstructive sleep apnea patients
J.Appl.Physiol. 61, 1403-1409 (1986)
51. Hung, J.; Withford, E. G.; Parsons, R. W. und Hillman, D. R.: Association of sleep apnoea with myocardial infarction in men
Lancet 336, 261-264 (1990)
52. Isono, S. und Remmers, J. E.: Anatomy and Physiology of Upper Airway Obstruction
In: Kryger, M. H.; Roth, T. und Dement, W. C.(eds.): Principles and Practice of Sleep Medicine
London Toronto Montreal Sydney Tokyo, W.B. Saunders Company, 642-656 (1994)
53. Isono, S.; Remmers, J. E.; Tanaka, A.; Sho, Y.; Sato, J. und Nishino, T.: Anatomy of pharynx in patients with obstructive sleep apnea and in normal subjects
J.Appl.Physiol. 82, 1319-1326 (1997)
54. Knaack L.; Hochban, W.; Heitmann, J.; Podszus, T. und Peter, J. H.: Hypoglossal nerve stimulation: A new treatment of Obstructive sleep apnea
J.cranio-max.fac.Surg. 26, Suppl 1, 75 (1998).
55. Knaack L.; Hochban, W.; Schwartz, A. R.; Smith, P. L.; O'Hearn, D.; Schneider, H.; Eisele, D.; Peter, J. H. und von Wichert, P.: Effekte der unilateralen Stimulation des N Hypoglossus auf die Funktion der Oberen Atemwege bei Patienten mit Obstruktiver Schlafapnoe
Somnologie Suppl.1, 123 (1998).
56. Knaack, L.: Die oberen Atemwege im Schlaf In: Schulz, H.(eds.): Kompendium Schlafmedizin für Ausbildung, Klinik
und Praxis Landsberg Lech, ecomed verlag, 1-3 (1998)
57. Knaack, L.; Canisius, S.; Hochban, W.; Penzel, T.; Schneider, H. und Peter, J. H.: Maxillo-Mandibulo-Advancement reduces sleep disordered breathing but does not normalize upper airway mechanics
2000 ALA/ATS International Conference (1999).
58. Knaack, L.; Canisius, S.; Hochban, W.; Schneider, H. und Peter, J. H.: Effekte von Körpergewicht und kephalometrischen Parametern auf die pharyngeale Kollapsibilität bei obstruktiver Schlafapnoe
Abstract der Jahrestagung SNAK/AGAP (1999).
59. Knaack, L.; Hochban, W.; von Elten, A. und Peter, J. H.: Pharyngeale Mechanik bei obstruktiver Schlafapnoe nach mandibulärer Protrusion
Somnologie 3, Suppl.1, 1-66 (1999)

- 69 -
60. Koella, W. P.: Die Physiologie des Schlafes Stuttgart New York, Fischer Verlag (1988)
61. Köhler, U.; Fett, I.; Hay, J.; Lübbeke, A.; Ploch, T.; Wolff, H. und Zindler, G.: Bradykarde Herzrhyrhmusstörungen im Schlaf: Das Morbiditätsspektrum bei Patienten mit Schlafapnoe und nächtlichen bradykarden Rhythmusstörungen
In: Peter, J. H.; Cassel, W. und Penzel, T.(eds.): Schlaf -Atmung - Kreislauf
Berlin Heidelberg New York, Springer, 374-383 (1993)
62. Kribbs, N. B.; Pack, A. I.; Kline, L. R.; Smith, P. L.; Schwartz, A. R.; Schubert, N. M.; Redline, S.; Henry, J. N.; Getsy, J. E. und Dinges, D. F.: Objective measurement of patterns of nasal CPAP use by patients with obstructive sleep apnea
Am.Rev.Respir.Dis. 147, 887-895 (1993)
63. Krieger, J.: Breathing during sleep in normal subjects In: Kryger, M. H.; Roth, T. und Dement, W. C.(eds.): Principles and
practice of sleep medicine Philadelphia London Toronto Montreal Sydney Tokyo, W.B. Saunders
Company, 212-223 (1994)
64. Krieger, J.; Turlot, J. C.; Mangin, P. und Kurtz, D.: Breathing during sleep in normal young and elderly subjects. Hypopnea, apneas, and correlated factors
Sleep 6, 108-120 (1983)
65. Kuhlo, W.; Doll, E. und Frank, M. C.: Erfolgreiche Behandlung eines Pickwick-Syndromes durch eine Dauertrachealkanüle
Deutsche Medizinische Wochenschrift 94, 1286-1290 (1969)
66. Kuna, S. und Brennick, M.: Effects of Pharyngeal Muscle Activation on Airway Pressure-Area Relationships
Am.J.Respir.Crit.Care Med. 166. pp., 972-977 (2002).
67. Lavie, P.: Incidence of sleep apnea in a presumably healthy working population: A significant relationship with excessive daytime sleepiness
Sleep 6, 312-318 (1983)
68. Lavie, P.; Kremermann, S. und Weil, M.: Sleep Disorders and Safety at Work in Industrial Workers
Accod.Anal.Prev. 14, 311-314 (1982)
69. Lowe, A. A.; Fleetham, J. A.; Adachi, S. und Ryan, C. F.: Cephalometric and computed tomographic predictors of obstructive sleep apnea severity
Am.J.Orthod.Dentofacial.Orthop. 107, 589-595 (1995)

- 70 -
70. Lowe, A. A.; Santamaria, J. D.; Fleetham, J. A. und Price, C.: Facial morphology and obstructive sleep apnea
Am J.Orthod.Dentofacial.Orthop. 90, 484-491 (1986)
71. Lyberg, T.; Krogstad, O. und Djupesland, G.: Cephalometric analysis in patients with obstructive sleep apnoea syndrome I: Skeletal morphology
J.Laryngol.Otol. 103, 287-292 (1989)
72. Lyberg, T.; Krogstad, O. und Djupesland, G.: Cephalometric analysis in patients with obstructive sleep apnoea syndrome II: Soft tissue morphology
J.Laryngol.Otol. 103, 293-297 (1989)
73. Mayer, G. und Meier-Ewert, K.: Cephalometric predictors for orthopaedic mandibular advancement in obstructive sleep apnoea
Eur.J.Orthod. 17, 35-43 (1995)
74. McKenzie Neill, A.; Angus, M. S.; Sajkov, D. und McEvoy, R. D.: Effects of Sleep Posture on upper Airway Stability in Patients with Obstructive Sleep Apnea
Am.J.Respir.Crit.Care Med. 155, 199-204 (1997)
75. Mezzanotte, W. S.; Tangel, D. G. und White, D. P.: Waking genioglossal elctomyogram in sleep apnea patients versus normal controls (a neuromuscular compensatory mechanism)
J.Clin.Invest. 89, 1571-1579 (1992)
76. Miller, W. P.: Cardiac Arrhythmias and Conduction Disturbances in the Sleep Apnea Syndrome
Am.J.Med. 73, 317-321 (1982)
77. Mitler, M. M.: Two-Peak 24-Hour Patterns in Sleep, Mortality, and Error In: Peter, J. H.; Penzel, T.; Podszus, T. und von Wichert, P.(eds.): Sleep
and Health Risk Berlin Heidelberg New York, Springer Verlag, 65-77 (1991)
78. Mortimore, I. A.; Marshall, I.; Wraith, P. K.; Sellar, R. J. und Douglas, N. J.: Neck and Total Body Fat Deposition in Nonobese and Obese Patients with Sleep Apnea Compared with That in Control Subjects
Am.J.Respir.Crit.Care Med. 157, 280-283 (1998)
79. O'Hearn, D.; Schneider, H.; LeBlanc, K.; Schubert; O'Donell, C. P. und Smith, P. L.: Effect of unilateral hypoglossal stimulation on upper airway function
Am.J.Respir.Crit.Care Med. 157 (3) (1998)

- 71 -
80. Odeh, M.; Schnall, R.; Gavriely, N. und Oliven, A.: Dependency of upper airway patency on head position: The effect of muscle contraction
Respir.Physiol. 100, 239-244 (1995)
81. Okada, H.; Iwase, S.; Mano, T.; Sugiyama, Y. und Watanabe, T.: Changes in muscle sympathetic nerve activity during sleep in humans
Neurology 41, 1961-1966 (1991)
82. Partinen, M. und Guilleminault, C.: Long-term Outcome for Obstructive Sleep Apnea
In: Peter, J. H.; Penzel, T.; Podszus, T. und von Wichert, P.(eds.): Sleep and Health Risk
Berlin Heidelberg New York, Springer Verlag, 108-115 (1991)
83. Penzel, T.; Hein, H.; Rasche, K.; Weeß, H.-G.; Fischer, J.; Hajak, G.; Mayer, G.; Wiater, A. und Zulley, J.: Leitfaden für die Akkreditierung von schlafmedizinischen Zentren der deutschen Gesellschaft für Schlafforschung und Schlafmedizin (DGSM)
Somnologie 4, 181-187 (2000)
84. Penzel, T. und Peter, J. H.: Problem-Oriented Diagnosis of Sleep disorders Using Computerized Methods
In: Peter, J. H.; Penzel, T.; Podszus, T. und von Wichert, P.(eds.): Sleep and Health Risk
Berlin Heidelberg New York, Springer Verlag, 11-19 (1991)
85. Pepin, J. L.; Ferretti, G.; Veale, D.; Romand, P.; Coulomb, M.; Brambilla, C. und Levy, P. A.: Somnofluoroscopy, computed tomography, and cephalometry in the assessment of the airway in obstructive sleep apnoea
Thorax 47, 150-156 (1992)
86. Peter, H.; Penzel, T. und Peter, J. H.: Enzyklopädie der Schlafmedizin Stuttgart, Springer Medizin Verlag (2007)
87. Peter, J. H.: Die Erfassung der Schlafapnoe in der Inneren Medizin Stuttgart New York, Georg Thieme Verlag (1987)
88. Peter, J. H.: Störungen der Atmungsregulation
In: Hornbostel, H.; Kaufmann, W. und Siegenthaler, W.(eds.): Innere Medizin in Praxis und Klinik, Band 1 : Herz, Gefäße, Atmungsorgane, Endokrines System
Stuttgart New York, Georg Thieme Verlag, 3.263-3.280 (1992)

- 72 -
89. Peter, J. H.; Becker, H.; Blanke, J.; Clarenbach, P.; Mayer, G.; Raschke, F.; Rühle, K. H.; Rüther, E.; Schläfke, M. und Schönbrunn, E.: Empfehlungen zur Diagnostik, Therapie und Langzeitbetreuung von Patienten mit Schlafapnoe
Med.Klin. 86, 46-50 (1991)
90. Peter, J. H.; Blanke, J.; Cassel, W.; Clarenbach, P.; Elek, H.; Faust, M.; Fietze, I.; Lund, R.; Mahlo, H. W. und Mayer, G.: Empfehlungen zur ambulanten Diagnostik der Schlafapnoe
Med.Klin. 87, 310-317 (1992)
91. Peter, J. H.; Bolm Audorff, U.; Eble, R.; Meinzer, K.; Penzel, T. und von Wichert, P.: Schlafapnoe und essentielle Hypertonie
Ver.Dtsch.Ges.Inn.Med. 89, 1132-1135 (1983)
92. Peter, J. H.; Hess, U.; Himmelmann, H.; Köhler, U.; Mayer, J.; Podszus, T.; Siegrist, J. und Sohn, E.: Sleep Apnea Activity and General Morbidity in a Field Study
In: Peter, J. H.; Podszus, T. und von Wichert, P.(eds.): Sleep Related Disorders and Internal Diseases
Berlin Heidelberg New York, Springer Verlag, 248-253 (1989)
93. Peter, J. H.; Podszus, T.; Becker, H. und von Wichert, P.: Schlafbezogene Atmungsstörungen - Schlafapnoe
Dtsch.Ärztebl. 86, 1478-1483 (1989)
94. Peter, J. H.; Siegrist, J.; Podszus, T.; Mayer, J.; Selzer, K. und von Wichert, P.: Prevalence of sleep apnea in healthy industrial workers
Klin.Wochenschr. 63, 807-811 (1985)
95. Petrof, B. J.; Pack, A. I.; Kelly, A. M.; Eby, J. und Hendricks, J. C.: Pharyngeal myopathy of loaded upper airway in dogs with sleep apnea
J.Appl.Physiol. 76, 1746-1752 (1994)
96. Phillipson, E. und Remmers, J. E.: American Thoracic Society Consensus Conference on Indications and Standards for Cardiopulmonary Sleep Studies
Am.Rev.Respir.Dis. 139, 559-568 (1989)
97. Podszus, T.: Beziehungen zwischen Herz-Kreislauferkrankungen und nächtlichen Atemregulationsstörungen
In: Dtsch.Gesellsch.Inn.Med.(eds.): Verhandlungen der Deutschen Gesellschaft für Innere Medizin
München, J.F. Bergmann Verlag, 341-345 (1988)
98. Podszus, T.; Bauer, W.; Mayer, J.; Penzel, T.; Peter, J. H. und von Wichert, P.: Sleep apnea and pulmonary hypertension
Klin.Wochenschr. 64, 131-134 (1986)

- 73 -
99. Podszus, T.; Becker, H.; Dorow, P.; Köhler, D.; Peter, J. H.; Raschke, F. und Schulz, V.: Empfehlungen zur nächtlichen nasalen Beatmungstherapie bei Atmungsstörungen
Pneumol. 47, 333-335 (1993)
100. Podszus, T.; Greenberg, H. und Scharf, S. M.: Influence of Sleep State and Sleep-Disordered Breathing on Cardiovascular Function
In: Saunders, N. A. und Sullivan, C. E.(eds.): Sleep and Breathing New York Basel Hong Kong, M. Dekker, 257-310 (1994)
101. Podszus, T. und von Wichert, P.: Schlafapnoe und Herzinsuffizienz - Pathophysiologie und Epidemiologie
Prax.Klin.Pneumol. 41, 394-396 (1987)
102. Powell, N. B.; Riley, R. W. und Robinson, A.: Surgical Management of Obstructive Sleep Apnea Syndrome
Chest 19, 77-86 (1998)
103. Rasche, K.; Orth, M.; Duchna, H. W.; Ullrich, H. U. und Schultze Werninghaus, G.: CPAP-Therapie bei obstruktiven Schlafapnoesyndrom: Nebenwirkungen und Akzeptanz im Langzeitverlauf
Med.Klin. 89, 86-88 (1994)
104. Rechtschaffen, A. und Kales, A.: A manual of standardized terminology, techniques and scoring system for sleep stages of human subjects
Washington DC, US Government Printing Service (1968)
105. Reeves-Hoche, M. K.; Meck, R. und Zwillich, C. W.: Nasal CPAP: an objective evaluation of patient compliance
Am.J.Respir.Crit.Care Med. 149, 149-154 (1994)
106. Remmers, J. E.; DeGroot, W. J.; Sauerland, E. K. und Anch, A. M.: Pathogenesis of upper airway occlusion during sleep
J.Appl.Physiol. 44, 931-938 (1978)
107. Riley, R. W.; Powell, N. B. und Guilleminault, C.: Obstructive sleep apnea syndrome: a surgical protocol for dynamic upper airway reconstruction
J.Oral.Maxillofac.Surg. 51, 742-749 (1993)
108. Rivlin, J.; Hoffstein, V.; Kalbfleisch, J.; McNicholas, W.; Zamel, N. und Byran, A. C.: Upper airway morphology in patients with idiopathic obstruktive sleep apnea
Am.Rev.Respir.Dis. 129, 355-360 (1984)
109. Rolfe, I.; Olson, L. G. und Saunders, N. A.: Long-term acceptance of continuous positive airway pressure in obstructive sleep apnea
Am.Rev.Respir.Dis. 144, 1130-1133 (1991)

- 74 -
110. Rowley, J. A.; Permutt, S.; Willey, S.; Smith, P. L. und Schwartz, A. R.: Effect of tracheal and tongue displacement on upper airway airflow dynamics
J.Appl.Physiol. 80, 2171-2178 (1996)
111. Rowley, J. A.; Williams, B. C.; Smith, P. L. und Schwartz, A. R.: Neuromuscular Activity and Upper Airway Collapsibility: Mechanism of Action in the Decerebrate Cat
Am.J.Respir.Crit.Care Med. 156, 515-521 (1997)
112. Safwan Badr, M.: Pathophysiology of upper airway obstruction during sleep
Chest 19, 21-32 (1998)
113. Sauerland, E. K. und Harper, R. M.: The Human Tongue during Sleep: Electromyographic Activity of the Genioglossus Muscle
Experiment.Neurology 51, 160-170 (1976)
114. Sauerland, E. K.; Orr, W. C. und Hairston, L. E.: EMG Patterns of oropharyngeal muscles during respiration in wakefulness and sleep
Electromyogr.Clin.Neurophysiol. 21, 307-316 (1981)
115. Schneider, H.; Boudewyns, A. N.; Smith, P. L.; O'Donell, C. P.; Canisius, S. und Stammnitz, A.: Modulation of upper airway collapsibility during sleep: influence of respiratory phase and flow regimen
J Appl Physiol 93, 1365-1376 (2002).
116. Schönhofer, B.; Wenzel, M.; Barchfeld, T.; Siemon, K.; Rager, H. und Köhler, D.: Wertigkeit verschiedener intra- und extraoraler Therapieverfahren für die Behandlung der obstruktiven Schlafapnoe und des Schnarchens
Med.Klin. 92, 167-174 (1997)
117. Schwartz, A. R.; Bennet ML; Smith, P. L.; De Backer, W. A.; Hedner, J. A.; Boudewyns, A. N.; Van de Heyning, P. H.; Ejnell H; Hochban, W.; Knaack, L.; Penzel, T.; Peter, J. H.; Goding GS; Testerman, R.; Ottenhoff F; Eisele, D. und Podszus, T.: Therapeutic electrical stimulation of the hypoglossal nerve in obstruvtive sleep apnea
Arch.Otolaryngol Head Neck Surg 127, 1216-23 (2001).
118. Schwartz, A. R.; Eisele, D. W.; Hari, A.; Testerman, R.; Erickson, D. und Smith, P. L.: Electrical stimulation of the lingual musculature in obstructive sleep apnea
J.Appl.Physiol. 81, 643-652 (1996)
119. Schwartz, A. R.; Gold, A. R.; Schubert, N.; Stryzak, A.; Wise, R. A.; Permutt, S. und Smith, P. L.: Effect of weight loss on upper airway collapsibility in obstructive sleep apnea
Am.Rev.Respir.Dis. 144, 494-498 (1991)

- 75 -
120. Schwartz, A. R.; Rowley, J. A.; Thut, D. C.; Permutt, S. und Smith, P. L.: Structural Basis for Alterations in Upper Airway Collapsibility
Sleep 19, 184-188 (1996)
121. Schwartz, A. R.; Schubert, N. M.; Rothman, W.; Godley, F.; Marsh, B.; Eisele, D.; Nadeau, J.; Permutt, L.; Gleadhill, I. C. und Smith, P. L.: Effect of Uvulopalatopharyngoplasty on Upper Airway Collapsibility in Obstructive Sleep Apnea
Am.Rev.Respir.Dis. 145, 527-532 (1992)
122. Schwartz, A. R.; Smith, P. L.; Kashima, H. K. und Proctor, D. F.: Respiratory Function of the Upper Airways
In: Murray, J. F. und Nadel, J. A.(eds.): Textbook of respiratory medicine Philadelphia, W.B. Saunders Company, 1451-1470 (1994)
123. Schwartz, A. R.; Smith, P. L.; Wise, R. A.; Bankman, I. und Permutt, S.: Effect of positive nasal pressure on upper airway pressure-flow relationships
J.Appl.Physiol. 66, 1626-1634 (1989)
124. Schwartz, A. R.; Smith, P. L.; Wise, R. A.; Gold, A. R. und Permutt, S.: Induction of upper airway occlusion in sleeping individuals with subatmospheric nasal pressure
J.Appl.Physiol. 64(2), 535-542 (1988)
125. Schwartz, A. R.; Thut, D. C.; Russ, B.; Seelagy, M.; Yuan, X.; Brower, R. G.; Permutt, S.; Wise, R. A. und Smith, P. L.: Effect of Electrical Stimulation of the Hypoglossal Nerve on Airflow Mechanics in the Isolated Upper Airway
Am.Rev.Respir.Dis. 147, 1144-1150 (1993)
126. Sforza, E.; Petiau, C.; Weiss, Th.; Thibault, A. und Krieger, J.: Pharyngeal Critical Pressure in Patients with Obstructive Sleep Apnea Syndrome
Am.J.Respir.Crit.Care Med. 159, 149-157 (1999).
127. Shepard, J. W., Jr. und Thawley, S. E.: Localization of Upper Airway Collaps during Sleep in Patients with Obstructive Sleep Apnea
Am.Rev.Respir.Dis. 141, 1350-1355 (1990)
128. Shepard, J. W. J.: Gas exchange and haemodynamics during sleep Med.Clin.North Am. 69, 1243-1264 (1985)
129. Shepard, J. W. J.; Garrison, M. W.; Grither, D. A. und Dolan, G. F.: Relationship of ventricular ectopy to oxyhemoglobin desaturation in patients with obstructive sleep apnea
Chest 88, 335-340 (1985)

- 76 -
130. Smith, P. L.; Eisele, D. W.; Podszus, T.; Penzel, T.; Grote, L.; Peter, J. H. und Schwartz, A. R.: Electrical Stimulation of Upper Airway Musculature
Sleep 19, 284-287 (1996)
131. Somers, V. K.; Dyken, M. E.; Clary, M. P. und Abboud, F. M.: Sympathetic Neural Mechanisms in Obstructive Sleep Apnea
J.Clin.Invest. 96, 1897-1904 (1995)
132. Stephan, S.; Cassel, W.; Schwarzenberger-Kesper, F.; Fett, I.; Henn-Kolter, C. und Peter, J. H.: Psychological Problems Correlated with Sleep Apnea
In: Peter, J. H.; Penzel, T.; Podszus, T. und von Wichert, P.(eds.): Sleep and Health Risk
Berlin Heidelberg New York, Springer Verlag, 167-173 (1991)
133. Strelzow, V. V.; Blanks, R. H.; Basile, A. und Strelzow, A. E.: Cephalometric airway analysis in obstructive sleep apnnea syndrome
Laryngoscope 98, 1149-1158 (1988)
134. Sullivan, C. E.; Issa, F. G.; Berthon-Jones, M. und Eves, L.: Reversal of Obstructive Sleep Apnea by Continuous Positive Airway Pressure Applied Through the Nares
Lancet I, 862-865 (1981)
135. Sullivan, C. E.; Issa, F. G.; Berthon-Jones, M.; McCauley, V. B. und Costas, L. J. V.: Home Treatment of Obstructive Sleep Apnea with Continuous Positive Airway Pressure Applied Through a Nose-Mask
Bull.Eur.Physiopathol.Respir. 20, 49-54 (1984)
136. Sullivan, C. E.; Issa, F. G.; Berthon-Jones, M. und Saunders, N. A.: Pathophysiology of sleep apnea
In: Saunders, N. A. und Sullivan, C. E.(eds.): Sleep and Breathing Lung Biology in Health and Disease
New York Basel Hong Kong, M. Dekker, 299-364 (1984)
137. Suratt, P. M.; McTier, R. F. und Wilhoit, S. C.: Collapsibility of the Nasopharyngeal Airway in Obsructive Sleep Apnea
Am.Rev.Respir.Dis. 132, 967-971 (1985)
138. Synder, F.; Hobson, J. A.; Morrisson, D. F. und Goldfrank, F.: Changes in respiration, heart rate, and systolic blood pressure in human sleep
J.Appl.Physiol. 19, 417-422 (1964)
139. Tilkian, A. G.; Guilleminault, C.; Schroeder, J. S.; Lehrman, K. L.; Blair Simmons, F. und Dement, W. C.: Sleep-Induced Apnea Syndrome, Prevalence of Cardiac Arrhythmias and their Reversal after Tracheostomy
Am.J.Med. 63, 348-358 (1977)

- 77 -
140. Webb, P.: Periodic breathing during sleep J.Appl.Physiol. 37, 899-903 (1974)
141. Wilcox, I.; Grunstein, R. R.; Hedner, J. A.; Doyle, J.; Collins, F. L.; Fletcher, P. J.; Kelly, D. T. und Sullivan, C. E.: Effect of nasal continuous positive airway pressure during sleep on 24-hour blood pressure in obstructive sleep apnea
Sleep 16, 539-544 (1993)
142. Woodson, B. T. und Conley, S. F.: Prediction of uvulopalatopharyngoplasty response using cephalometric radiographs
Am.J.Otolaryngol. 18, 179-184 (1997)
143. Yildirim, N. M.; Fitzpatrick, M. F.; Whyte, K. F.; Jalleh, R.; Wightman, A. J. A. und Douglas, N. J.: The effects of posture on upper airway dimensions in normal subjects and in patients with the sleep apnea syndrome
Am.Rev.Respir.Dis. 144, 845-847 (1991)
144. Young, T.; Palta, M.; Dempsey, J.; Skatrud, J.; Weber, S. und Badr, S.: The occurence of sleep disordered breathing among middle-aged adults
N.Engl.J.Med. 328, 1230-1235 (1993)
145. Zermaityte, D.; Varoneckas, G. und Sokolov, E.: Heart rhythm control during sleep
Psychophysiology 21, 279-289 (1984)
146. Zucconi, M.; Ferini-Strambi, L.; Palazzi, S.; Orena, C.; Zonta, S. und Smirne, S.: Habitual snoring with and without obstructive sleep apnoea: the importance of cephalometric variables
Thorax 47, 157-161 (1992)
147. Zucconi, M.; Oldani, A.; Ferini-Strambi, L.; Calori, G.; Castronovo, C. und Smirne, S.: EEG arousal pattern in habitual snorers with an without obstructive sleep apnoea
J.Sleep Res. 4, 107-112 (1995)

- 78 -
8. Anhang
8.1. Abkürzungsverzeichnis
AHI Apnoe- Hypopnoe- Index
AI Apnoe- Index
ASDA American Sleep Disorders Association
BMI Body Mass Index
COPD Chronical Obstructive Pulmonary Disease
EEG Elektroenzephalogramm
EKG Elektrokardiographie
EMG Elektromyogramm
EOG Elektroocculogramm
HI Hypopnoe- Index
ICSD International Classification of Sleep Disorders
IPPV Intermittent Positive Pressure Ventilation
KRPSG Kardiorespiratorische Polysomnographie
MESAM IV vierkanaliger Madaus Elektronik Schlaf Apnoe Monitor
MMO Maxillo-Mandibulare Osteotomie
N. Nervus
Nn. Nervi
nBIPAP nasal BI Level Positive Airway Pressure
nCPAP nasal Continuous Positive Airway Pressure
NREM Non Rapid Eye Movement
OSA Obstruktive Schlafapnoe
Pcrit kritischer pharyngealer Verschlussdruck, Druck im kollabilen
Segment
Pds Druck des sog. „downstream“ Segments; das Segment, das
unterhalb des kollabilen Segments liegt
Pin Intraluminaler Druck
Pout Umgebungsdruck
Pus Druck des sog. „upstream“ Segments; das Segment, das oberhalb
des kollabilen Segments liegt
RDI Respiratory Disturbance Index

- 79 -
Rds unterer Atemwegswiderstand
REM Rapid Eye Movement
Rph pharyngealer Widerstand
Rus oberer Atemwegswiderstand
SBAS Schlafbezogene Atmungsstörungen
SO2 Sauerstoffsättigung
TST Total Sleep Time
UPPP Uvulopalatopharyngoplastik
V Volumenfluss
8.2. Verzeichnis der Abbildungen
Abb.1: Das Starling-Resistor Modell
Abb.2: Ausmaß der pharyngealen Kollapsibilität korreliert mit der
Ausprägung der schlafbezogenen Atmungsstörungen
Abb.3: Mögliche Einflussfaktoren der pharyngealen Kollapsibilität
Abb.4: Beispielabbildung einer polysomnographischen Registrierung mit
den Elektrodenpositionen für deren Ableitung
Abb.5: Schematische Zeichnung des Versuchsaufbaus zur Messung des
kritischen pharyngealen Verschlussdruckes
Abb.6: Registrierbeispiel einer Kardiorespiratorischen Polysomnographie
mit zusätzlicher Messung des kritischen pharyngealen
Verschlussdruckes Pcrit
Abb.7: Darstellung von Masken- und Flusskurven im Verlauf eines
Atemzyklus
Abb.8: Schematische Zeichnung eines implantierbaren N. Hypoglossus
Stimulationssystems
Abb.9: Schnittführung und Kabelverlauf des N. Hypoglossus-
Stimulationssystems am Patienten
Abb.10: Polysomnographische Aufzeichnung mit und ohne
Schrittmacherfunktion
Abb.11: Veränderung des Apnoe/Hypopnoe-Index bei den
Studienpatienten

- 80 -
Abb.12: Registrierbeispiele von Drucksenkungsversuchen in NREM-Schlaf
in Rückenlage links vor Schrittmacherimplantation, rechts nach
Schrittmacherimplantation
Abb.13: Pressure-Plots für Druck-Fluss-Beziehung bei Patienten in NREM-
und REM-Schlaf mit und ohne Schrittmachereffekt
Abb.14: Veränderung des Pcrit unter Stimulation
Abb.15: Veränderung des Rus unter Stimulation
Abb.16: Registrierbeispiel für Artefakte, die zu keinen therapeutischen
Effekten führten
8.3. Verzeichnis der Tabellen
Tabelle 1: Funktionsweise der an Inspiration und Exspiration beteiligter
Muskeln nach Horner et al.
Tabelle 2: Präoperative Ausgangswerte und Index für schlafbezogene
Atmungsstörungen des Patientenkollektivs
Tabelle 3: Veränderung der schlafbezogenen Atmungsstörungen der
Studienpatienten
Tabelle 4: Veränderung der Schlafarchitektur der Studienpatienten
Tabelle 5: Veränderung der Schrittmacher-Implantationsparameter während
des Studienzeitraums
Tabelle 6: Veränderung des Apnoe/Hypopnoe-Index, kritischer
Verschlussdruck (Pcrit) und Widerstand der oberen Atemwege
(Rus) des Patientenkollektivs
8.4. Danksagung
Ich danke Herrn Prof. Dr. Dr. Peters und Prof. Dr. Penzel für die Überlassung
des Themas. Danken möchte ich Dr. Lennart Knaack für die anfängliche und
Dr. Sebastian Canisius für die abschliessende Betreuung dieser Arbeit. Für
moralische Unterstützung möchte ich meiner Familie, Fr. Dr. Sabine Dustmann
sowie insbesondere meiner Frau Julia danken.
Darüber hinaus danke ich Herrn Dipl. Psych. Thomas Ploch für die
abschliessende Korrektur der Arbeit und seine guten Einfälle.

- 81 -
8.5. Akademische Lehrer
Meine akademischen Lehrer in Marburg waren die Damen und Herren:
Amon, Arnold, Aumüller, Austermann, Aziz, Back, Barth, Basler, Bauer, Baum,
Beato, Becker, Behr, Berendes, Berger, Berndt, Bernhardt, Bertalanffy,
Besedovsky, Beyer, Bien, Blankenburg, Braasch, Cetin, Czubayko, Daume,
Daut, Dibbets, Dittrich, Dombrowski, Doss, Egbring, Ehrhardt, Eilers, Engel,
Engenhardt-Cabillic, Eschenbach, Flores de Jacoby, Feuser, Friederich,
Fruhstorfer, Fuhrmann, Garten, Gemsa, Geus, Göke, Görg, Golenhofen,
Gotzen, Graul, Gressner, Grimm, Griss, Gröne, Grundner, Grzeschik,
Gudermann, Habermehl, Hamer, Happle, Hardewig, Hartmann, Hasilik,
Havemann, Hebebrand, Heeg, Heidenreich, Hellinger, Hemmer, Hennis, Hesse,
Hering, Herpertz-Dahlmann, Herzum, Heß, Heufelder, Hildebrandt, Hilgermann,
Hofmann, Hoffmann, Huffmann, Ihm, Jacob, Janke, Jones, Joseph, Kälble,
Kaffarnik, Karlson, Katschinski, Kern, Kleine, Kleinsasser, Klenk, Klötzer, Klose,
Knauff, Knoll, Koehler, Koolman, Koransky, Krause, Kretschmer, Krieg, Kroh,
Kroll, Kuhn, Kuni, Lang, Lange, Lauer, Lehmann, Legrum, Lennartz, Lill,
Lippert, Lorenz, Lotzmann, Ludwig, Lührmann, Lütcke, Maisch, Martini,
Mannheim, Massarrat, Mennel, Moll, Moosdorf, Mueller, Müller, Mutters, Netter,
Neubauer, Neurath, Niemeyer, Niessing, Oepen, Oertel, Peter, Petry, Pfeiffer,
Pieper, Pohlen, Portig, Radsak, Rehder, Remschmidt, Renz, Richter,
Riedmiller, Riße, Rodeck, Rosemann, Rosenow, Rothmund, Schachtschabel,
Schäfer, Schäfer, Schepelmann, Schiff, Schleyer, Schmid, Schmidt, Schmitz-
Moormann, Schnabel, Schneider, Schumacher, Schüffel, Schulz, Schwarz,
Seifart, Seitz, Seyberth, Slenczka, Sommer, Stachniss, Steiniger, Strempel,
Sturm, Tampé, Thomas, Vogelmeier, Voigt, Weber, Weihe, Werner,
Wesemann, von Wichert, Wiegandt, Wolf, Wulf, Ziegler, Zielke