Schema zur Analytik von synth. Peptiden · Schema zur Analytik von synth. Peptiden Synthese...
Transcript of Schema zur Analytik von synth. Peptiden · Schema zur Analytik von synth. Peptiden Synthese...

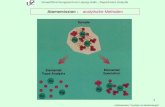
Schema zur Analytik von synth. PeptidenSynthese (manuel, automatisch, parallel)
Abspaltung (Fällung aus unpolarem Lösungsmittel)
Gefriertrocknung
HPLCMSMS/MSSequenzierung
Kopplung mitUV, MS
Aminosäurenanalyseggf. an chiraler Säule
Reinheit
Identität
SalzgehaltEntantiomerenreinheit
1

Chromatographie
Peptidsynthese in Lösung
2

Säulehydrophob: SiR3-O-C12H25
Pumpen
Laufmittel: Wasser, pH 2; Acetonitril
Probenaufgabesystem
Detektor
Octadecyl‐Phase C18
3

Wellenlänge [nm]
Peptid (enthält Tyrosin)
Peptid (mit Fmoc-Schutzgruppe)
Peptid (mit Mtr-Schutzgruppe)
UV-Spektren von Peptiden mit und ohne Schutzgruppen
220 240 260 280 300 4

HPLC eines Roh-Peptides
Cy3-NPYCy3-NPY
220 nm 552 nm
5

Dünnschicht-chromatographie(2-dimensional)
Detektion mit Ninhydrin-Sprühreagenz
Ionenaustausch-chromatographie
Derivatisierung mit Ninhydrin
Absorption l=570nm
A
t [h]
Derivatisierung
RP-HPLC/chiralerSäuleDetektion im UV,Fluoreszenz
A
t [min]
Aminosäurenanalyse
Peptid Totalhydrolyse (6N HCl, 24 h, 110 °C)Totalhydrolyse (6N HCl, 24 h, 110 °C)
Ninhydrin reagiert mit α‐Aminosäuren
Ruhemanns Violett 6

PITC=PhenylisothiocyanatPTC=PhenylthiocarbamoylATZ=AnilinothiazolinonPTH=Phenylthiohydantoin
Sequenzierung nach Edman
1. Schritt: Kupplung2. Schritt: Spaltung3. Schritt: Umwandlung
N-terminaler Sequenzierungszyklus
7

Phenylisothiocyanat
(Phenylthiocarbamoylpeptid)
1. Schritt: Kupplung
Sequenzierung nach Edman
8

ATZ-Aminosäure(Anilinothiazolinon)
um eine Aminosäureverkürztes Peptid
2. Schritt: Spaltung
Wird mit einem hydrophoben Lösungsmittel extrahiert
Sequenzierung nach Edman
(Phenylthiocarbamoylpeptid)
9

Phenylthiohydantoin-Aminosäure
3. Schritt: Umwandlung (Hydrolyse+ Umlagerung)
Phenylthiocarbamoyl-Aminosäure
Sequenzierung nach Edman
10

W
min
Analyse mittels HPLC
11

12

Massenspektrometrie
Essentielle Eigenschaften von allen MS Verfahren:• Erzeugung von Ionen in der Gas- oder Plasmaphase• Beschleunigung der Ionen in einem elektrischen Feld• Trennung der Ionen entsprechend der m/z Verhältnis
in einen Massenanalysator• Detektion der Ionen
13

Massenspektrometer
“soft"
14

MALD-Ionisierung
• Probe in lichtabsorbierender Matrix• Laserbestrahlung• thermische, photochemische Anregung Ionisierung
Matrixassistierte LaserdesorptionIonisations(MALDI)-Massenspektrometrie
Koichi Tanaka
Nobel Price in Chemistry 20021/4 share
15

Matrix
2,5-dihydroxybenzoesäure(DHBA)MW 154.12
-Cyano-4-hydroxyzimtsäure (CHCA) MW 189.17
Sinapinsäure (SA)3,5-Dimethoxy-4-hydroxzimtsäureMW 224.21
266 nm337 nm355 nm
337 nm355 nm
266 nm337 nm355 nm
Peptide,Proteine
Peptide
Proteine
16

Massenanalysator
Matrixkristallmit Analyten
LaserN2 337 nm 3-5 nsNd:YAG 355 nm 5-15 nsEr:YAG 2.94 μm 90 ns
MALD-Ionisierung
pulsed
17

MALDI-TOF-Massenspektrometrie
Laser
Probein
Matrix
TOF = T1-T0
Linsensystem
T0
Ionen
Laser
Probein
TOF = T -T0
Detektor
Linsensystem
T0
T1
Ionen
(TOF = Time Of Flight)
18

Vacuum
MALDI/TOF-Massenspektrometrie
19

MALDI-TOF-Massenspektrometrie
++
Probe + Matrix Ionen mit gleicher Masseverschiedener Geschwindigkeit
Problem: Peaks sind inhärent breit in MALDI-TOF Spektra (niedrige Massenauflösung)
Ungleiche Energieverteilung bei der Ionisierung +
20

MALDI-TOF-MassenspektrometrieMethoden zur Kompensation der initialen Geschwindigkeits‐verteilung der Ionen:• Verzögerte Ionenextration (delayed extraction)
Das elektrische Feld wird zeitversetzt zum Laser Desorptionsimpuls eingeschaltet.
• Ionenspiegeln (Reflektoren)Elektrisches Gegenfeld angeschlossen an die Driftstrecke
SchärferePeaks
21

Kein elektrisches Feld, Ionen streuen.
++ +
Ionen mit gleicher Masse, unterschiedlicher Geschwindigkeit
Feld angelegt, langsame Ionen beschleunigen mehr als die Schnelleren
0 V.
0 V.
++ +
Langsame Ionen erreichen die Schnellen
20 kV.
20 kV.
0 V.
0 V.+++
MALDI-TOF-Massenspektrometrie
Delayed extraction
1.
2.
3.
22

MALDI-TOF-Massenspektrometrie
Reflektor
23

TOF: Time-of-flight
• Trennung der Ionen aufgrund unterschiedlicher Flugzeit bei vorgegebenem Wegt = f ( 2m/z )
• Reflektor und Delayed Extraction (DE): erhöhen Genauigkeit und Empfindlichkeit
24

MALDI-TOF von Angiotensin: M+H+theor. 1046.54
25

MALDI-TOF von recombinant SERPINA12 / Vaspin
26

Elektrospray-Ionisierung
Spray Elektrospray
27

Elektrospray-Ionisierung
28

Elektrospray-Ionisierung
Verdampfungdes Lösungsmittels
29

Elektrospray-Ionisierung
• protonenhaltige Lösung der Probe• Zerstäubung im Hochspannungsfeld• Lösungsmittel verdunstet• Zerfall der Molekülcluster in vielfachgeladene Ionen:[M+nH]n+ oder [M‐nH]n‐
John B. Fenn
Nobel Price in Chemistry 20021/4 share
30

Interface zwischen ESI-Quelle und Quadrupole
Atmosphärendruck Hochvakuum
Vorvakuum
31

Quadrupol-Filter
-
-
+
+
-
-+
+
32

Quadrupol-Filter
33

Quadrupol-Detektion
• Massentrennung durch Schwingung der Ionen in einem hochfrequenten elektrischen Feld(Kombination von Radiofrequenzspannung V und Gleichspannung U)
• V/U konstant nur ein m/z‐Ion stabil• Veränderung der Amplitude Spektrum
34

ESI-MS von Neurotensin 1673,5
35

36

MALDI gegen ESI
MALDI ESIAnalyte in matrix Analyte in solutionSample bombardment with laser to desolvate ions
Dissolved charged sample desolvated, “cold ions”
Ionization takes place through the matrix
Ions are brought to the gas phase
Ionization in vacuum Spray in atmospheric pressureGenerates ion pulses Generates a continuous current
Historically coupled to:TOF analyzer Quadrupole analyzer
37

ESI-MS-MS: Tandem-Massenspektrometrie
Sequenzierung mittels Massenspektrometrie
38

Fragmentierung der Peptidbindung
39

40

Sequenzierung von Peptiden mit MS
41

200 400 600 800 1000 1200 14000
1
2
3
4
5
6
7
8
9
10
11
Abs. Int. * 1000a H M K*b H M K*y R P S F S P K* M H
110.050a 1
138.060b 1
175.075y 1
H241.060
a 2
269.054b 2
272.117y 2
595.190a 3
623.188b 3
359.112y 3
K*
506.189y 4
P
593.178y 5
926.408a 6
690.248y 6
F
1044.330y 7
1175.506y 8
1312.655y 9
R
KPy7b4
PSy6b5
SFy5b6
KPSy7b5
PSF y6b6
PSFSPy6b8
42

m /z750 1000 1250 1500 1750 2000 2250 2500 2750 3000 3250 3500 3750
5
10
15
20
25
30
35
40
45
50
Abs. Int . * 1000
1115.60243-50
1129.658295-301
1217.607356-363
1219.688280-285
1306.66951-61
1312.657216-224
1335.719346-355
1687.99859-70
1690.87129-40
1938.011349-363 1975.054
29-42
1989.058331-345
2002.25047-61
2159.12929-42
2350.269216-232
2392.279216-232
2533.375321-340
2979.637322-345
3149.689150-175
43

Schema zur Analytik von PeptidenSynthese (manuel, automatisch, parallel)
Abspaltung (Fällung aus Lösungsmittel)
Gefriertrocknung
HPLCMSMS/MSSequenzierung
Kopplung mitUV, MS
Aminosäurenanalyseggf. an chiraler Säule
Reinheit
Identität
SalzgehaltEntantiomerenreinheit
44