Seminar zum Quantitativen Anorganischen Praktikum WS · PDF file5,4g = M(NH ) m(NH ) n(NH ) =...
Transcript of Seminar zum Quantitativen Anorganischen Praktikum WS · PDF file5,4g = M(NH ) m(NH ) n(NH ) =...
Universitt zu Kln
Seminar zumQuantitativen Anorganischen Praktikum
WS 2011/12
Teil des Moduls MN-C-AlC
Dr. Matthias BrhmannDr. Christian Rustige
Universitt zu Kln
InhaltMontag, 09.01.2012, 8-10 Uhr, HS III
Allgemeine Einfhrung in die Quantitative Analyse Zusatzausrstung / Glasgerte Gravimetrie: A5/A6
Freitag, 13.01.2012, 8-9 Uhr, HS III Physikalische Methoden: A7
Montag, 16.01.2012, 8-10 Uhr, HS III A4 (Photometer) / A2 (pH-Meter) Volumetrie: A10
Freitag, 20.01.2012, 8-9 Uhr, HS III Volumetrie: A11/A12/A13 A3 (Kationenaustauscher)
Universitt zu Kln
Praktikum: Aufgabe 11Komplexometrische (chelatometrische) Bestimmung von Zink
Vor dem Versuch
Ansetzen einer 0,05 M EDTA-Malsung (Aufgabe 8 (II))
Ansetzen einer NH4Cl / NH3-Pufferlsung pH10
Versuchsdurchfhrung
Entnahme von 25 mL der auf 100 mL aufgefllten Probe
Komplexbildungstitration der gepufferten Analyse mit EDTA-Malsung
Jeweils eine Erio-T-Puffertablette zur Endpunktsindikation hinzugeben
Dreimalige Versuchsdurchfhrung
Universitt zu Kln
Praktikum: Aufgabe 8 (II)Ansetzen der 0,05 M EDTA-Malsung
Urtitersubstanz
Achtung: EDTA-Gehalt laut Chemikalienbehlter beachten
meist Na2H2C10H12O8N2 2 H2O
Handelsnamen: Komplexon III, Titriplex III, Idranal III
Bestimmung des Titers t:
)Auswaage(m)Auswaage(m
=tsoll
ist
Ethylendiamintetraacetat
4 H+
4 -
Universitt zu Kln
Praktikum: Aufgabe 11Ansetzen einer Pufferlsung (Ammoniakpuffer: NH4Cl / NH3) pH 10
Pufferlsungen sind Lsungen, die auch bei Zugabe erheblicher Mengen Sure oder Base ihren pH-Wert nur wenig ndern.
Henderson-Hasselbalch Gleichung)A(c)HA(c
lg)HA(pK=pH S
5,4 g ! NH4Cl in 20 ml H2O lsen, 35 ml konz. NH3 (25%ig) zugeben und auf 100 ml verdnnen.
mol1,0g4912,53
g4,5=
)NH(M)NH(m
=)NH(n +4
+4+
4 mol46,0g03056,17g9,7
)NH(M)NH(m
=)NH(n3
33
10L/mol6,4
L/mol1lg25,9=
)NH(c)NH(c
lg)NH(pK=pH3
+4+
4S
Universitt zu Kln
Praktikum: Aufgabe 11Der Indikator Eriochromschwarz T
H2X- pH < 6HX2- pH = 7-11X3- pH > 12 Metall-Indikator-Komplex: weinrote Lsung
Universitt zu Kln
Praktikum: Aufgabe 11Komplexbildungstitrationen
Hauptreaktion: Zn2+ + EDTA Zn2+-EDTA-Komplex (starker Komplex, farblos)
Indikatorreaktion: Zn2+-Erio-T-Komplex + EDTA Zn2+-EDTA-Komplex + Erio-T
(weinrot) (grnlich)
Prinzip: Der strkere Ligand (EDTA) verdrngt den schwcheren (Erio-T) aus dem Komplex.
Universitt zu Kln
Praktikum: Aufgabe 11Auswertung
a) Verbrauchsmittelwert berechnen
Stark abweichende Werte mglicherweise fehlerhaft
b) Angabe der gesamten Masse von Zn2+ in der Probe
tVc=)gesucht(n Verbrauchsoll
Berechnung der Stoffmenge ber Volumenverbrauch
Umrechnung der Stoffmenge in (Gesamt)-Masse
4Mn=mUmrechnungsfaktor gesamte Analyse!
Universitt zu Kln
Praktikum: Aufgabe 12Manganometrische Bestimmung von Eisen nach Reinhardt-Zimmermann
Vor dem Versuch Ansetzen einer 0,1 N KMnO4-Malsung (Aufgabe 9 (I))
Aufbewahrung in brauner Flasche
Versuchsdurchfhrung
Lsen des erhaltenen Feststoffes in einem 100 ml-Mekolben
Entnahme von 25 mL der auf 100 mL aufgefllten Probe
Redoxtitration der Analyse mit KMnO4-MalsungJeweils 2 ml verdnnte Salzsure und
10 ml Reinhardt-Zimmermann-Lsung (steht aus) zugeben
Dreimalige Versuchsdurchfhrung
Universitt zu Kln
Praktikum: Aufgabe 9 (I)Ansetzen der 0,1 N KMnO4-Malsung
0,1 N KMnO4 = 0,02 M KMnO4 (im Sauren Redoxqivalent: 1/5 KMnO4) Spuren von Staubteilchen und anderen organischen Verunreinigungen fhren zur Bildung
von Braunstein (MnO2) Abkochen und Filtrieren ber Glasfiltertiegel keine Urtitersubstanz indirektes Verfahren
Reaktion im Sauren: 2 MnO4- + 5 C2O4 2- + 16 H+ 2 Mn2+ + 10 CO2 + 8 H2O
Na2C2O4 im Trockenschrank (ca. 220C) trocknen Getrocknetes Na2C2O4 auf Analysenwaage abwiegen Probe ansuern (je 5 ml verd. H2SO4) In der Hitze (ca. 80C) titrieren Endpunkt: Rosafrbung durch MnO4- bleibt kurzzeitig bestehen
Einstellen der Malsung durch Titration von Natriumoxalat
Universitt zu Kln
Praktikum: Aufgabe 12Redoxtitration
Redoxreaktion: 5 Fe2+ + MnO4- + 8 H+ 5 Fe3+ + Mn2+ + 4 H2O
Am quivalenzpunkt gilt: n (Fe2+) = 5 n (MnO4-)
Hinweise Die gelste Probe muss sehr bald titriert werden.
Fe2+-Ionen werden in wssriger Lsung schnell oxidiert.
Zugabe von Reinhardt-Zimmermann-Lsung verhindert die Oxidation von Chlorid-Ionen (Ansuern mit verd. HCl) und erleichtert die Endpunkterkennung.
Endpunkt: Die Rosafrbung durch berschssiges MnO4- bleibt kurzzeitig bestehen.
Universitt zu Kln
Praktikum: Aufgabe 12Auswertung
Redoxreaktion: 5 Fe2+ + MnO4- + 8 H+ 5 Fe3+ + Mn2+ + 4 H2O
Am quivalenzpunkt gilt: n (Fe2+) = 5 n (MnO4-)
Berechnung der Stoffmenge ber Volumenverbrauch
Umrechnung der Stoffmenge in (Gesamt)-Masse
4Mn=mUmrechnungsfaktor gesamte Analyse!
tVL/mol02,05=)gesucht(n Verbrauchs. Stchiometrie quivalenzpunktNormalitt (0,1 N)
Universitt zu Kln
Praktikum: Aufgabe 13Iodometrische Bestimmung von Kupfer
Vor dem Versuch Ansetzen einer 0,1 N Na2S2O3-Malsung (Aufgabe 9 (II))
erst nach 1-2 Wochen titerbestndig
Ansetzen einer Strkelsung
Versuchsdurchfhrung
Entnahme von 25 mL der auf 100 mL aufgefllten Probe
Redoxtitration der Analyse mit Na2S2O3-MalsungJeweils 1 ml verdnnte Schwefelsure und 3 g Kaliumiodid zugebenZugabe von 2-3 ml Strkelsung kurz vor dem Endpunkt zu dessen Indikation.
Dreimalige Versuchsdurchfhrung
Universitt zu Kln
Praktikum: Aufgabe 9 (II)Ansetzen der 0,1 N (bzw. 0,1 M) Na2S2O3-Malsung
Thiosulfatlsungen knnen durch Zugabe von wenig Na2CO3 haltbar gemacht werden, sind jedoch erst nach etwa 1-2 Wochen titerbestndig.
keine Urtitersubstanz indirektes Verfahren
IO3- + 5 I- + 6 H+ 3 I2 + 3 H2O 6 S2O32- + 3 I2 3 S4O62- + 6 I-
Titerbestimmung erst am Tag der iodometrischen Titration von Kupfer (Aufgabe 13)! ca. 250 mg KIO3 (notieren!) auf 100 ml auffllen und hiervon drei Proben a 25 ml entnehmen Die auf ca.100 ml verdnnten Proben mit verd. H2SO4 ansuern und ca. 3 g KI (Laborwaage)
beifgen Zur Endpunktserkennung 2-3 ml Strkelsung hinzugeben
,,Indirektes Einstellen der Malsung durch Titration von Kaliumiodat-Lsung
Universitt zu Kln
Praktikum: Aufgabe 13Ansetzen einer Strkelsung
Ca. 0,5 g lsliche Strke werden mit wenig kaltem Wasser in einer Reibschale solange verrieben, bis ein ,,Brei gleichmiger Konsistenz entsteht. Diesen ,,Brei gibt man zu ca. 100 ml siedendem Wasser und kocht einige Minuten weiter. Nach Abkhlen dekantiert oder filtriert man die klare Lsung ab.
Iodlsungen aus Iod und Kaliumiodid: komplexes Triiodidion I3- (tiefbraun) auch bei starker Verdnnung noch gelb gefrbt
Zusatz von Strkelsung als Indikator (Amylose) Iod-Strke Reaktion (tiefblaue Einschlussverbindung) Iodkonzentrationen von 10-5 mol/L erkennbar
Universitt zu Kln
Praktikum: Aufgabe 13Redoxtitration
Hinweise Ein groer berschuss an KI (ca. 3 g) ist notwendig um eine vollstndige Umsetzung zu
CuI und I2 zu gewhrleisten. Zur Endpunktserkennung 2-3 ml Strkelsung hinzugeben.
Der Endpunkt ist erreicht, wenn die blaue Frbung des Iod-Strke-Komplexes vollstndig verschwunden ist.
Achtung: Beim lngeren Stehenlassen frbt sich die Lsung infolge einer Oxidation durch Luftsauerstoff wieder blau.
Redoxreaktionen: 2 Cu2+ + 4 I- 2 CuI + I2 n (Cu2+) = n (I2)
I2 + 2 S2O32- 2 I- + S4O62- n (S2O32-) = n (I2)
Am quivalenzpunkt gilt: n (Cu2+) = n (S2O32-)
Universitt zu Kln
Praktikum: Aufgabe 13Auswertung
a) Verbrauchsmittelwert berechnen
Stark abweichende Werte mglicherweise fehlerhaft
b) Angabe der gesamten Masse von Cu2+ in der Probe
tVc=)gesucht(n Verbrauchsoll
Berechnung der Stoffmenge ber Volumenverbrauch
Umrechnung der Stoffmenge in (Gesamt)-Masse
4Mn=mUmrechnungsfaktor gesamte Analyse!
Am P: n (Cu2+) = n (S2O32-)
Universitt zu Kln
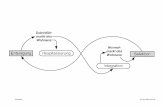
IonenaustauscherBestimmung nach Ionenaustausch
Kationen werden mit Hilfe eines Kationenaustauschers
gegen H3O+-Ionen ausgetauscht, welche anschlieend
mit NaOH titriert werden.
Anionen werden mit Hilfe eines Anionenaustauschers
gegen OH--Ionen ausgetauscht, welche anschlieend mit
H2SO4 titriert werden.
R(SO3-)n(H+)n + nM+ R(SO3-)n(M+)n + nH+
R(NR3+)n(OH-)n + nA- R(NR3+)n(A-)n + nOH-
Universitt zu Kln
IonenaustauscherBeispiel eines Kationenaustauschers (H+-Form)
Polymeres Harzgerst
Endstndige anionische Gruppen
Kationen ionogen gebunden
sonst kein Austausch mglich
Universitt zu Kln
IonenaustauscherBeispiel eines Anionenaustauschers (Cl--Form)
Polymeres Harzgerst
Endstndige kationische Gruppen
Anionen ionogen gebunden
sonst kein Austausch mglich
Cl Cl
CH2N
+
CH3
CH3CH3
CH2N
+
CH3
CH3
CH3
CH
CH2
CH2
CH
CH2
CH
CH2
CH
CH2 CH2
CH CH CH2
CH2