Therapie postoperativer Darmpassagestörungen in der ... · Dieses Dokument wurde zum persönlichen...
Transcript of Therapie postoperativer Darmpassagestörungen in der ... · Dieses Dokument wurde zum persönlichen...

Therapie postoperativerDarmpassagestörungenin der Intensivmedizin
Theresa MeißnerChristoph Reißfelder
Intensivmedizin up2date
1 · 2018
Operative Intensivmedizin 4
VNR: 2760512018154651749
DOI: 10.1055/s-0043-120030
Intensivmedizin up2date 2018; 14 (1): 87–102
ISSN 1614-4856
© 2018 Georg Thieme Verlag KG
Die
ses
Dok
umen
t wur
de z
um p
ersö
nlic
hen
Geb
rauc
h he
runt
erge
lade
n. V
ervi
elfä
ltigu
ng n
ur m
it Z
ustim
mun
g de
s V
erla
ges.

Unter dieser Rubrik sind bereits erschienen:
Intensivbehandlung des polytraumatisierten PatientenC. Waydhas, U. Hamsen Heft 4/2017
Patient Blood Management in der IntensivmedizinP. Meybohm, S. Choorapoikayil, K. Zacharowski Heft 3/2017
Operative Interventionen auf der Intensivstation U. Klaiber,C. Philipsenburg, L. Schneider, T. Brenner Heft 2/2017
Prävention der unbeabsichtigten perioperativen HypothermieA. Bräuer, S. Scheithauer Heft 1/2017
Das akute Abdomen auf der Intensivstation L. Fischer, M. Apitz,A. Billeter, S. Hofer Heft 4/2016
Endovaskuläre Aortenchirurgie – besondere Herausforderungfür die perioperative Intensivmedizin D. Dovzhanskiy,M. Bischoff, K. Meisenbacher, D. Böckler Heft 2/2016
Postoperatives Management nach Pankreasresektion J. Kaiser,M. Mieth, T. Hackert Heft 1/2016
Update: Immunsuppression bei OrgantransplantationenG. Polychronidis, P. Houben, M. Mieth, C. Morath, D. Gotthardt,P. Schemmer Heft 3/2015
Spezielle Aspekte der intensivmedizinischen Therapie nachherzchirurgischen Eingriffen C. Kerscher, S. Wittmann,S. Schopka, D. Lunz, Y. Zausig Heft 1/2014
Perioperativer Myokardinfarkt O. Spelten, V. RudolphHeft 1/2014
Drainagemanagement in der Viszeralchirurgie E. Wurster,P. Knebel, M. Diener Heft 4/2013
Abdominelles Kompartmentsyndrom K. Ukegjini, M. Adamina,M. Zadnikar, I. Tarantino Heft 2/2013
Schädel-Hirn-Trauma beim Erwachsenen H. Stubbe, J. WölferHeft 4/2012
Frühmobilisierung des chirurgischen IntensivpatientenS. Weiterer, A. Hecker, G. Szalay, M. Heinrich, K. Mayer,M. Weigand Heft 3/2012
Darmpassagestörungen in der Intensivtherapie J. Kirchberg,C. Reißfelder, M. Mieth, M. Büchler Heft 3/2012
Anastomoseinsuffizienz im Gastrointestinaltrakt T. Welsch,M. Büchler Heft 3/2011
Perioperative Therapie bei abdominothorakaler Ösophagus-resektion K. Ott, S. Hofer, R. Haken, M. Büchler Heft 3/2010
Fast-Track-Chirurgie P. Knebel, A. Schellhaaß, A. Walther,C. Seiler Heft 2/2010
Haut- und Weichgewebsinfektionen auf der IntensivstationP. Kujath, C. Eckmann Heft 1/2010
Ogilvie-Syndrom – akute idiopathische KolondilatationJ. Kirchberg, K. Ott, M. Büchler Heft 1/2010
Transfusionsstrategien: Leitliniengerechte Diagnostikund Therapie R. Pschowski, J. Schefold, A. Walther, S. HoferHeft 4/2009
Chirurgie im hohen Lebensalter V. Schumpelick, K. Junge,C. Krones Heft 1/2009
Mechanische Assist-Systeme zur Herzunterstützung S. Klotz,H. Scheld Heft 2/2008
Infektionen unter medikamentöser Immunsuppression beitransplantierten Intensivpatienten C. Lichtenstern, J. Schmidt,J. Encke, M. Weigand Heft 1/2008
Gastrointestinale Auswirkungen des (septischen) SchocksH.P. Knaebel, M. Büchler Heft 4/2007
Medikamentöse Immunsuppression nach Organtrans-plantation C. Lichtenstern, J. Schmidt, J. Encke, M. WeigandHeft 3/2007
Probleme nach Lebertransplantation B. Schmied, P. Sauer,S. Müller Heft 3/2007
Intensivbehandlung des Schädel-Hirn-Traumas K. Zweck-berger, O. Sakowitz, K. Kiening, A. Unterberg Heft 2/2007
JETZT FREISCHALTEN
Sie haben Ihre Zeitschrift noch nicht
freigeschaltet? Ein Klick genügt:
www.thieme.de/eref-registrierung
ALLES ONLINE LESEN
Mit der eRef lesen Sie Ihre Zeitschrift:
online wie offline, am PC und mobil, alle bereits
erschienenen Artikel. Für Abonnenten kostenlos!
https://eref.thieme.de/intensiv-u2d
CME-Fortbildung
Die
ses
Dok
umen
t wur
de z
um p
ersö
nlic
hen
Geb
rauc
h he
runt
erge
lade
n. V
ervi
elfä
ltigu
ng n
ur m
it Z
ustim
mun
g de
s V
erla
ges.

Therapie postoperativer Darmpassage-störungen in der Intensivmedizin
Theresa Meißner, Christoph Reißfelder
FA
Sie
ph
Fra
ass
alt
No
for
gew
Fra
sta
tio
deu
Dra
So
unw
gan
rich
ist
rein
„De
CME-Fortbildung
Meißner
ustim
mun
g de
s V
erla
ges.
Der postoperative Ileus (POI) ist eine physiologische Reaktion des Magen-Darm-Traktes, welche vor allem nach offenen abdominal-chirurgischen Eingriffenbeobachtet wird. Das häufige Krankheitsbild belastet nicht nur den individuellenPatienten, sondern auch das Gesundheitssystem über längere Krankenhaus-verweildauer und konsekutiv höhere Behandlungskosten. Der vorliegende Artikelfasst die aktuelle Datenlage zur Therapie des POI zusammen.
LLBEISPIEL
beginnen die allmorgendliche Visite auf der peri-
eren Station.
u G. war vor 4 Tagen notfallmäßig laparoskopisch
istiert das Sigma reseziert worden. Sie ist 85 Jahre
und wurde heute von der Intensivstation auf die
rmalstation zurückverlegt. Sie war nach einer Per-
ation mit ausgedehnter Peritonitis initial septisch
esen. Prinzipiell würden Sie die Entlassung für
u G. für Ende der Woche planen. Sie hatte sich er-
unlich schnell erholt. Der Eingriff verlief komplika-
nslos, die postoperativen Entzündungswerte sind
tlich rückläufig, und heute werden Sie die übrigen
inagen ziehen.
gerne Frau G. wieder nach Hausemöchte, so
ohl fühlt sie sich aber auch, denn „Mit dem Stuhl-
g hat es leider immer noch nicht geklappt. So
tig was zu essen vertragʼ ich auch noch nicht, mir
so übel. Aber Winde, Frau Doktor, grad bevor Sie
kamen, da ist ein bisschen was abgegangen.“
finitiv!“, kommentiert ihre Bettnachbarin Frau S.
DEFINITION
Postoperativer Ileus (POI)
Ein POI wird als eine vorübergehende Inhibierung
der gastrointestinalen Motilität nach chirurgischer
Intervention aufgrund nicht mechanischer Ursachen,
welche eine ausreichende orale Nahrungsaufnahme
verhindern, betrachtet [2].
Die
ses
Dok
umen
t wur
de z
um p
ersö
nlic
hen
Geb
rauc
h he
runt
erge
lade
n. V
ervi
elfä
ltigu
ng n
ur m
it Z
BegriffsbestimmungLange Zeit stand eine einheitliche Definition des klinischhäufig beobachteten Krankheitsbildes aus. Es handeltsich um eine multifaktoriell bedingte Paralyse der gas-trointestinalen Motilität, welche als physiologische Reak-tion des Magen-Darm-Traktes auf einen Eingriff, gehäuftvor allem nach offenen abdominalchirurgischen Opera-tionen, beobachtet wird. Bei länger ausbleibender Darm-passage spricht man von einem prolongierten POI. Die
T, Reißfelder C. Therapie postoperativer Darmpassagestörungen… Intensivmed
Definition des pathologischen POI variiert zwischen dem3. und 7. postoperativem Tag mit fehlender Passage [1].
Eine Leitlinie zum diagnostischen und therapeutischenVorgehen fehlt ebenfalls. 2016 wurde von Gero et al. mit-hilfe eines webbasierten Delphi-Prozesses ein internatio-naler Konsens gefunden [2]. Aus diesem Gremium gehtdie erste einheitliche Definition des POI hervor, die sichnicht auf einen bestimmten Zeitraum des Auftretensfestlegt.
KlassifikationUnterschieden wird der primäre POI ohne andere aus-lösende Ursache vom sekundären POI auf dem Bodeneiner anderen Komplikation wie z. B. Sepsis oder Anasto-moseninsuffizienz [3,4].
Ein wiederkehrender POI tritt nach der klinischen Auf-lösung eines ersten, direkt postoperativen POI-Ereignis-ses auf.
Der prolongierte Ileus hält > 3 Tage nach einem laparo-skopischen Eingriff und > 5 Tage nach einem offenen Ein-griff an.
87izin up2date 2018; 14: 87–102

▶ Tab. 1 Die 3 Subtypen des postoperativen Ileus (POI).
Einteilung Lokalisation Symptome, Befunde
Typ I gesamter GI-Takt betroffen Übelkeit
Erbrechen
fehlender Abgang vonWinden und Stuhl
Typ II oberer GI-Trakt ammeisten betroffen Übelkeit und Erbrechen
Stuhl undWinde gehen ab
Typ III untere GI-Trakt ammeisten betroffen fehlender Abgang vonWinden und Stuhl
die orale Nahrungsaufnahme wird allerdings toleriert
88
CME-Fortbildung
stim
mun
g de
s V
erla
ges.
Außerdem kann man anhand der am stärksten betroffe-nen anatomischen Region zwischen 3 Subtypen des POIunterscheiden (▶ Tab. 1) [5].
heru
nter
gela
den.
Ver
viel
fälti
gung
nur
mit
Zu
InzidenzDie Inzidenz des POI liegt bei 10–30%, die des prolongier-ten POI ebenfalls [6–8]. Nach größeren Eingriffen wiez.B. der offenen Kolektomie ist ein POI häufiger zu beob-achten.
MerkeNicht nur abdominalchirurgische Eingriffe führen zueinem POI. Die Inzidenz nach kardialen oder ortho-pädischen Eingriffen, insbesondere bei Wirbelsäulen-operationen, wurde mit 10% angegeben [9].
Die
ses
Dok
umen
t wur
de z
um p
ersö
nlic
hen
Geb
rauc
h
Ätiologie, PathophysiologieDie Aktivität des Magen-Darm-Traktes wird maßgeblichneurogen reguliert. Beim Gesunden regen kalorienreicheMahlzeiten, das morgendliche Erwachen und elektrischeStimulation die antegrade Peristaltik im Kolon und dieDefäkation an. Beim POI kommt es mutmaßlich zu einerAbschwächung oder sogar einem Ausfall dieser neurogenvermittelten Aktivität [1].
Die Entstehung eines POI ist multifaktoriell bedingt, wo-bei nicht alle Teilaspekte der Pathophysiologie hinrei-chend erforscht sind.
MerkeImmunologische und entzündliche Prozesse werdennach operativen Eingriffen genauso beschrieben wieeine Dysregulation des autonomen Nervensystems,rezeptorgesteuerte Prozesse und Elektrolytstörun-gen.
Aus den in den nächsten Abschnitten erläuterten multi-faktoriellen Ursachen ergeben sich in der Folge auch dieunterschiedlichen Therapieansätze des POI.
Meißner T, Reißfelder C. Therapie posto
Entzündungsreaktion
Durch die Verletzung des Peritoneums und die nachfol-gende Manipulation am Darm wird eine Entzündungskas-kade ausgelöst, an der vor allem Histamine, Prostaglan-dine, Interleukine und Mastzellaktivierung im Peritoneumund der Muscularis propria beteiligt sind. Viele der Ent-zündungsmediatoren wirken relaxierend auf die glatteMuskulatur.
Bei Manipulation des Darms wird ab der 3. Stunde einerLaparotomie über die Aktivierung von dendritischen Zel-len und deren Ausschüttung von Interleukin 12 ebenfallseine Entzündungsreaktion getriggert. IL12 bindet an T1-Helferzellen, die auch in nicht affektierte Regionen desAbdomens wandern und dort per Sekretion von TNF-αund die darüber gesteuerte Aktivierung von Makropha-gen eine vom eigentlichen Ort der Intervention entfernteEntzündungsreaktion auslösen. Dieser Effekt erklärt auchdie Wirkung von liegenden Drainagen, die eine lokaleEntzündungsreaktion auslösen, auf das verzögerte Wie-dereinsetzen der Darmpassage [10,11].
Wasser- und Elektrolythaushalt
Die erhöhte Permeabilität der Darmwand aufgrund derlokalen Entzündungsreaktion führt zu einem Ödem der-selben, das wiederum ein mechanisches Hindernis füreine effiziente Muskelkontraktion darstellt. Ein unaus-geglichener Wasser- und Elektrolythaushalt – insbeson-dere die perioperative Überladung mit Flüssigkeit – führtzusätzlich zu einem Ödem der Darmwand.
Elektrolytstörungen wie Hypokaliämie, Hyponatriämieund Hypokalziämie werden mit einem POI und ihr Aus-gleich mit einer Wiederherstellung der normalen Darm-funktion assoziiert. Allerdings sind alle Studien darüberretrospektiv, was eine Kausalitätszuschreibung er-schwert. Es ist ebenso gut möglich und wahrscheinlich,dass es durch die Flüssigkeitsverschiebungen im Rahmendes POI erst konsekutiv zu einer Elektrolytverschiebungkommt, welche den Zustand aggraviert und prolongiert.
perativer Darmpassagestörungen… Intensivmedizin up2date 2018; 14: 87–102

ÜBERSICHT
Risikofaktoren für die Entstehung eines POI
Beeinflussbare Risikofaktoren
▪ perioperativer Opioidgebrauch
▪ perioperativer Blutverlust
▪ offene Eingriffe
▪ lange OP-Zeiten
▪ ausgedehnte Manipulation am Darm
▪ präoperativ niedrige Albuminwerte
▪ Rauchen
▪ Übergewicht
▪ präoperative orale Antibiotikagabe
▪ präoperative Darmvorbereitung
▪ präoperative Chemotherapie
Nicht beeinflussbare Risikofaktoren
▪ höheres Alter
▪männliches Geschlecht
▪ abdominelle Voroperationen
▪ Stoma- oder Anastomosenanlage
▪ Notfalleingriff
▪ asiatisch-kaukasische Volkszugehörigkeit
▪ vorbestehende Komorbiditäten, insbesondere:
– respiratorische und Gefäßerkrankungen
– Morbus Crohn oder Volvulus
– präoperativer Aszites
– präoperative Sepsis
Die
ses
Dok
umen
t wur
de z
um p
ersö
nlic
hen
Geb
rauc
h he
runt
erge
lade
n. V
ervi
elfä
ltigu
ng n
ur m
it Z
ustim
mun
g de
s V
erla
ges.
Blutversorgung
Es wird vermutet, dass eine relative Darmischämie eineRolle beim Ileus spielt. Diese wird einerseits durch dieEntzündungsreaktion befördert, andererseits durch einedirekte Reduktion des Blutflusses während der Interven-tion. Durch einen ggf. allgemeinen Blutverlust im Rah-men größerer oder notfallmäßiger Eingriffe wird diesesProblem zusätzlich verstärkt.
Neurogene MechanismenAutonomes Nervensystem
Während und nach einem chirurgischen Eingriff über-wiegt die Aktivität des sympathischen Nervensystems.Somatischer Schmerz, welcher z. B. durch die Verletzungder Bauchwand entsteht, wird über spinale Afferenzenund eine direkt über das Seitenhorn laufende autonom-sympathische Efferenz verarbeitet. Diese führen übereine Inhibierung der Acetylcholinfreisetzung und eine ge-steigerte Freisetzung von NO zur verminderten Aktivitätder Myozyten. Zusätzlich wird die Lokalisation und Pro-jektion des Schmerzes über spinothalame Bahnen gelei-tet.
Enterisches Nervensystem
Viszeraler Schmerz wird hauptsächlich über das enteri-sche Nervensystem und die subdiaphragmal gelegenenafferenten Anteile des N. vagus transportiert. Es erfolgtdie direkte Weiterleitung in den Hirnstamm zum Nucleustractus solitarius. Eine nicht adrenerge, nicht cholinerge,vagal vermittelte Efferenz blockiert die gastrointestinaleMotilität über die direkte Freisetzung von NO und vaso-aktivem intestinalem Peptid (VIP).
Durch die Resektion von Hohlorgananteilen kommt es zueiner Unterbrechung des intramuralen enterischen Ner-vensystems und des Geflechtes aus interstitiellen Cajal-Zellen, welche die Kontraktilität der Myozyten beeinflus-sen. Zwar kommt es hier im Laufe des Heilungsprozesseszu einer Regeneration, direkt postoperativ liegt aber anjeder Anastomose eine physikalische Barriere der elektro-mechanischen Kopplung vor.
Hormonelle Mechanismen
Sowohl die chirurgisch herbeigeführte Verletzung alsauch die perioperativ ausbleibende orale Nahrungsauf-nahme führen zu einer Dysregulation des gastrointestina-len Hormon- und Neuropeptidhaushaltes. Die genauenMechanismen und Wirkungsweisen von z.B. VIP, Sub-stanz P und Motilin und ihre Bedeutung für den POI sindallerdings noch Gegenstand der Forschung.
Einfluss einer perioperativen Opioidtherapie
Durch den chirurgischen Stress werden endogene Opio-ide ausgeschüttet, gleichzeitig werden zur Schmerzthe-rapie exogene Opioide zugeführt. Im zentralen Nerven-system wirken diese schmerzdämpfend. Peripher wirkensie als Agonisten des peripheren µ-Rezeptors im Plexus
Meißner T, Reißfelder C. Therapie postoperativer Darmpassagestörungen… Intensivmed
myentericus. Dies führt zu einer Blockade der Acetylcho-linausschüttung und damit einer verminderten Kontrak-tilität der glatten Muskulatur.
Erholung der Magen-Darm-FunktionDiese oben beschriebene physiologische Stressreaktiondes Körpers führt zu einer Darmparalyse, von der sichdie verschiedenen Teile des Gastrointestinaltrakts unter-schiedlich schnell erholen.
MerkeDie Peristaltik des Dünndarms kommt nach meist< 24 Stunden als erstes wieder in Gang. Darauf folgtder Magen mit 24–48 Stunden und zuletzt, nach über48 Stunden, der Dickdarm [1].
Aus dieser asynchron wieder einsetzenden Aktivität desGastrointestinaltrakts ergeben sich die typischen Symp-tome des POI.
RisikofaktorenAus der o.g. Pathophysiologie kann man die in der fol-genden Übersicht zusammengefassten Risikofaktorenfür die Entstehung eines POI ableiten [4, 8]:
89izin up2date 2018; 14: 87–102

90
CME-Fortbildung
igun
g nu
r m
it Z
ustim
mun
g de
s V
erla
ges.
SymptomeMerke
Ein distendiertes, druckempfindliches Abdomen istlaut Expertenkonsensus das relevanteste klinischeZeichen für einen POI [2].
Weitere Symptome sind:▪ Übelkeit und Erbrechen,▪ eine Intoleranz gegenüber oraler Nahrungsaufnahme,▪ verzögerter Abgang von Winden und Stuhl.
Die Abgrenzung von POI und PONV (Postoperative Nau-sea and Vomiting) ist nicht zu 110% geklärt. Teils wirdPONV als Teil eines POI gesehen, teils POI als Teil desPONV. Bisher fehlt hier eine klare Trennung, wobei inden Leitlinien der Society of Ambulatory Anesthesia 2014[12] zu lesen ist, dass PONV nicht auf die ersten 24 post-operativen Stunden begrenzt ist, sondern zu jeder Zeit impostoperativen Verlauf auftreten kann und ebenfalls mul-tifaktoriell patienten- sowie umweltbezogene Ursachenhat.
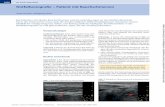
▶ Abb. 1 Konventionelles Röntgen mit charakteristischerSpiegelbildung bei Ileus. Quelle: Oestmann J. WelcheDiagnose stellen Sie? In: Oestmann J, Hrsg. Radiologie.2., akt. Aufl. Stuttgart: Thieme; 2005. doi:10.1055/b-004-135642.
PRAXISTIPP
Man untersucht den Patienten gezielt auf klinische,
laborchemische und radiologische Zeichen eines
sekundären POI aufgrund einer Komplikation:
▪ Hohlorganperforation:
– akutes Abdomen,
– erhöhte Infektionswerte,
– freie Luft im Röntgenbild des Abdomens,
▪ intraabdominaler Abszess:
– persistierend erhöhte Infektwerte,
– evtl. auffällige Drainageförderung,
▪ Anastomoseninsuffizienz:
– erhöhte Infektwerte,
– evtl. auffällige Drainageförderung.
Die
ses
Dok
umen
t wur
de z
um p
ersö
nlic
hen
Geb
rauc
h he
runt
erge
lade
n. V
ervi
elfä
lt
DiagnostikDas Expertengremium fand keinen Konsens bezüglichdes diagnostischen Vorgehens bei postoperativem Ileus,insbesondere was die Notwendigkeit der Bildgebung an-belangt [2].
MerkeDer postoperative Ileus ist in erster Linie eine kli-nische Diagnose, welche mittels Anamnese und kör-perlicher Untersuchung gestellt wird.
Konventionelles Röntgen (▶ Abb. 1), MRT (▶ Abb. 2), CT(▶ Abb. 3) und Kontrastmittelstudien sind alle als dieDiagnose stützende Bildgebung möglich, wobei das CTam sichersten eine mechanische oder andere Komponen-te eines sekundären Ileus darstellen kann.
CaveKlinische und radiologische Zeichen eines Ileusstimmen in der Praxis nicht immer überein.
So kann ein Patient mit ausgeprägter Spiegelbildung qua-si symptomfrei sein, ein anderer Patient mit wenigenSpiegeln im Röntgenbild hingegen massiv Beschwerdenhaben.
Ist ein sekundärer POI auszuschließen, muss man diffe-renzialdiagnostisch vor allem an eine mechanische Ob-struktion denken, z. B. durch eine torquierte Dunndarm-schlinge oder eine zu eng angelegte Anastomose. Be-steht ein solcher Verdacht, ist je nach Lokalisation ein Ab-domen-CT oder eine Endoskopie erforderlich.
Meißner T, Reißfelder C. Therapie postoperativer Darmpassagestörungen… Intensivmedizin up2date 2018; 14: 87–102

ng d
es V
erla
ges.
FAZIT
Der postoperative Ileus tritt in ca. 10% der Fälle als
physiologische Paralyse nach vor allem abdominal-
chirurgischen Eingriffen auf und kann, wenn er pro-
longiert besteht, sowohl den Patienten stark belas-
ten als auch erhebliche Kosten für das Gesundheits-
system verursachen.
Neurogene, hormonelle und iatrogene Ursachen sind
an der Entstehung eines POI beteiligt. Aus den un-
terschiedlichen Aspekten der Pathophysiologie des
POI ergeben sich zahlreiche beeinflussbare und vor-
gegebene Risikofaktoren für dessen Entwicklung.
Folglich ist auch die Therapie multimodal.
▶ Abb. 3 CT bei Ileus mit Darstellung der Flüssigkeitsspiegel. Quelle:
▶ Abb. 2 MRT bei Ileus mit klassischen Spiegeln. Quelle: Institut für Ra-diologische Diagnostik, Universitätsklinikum Carl Gustav Carus Dresden.
zum
per
sönl
iche
n G
ebra
uch
heru
nter
gela
den.
Ver
viel
fälti
gung
nur
mit
Zus
timm
u
KostenDa ein POI in der Regel einen prolongierten Krankenhaus-aufenthalt mit sich bringt, entstehen hierdurch relevanteKosten für das Gesundheitssystem.
Die Dauer der stationären Behandlung verlängert sich ummindestens 2–3 Tage. Hiermit gehen nicht nur höhereAufenthalts- und Behandlungskosten sowie ein erhöhterArbeitsausfall für die Patienten einher. Es besteht zusätz-lich eine höhere Wahrscheinlichkeit für das Auftreten an-derer Erkrankungen wie Pneumonie, Thrombose, Lun-genarterienembolie und Wundinfektionen sowie dieÜbertragung multiresistenter Erreger. Die Wiederaufnah-merate bei Patienten mit POI ist um 10% höher als bei Pa-tienten mit einem unauffälligen postoperativen Verlauf.
FAZIT
In den USA werden durch den POI Folgekosten von
geschätzt über 1,5 Milliarden US-Dollar im Jahr ver-
ursacht [13].
Institut für Radiologische Diagnostik, Universitätsklinikum Carl GustavCarus Dresden.
FALLBEISPIEL
Frau S. wurde heute zur Rechts-Hemikolektomie aufgenommen.
Schon im OP-Hemd und prämediziert fragt sie: „Frau Doktor,
sagen Sie mal, also ich habe normalerweise nie Problememit
dem Stuhlgang. Wie kommt denn so was? Also so was will ich ja
für mich nicht hoffen. Sie wissen, lange kann ich hier nicht blei-
ben… der Garten…“
Die Patientin ist zur postoperativen Überwachung auf die Inten-
sivstation geplant. Sie ist 70 Jahre alt, sowohl pulmonal als auch
kardial vorerkrankt und außerdemmassiv adipös.
Abmorgen werden Sie auf der Intensivstation eingesetzt sein.
Wie Sie bereits von Ihren Kollegen gehört haben, werden Ihnen
Problemewie die von Frau G. aus demersten Fallbeispiel hier teils
in noch stärkerer Ausprägung begegnen. Daher bitten Sie die
Anästhesie bei Frau S., besonders akribisch auf ein gutes peri-
operatives Management zu achten. Außerdem erläutern Sie der
Patientin selber noch einmal die wichtigsten Punkte der Opera-
tion und des perioperativen Geschehens.
91Meißner T, Reißfelder C. Therapie postoperativer Darmpassagestörungen… Intensivmedizin up2date 2018; 14: 87–102
Die
ses
Dok
umen
t wur
de

92
CME-Fortbildung
Die psychischen Konsequenzen eines verlängerten Kran-kenhausaufenthaltes für den Patienten und die damitmöglicherweise einhergehenden negativen Einflüsse aufdie Genesung werden hier nicht mit eingerechnet.
Ver
lage
s.
Therapie der postoperativenDarmpassagestörungen
MerkeDie Therapie der postoperativen Darmpassagestö-rungen basiert hauptsächlich auf einer guten Ileus-prophylaxe.
PRAXISTIPP
In Bezug auf den postoperativen Ileus liegt die Be-
tonung auf der Prävention des Krankheitsbildes mit
einer starken Empfehlung zu folgenden Maßnahmen:
▪ Einsatz der Epiduralanalgesie,
▪ Vermeiden von Überwässerung,
▪ Vermeiden einer nasogastralen Sonde.
Zur Therapie wird zu Kaugummikauen und dem Ein-
satz von Alvimopan geraten, vorausgesetzt, dass eine
Opioidtherapie durchgeführt wird. Die orale Gabe von
Magnesium erhält nur eine schwache Empfehlung.
Andere Maßnahmen, die im täglichen klinischen All-
tag verwendet werden, weisen aktuell ein zu geringes
Evidenzlevel auf.
Die
ses
Dok
umen
t wur
de z
um p
ersö
nlic
hen
Geb
rauc
h he
runt
erge
lade
n. V
ervi
elfä
ltigu
ng n
ur m
it Z
ustim
mun
g de
s
Präventive AllgemeinmaßnahmenERAS-Protokolle
Programme zur Enhanced Recovery after Surgery (ERAS-Programme) wurden entwickelt, um über festgesetztemultimodale perioperative Ansätze die Stressantwortdes Organismus auf einen operativen Eingriff zu reduzie-ren. Für die verschiedenen chirurgischen Fächer sind spe-zifische Guidelines auf der ERAS-Website zu finden. DieEmpfehlungen zum perioperativen Management vonelektiven Koloneingriffen wurden zuletzt 2013 überarbei-tet [14].
Epiduralanalgesie
Eine epidurale Lokalanästhesie kann den somatischenSchmerz vermindern. Anhand der oben beschriebenenSchmerzbahnen und des großen Anteils des N. vagus inder Verarbeitung viszeraler Schmerzen ist allerdingsnachvollziehbar, dass hiermit keine komplette Ausschal-tung der viszeralen Afferenzen und des sympathischenÜbergewichts in den efferenten Bahnen zu erreichen ist.Nichtsdestotrotz führt eine hohe Epiduralanalgesie überdie Blockade mitbeteiligter spinaler Bahnen zu einer be-
Meißner T, Reißfelder C. Therapie posto
schleunigten Rekonvaleszenz und vor allem einer deutli-chen Reduktion der abgerufenen Dosis an Opioidanalge-tika. Dies wiederum führt zu einer Reduktion des Auftre-tens eines POI bei Patienten, die mit einer Epiduralanal-gesie ausgestattet sind [15–17].
Andere Autoren fanden bei Patienten im ERAS-Pro-gramm keine Vorteile der Epiduralanalgesie im Vergleichzu anderen Analgetikaformen [18,19].
FAZIT
Obgleich die direkten Effekte der Epiduralanalgesie
auf die Darmmotilität bisher unklar bleiben, lässt sich
zusammenfassen, dass allein aufgrund der Tatsache,
dass Opioide eingespart werden können, die Epidu-
ralanalgesie in der Behandlung des POI von Nutzen
ist.
Wasser- und Elektrolythaushalt
Die Auswurfleistung des Herzens wird wesentlich vom in-travaskulären Volumen bestimmt. Bei einer intravaskulä-ren Hypovolämie kann es zu einer Hypoperfusion der Or-gane, insbesondere des Magen-Darm-Traktes, und einerdamit einhergehenden relativen Ischämie führen. BeiÜberwässerung hingegen wird ein Ödem der Darmwandriskiert, was ebenso zu Komplikationen führen kann.
Flüssigkeitsverschiebungen sollten über den Einsatz vonlaparoskopischen Verfahren und kurzen OP-Zeiten mini-miert werden. Die Manipulation am Darm, das Eventerie-ren desselben und die Vermeidung hoher Blutverlusteführt ebenso wie die orale Flüssigkeitsaufnahme bis zu2 Stunden vor dem Eingriff zu einer Reduktion des ver-schobenen Verteilungsvolumens [14].
Minimalinvasives Monitoring der Auswurfleistung kannbei der Regulierung des Flüssigkeitshaushaltes vor allembei kritischen Patienten hilfreich sein.
Postoperativ sollte ebenfalls eine Normovolämie – ambesten über orale Flüssigkeitsaufnahme – angestrebtwerden.
Minimalinvasive Eingriffe
MerkeBei einfachen laparoskopischen Eingriffen bleibt dieAktivierung der oben beschriebenen Entzündungs-kaskade nach Darmmanipulation aus. Für laparosko-pisch assistierte Eingriffe gilt dies allerdings nicht[20].
Nach Herausgabe der ERAS-Leitlinien zur kolorektalenChirurgie zeigten lediglich die laparoskopischen Eingriffe
perativer Darmpassagestörungen… Intensivmedizin up2date 2018; 14: 87–102

Die
ses
Dok
umen
t wur
de z
um p
ersö
nlic
hen
Geb
rauc
h he
runt
erge
lade
n. V
ervi
elfä
ltigu
ng n
ur m
it Z
ustim
mun
g de
s V
erla
ges.
eine Wirksamkeit auf die postoperative systemische Ent-zündungsreaktion. [21].
Opioidreduktion
Eine analgetisch wirksame Opioiddosis führt immer auchzu einer Affektion der gastrointestinalen Motilität, dahierfür bereits eine weitaus geringere Dosis ausreicht.Eine postoperativ höhere kumulative Opioiddosis korre-liert mit einer signifikant höheren Inzidenz eines POI [7].
Orale Nahrungsaufnahme
Eine frühe orale Nahrungsaufnahme – meist in Form vonFlüssigkost ab dem 1. postoperativen Tag – nach elekti-ven kolorektalen Operationen verkürzt die Krankenhaus-aufenthaltsdauer signifikant und senkt die Komplikati-onsrate. Die Sorge um eine Zunahme an Anastomosen-insuffizienzen bei zeitiger oraler Nahrungsaufnahme istunbegründet, da nicht nachzuweisen [22,23]. Obwohles bei einer frühen oralen Nahrungsaufnahme häufigerauch zu postoperativem Erbrechen kommt, ist die stan-dardisierte Anlage einer nasogastralen Sonde in der Regelnicht vonnöten.
Einige Studien propagieren die bereits präoperative Gabevon kohlenhydratreichen Flüssigkeiten am Tag vor demgeplanten Eingriff und am Morgen des OP-Tags, um einefrühzeitigere Wiederherstellung der Darmfunktion zu er-reichen. Die postoperative Insulinresistenz wird damitvermindert.
Mobilisation
Die frühe Mobilisation von Patienten ab dem 1. postope-rativen Tag führt zu einer signifikant kürzeren Kranken-hausaufenthaltsdauer. Innerhalb der ERAS-Protokollenimmt die Mobilisation der Patienten einen hohen Stel-lenwert ein, da sie nicht nur die Darmmotilität fördert,sondern auch zur Patientenmotivation beiträgt, pulmo-nalen Komplikationen vorbeugt und dem Katabolismusentgegenwirkt. Außerdem wirkt sie sich positiv auf eingeringeres Schmerzempfinden aus.
Kaugummi
Multiple Studien propagieren einen günstigen Effekt vonperi- und postoperativem Kaugummikauen auf das Wie-dereinsetzen der Darmtätigkeit [24–26]. Über zephalo-vagale Reflexe stimuliert eine „Schein-Fütterung“ mitKaugummi die intestinale myoelektrische Aktivität in Ma-gen, Duodenum und Rektosigmoid. Außerdem beobach-tet man eine erhöhte Serumkonzentration von Gastrin,Neurotensin und pankreatischem Polypeptid sowie eineerhöhte duodenale Sekretion.
Meißner T, Reißfelder C. Therapie postoperativer Darmpassagestörungen… Intensivmed
PRAXISTIPP
Diese vorgetäuschte Nahrungsaufnahme durch
Kaugummikauen verkürzt die Zeit bis zum ersten
Abgang von Winden und Stuhl, ohne die negativen
Nebeneffekte einer zeitnahen tatsächlichen Nah-
rungsaufnahme mit sich zu bringen.
Es fand sich interessanterweise eine niedrigere Plasma-konzentration von Entzündungsmarkern wie IL-8 undTNFRSF1A bei Patienten in der Kaugummi-Interventions-gruppe nach kolorektalen Eingriffen [27].
Dennoch wird der Effekt des Kaugummikauens aufgrunddes uneinheitlichen Studiendesigns mit geringen Patien-tenzahlen kontrovers diskutiert [28, 29], da bei größerenPatientenkollektiven teils nur geringe bis keine mess-baren Vorteile von Kaugummikauen gegenüber demStandard-ERAS-Programm erhoben wurden.
Bei der Expertenbefragung durch Gero et al. [2] erhältKaugummikauen keine 70%ige Zustimmung des Gremi-ums und wird daher nicht als Konsens in die internationa-len Empfehlungen mit aufgenommen. Allerdings wirdauch keine Ablehnung dieser potenziell prophylaktischenMaßnahme notiert und kein schädigender Effekt vonKaugummikauen festgestellt.
Nasensonde
Die Anlage einer nasogastralen Sonde ist laut Experten-konsens beim POI nicht obligatorisch. Eine postoperativnoch liegende Sonde kann auch ohne vorheriges Abklem-men oder Kontrastmittelgabe entfernt werden [2].
MerkeDas routinemäßige, prophylaktische Einbringen einerMagensonde bringt keine Vorteile in Bezug auf Ileus-prävention, Entlastung einer Anastomose, Wohl-befinden des Patienten, das Auftreten von pulmona-len Infekten oder die Krankenhausaufenthaltsdauer[30].
Das postoperative Belassen oder Wiedereinbringen einernasogastralen Sonde sollte bei wachen Patienten nachsorgfältiger Abwägung – auch der möglichen Komplika-tionen – eine Einzelfallentscheidung bleiben und vor al-lem dann in Betracht gezogen werden, wenn im Rahmeneines POI Erbrechen und ein aufgetriebenes Abdomenüberwiegen.
Totale parenterale Ernährung
Eine totale parenterale Ernährung wird bei POI erst abdem 7. Tag insuffizienter oraler Nahrungsaufnahmeempfohlen [2].
93izin up2date 2018; 14: 87–102

FAZIT
Therapieoptionen des postoperativen Ileus
Präventive Allgemeinmaßnahmen▪ Umsetzen der ERAS-Empfehlungen
▪ Epiduralanalgesie
▪ ausgeglichener Wasser- und Elektrolythaushalt
▪minimalinvasive Operationstechnik
▪Opioidreduktion
▪ Kaugummi kauen
▪ frühe orale Nahrungsaufnahme
▪ frühe Mobilisation
▪ Vermeiden einer nasogastralen Sonde
Medikamentöse Therapie▪ Alvimopan
▪ Lidocain i. v.
▪Magnesium i. v. intraoperativ
▪ Koffein
▪ Gastrografin
▪ Einsatz von NSAID
▪ Daikenchuto
▪Mosapride
▪ Laxanzien
▪ Erythromycin i. v.
FALLBEISPIEL
Ihre Kollegen von der Anästhesie beteuern, alle peri-
operativen Maßnahmen zur Ileusprophylaxe einge-
halten zu haben. Die Operation von Frau S. war kom-
plikationslos durchgeführt worden, die OP-Zeit kurz
und die Manipulation am Darm laut Berichten der
Operateure gering. Dennoch kommt die Magen-
Darm-Passage der Patientin nicht so recht in Gang.
Sie liegt aufgrund eines postoperativen Delirs auch
immer noch auf Ihrer Intensivstation. AnMobilisation,
Kaffeetrinken oder Kaugummikauen ist bei der älte-
renDameaufgrund der fehlenden Compliance aktuell
nicht zu denken. Pfleger Tim schlägt einen „Donner-
tropf“ vor. Sie informieren sich zunächst über andere
medikamentöse Behandlungsoptionen für Patienten
mit mangelnder Mitarbeit.
94
CME-Fortbildung
Die
ses
Dok
umen
t wur
de z
um p
ersö
nlic
hen
Geb
rauc
h he
runt
erge
lade
n. V
ervi
elfä
ltigu
ng n
ur m
it Z
ustim
mun
g de
s V
erla
ges.
Therapieoptionen des POI fasst die folgende Übersichtzusammen.
Medikamentöse Therapie
MerkeAlvimopan p. o. und die intravenöse Gabe von Lido-cain und Neostigmin haben vermutlich eine positiveWirkung auf die Motilität des GI-Traktes. Alle anderenin der Praxis häufig eingesetzten Wirkstoffe ergabenkeine positiven Effekte auf den POI [31].
Zu den untersuchten Substanzen gehören Erythromycin,Cisaprid, Cholezystokinin-Varianten, Dihydroergotamin,Propranolol, Albumin, Vasopressin, Fruktose, Pantothen-säure und Dopaminantagonisten. Ihre nach Studienlageeher fragliche Wirksamkeit beruht u. a. auch auf sehr in-homogenen Daten.
Cisaprid wurde inzwischen aufgrund von ausgeprägtenkardialen Nebenwirkungen vom Markt genommen. Fürdie anderen Arzneimittel wurden bisher keine regelmäßi-gen adversen Ereignisse dokumentiert.
Meißner T, Reißfelder C. Therapie posto
µ-Rezeptor-Antagonist (Alvimopan)
MerkeDie prophylaktische orale Einnahme von Alvimopan2 Stunden vor einem Eingriff und dann 2 × täglichzeigten einen signifikanten Effekt auf das zeitigereWiedereinsetzen der gastrointestinalen Funktionen.
Die Wirkung von sowohl 12mg als auch eine niedrigereDosis von 6mg von Alvimopan war insbesondere in derSubgruppe der Patienten, welche eine PCA erhielten, er-kennbar [32]. Die Gabe dieser Arznei zeigte sich in dieserMetaanalyse von Drake u. Ward relativ nebenwirkungs-arm mit einem berichteten häufigeren Vorkommen vonHypokaliämie, Schlaflosigkeit, Übelkeit und Pyrexie. Eswurden keine schwerwiegenden Nebenwirkungen beob-achtet.
Lidocain i. v.
Die perioperative intravenöse Gabe von Lidocain (in derRegel ein Bolus von 1,5–2mg/kg und einer anschließen-den Infusion von 1,5–3mg/kgKG/h) für bis zu 24 Stundenpostoperativ verkürzt nicht nur die Zeit bis zur ersten De-fäkation signifikant, sondern senkt ebenfalls den Opio-idbedarf und die Plasmalevel der Interleukine 8, 6 und1. Diese Effekte wurden allerdings nur bei abdominellenEingriffen beobachtet [33]. Wongyingsinn et al. zeigten,dass die i. v. Gabe von Lidocain bei laparoskopisch assis-tierten kolorektalen Eingriffen in Bezug auf Wiederher-stellung der Magen-Darm-Funktion, Schmerzempfinden,Komplikationsrate und Krankenhausaufenthaltsdauergleichwertig zur thorakalen Epiduralanalgesie ist [34].
perativer Darmpassagestörungen… Intensivmedizin up2date 2018; 14: 87–102

Die
ses
Dok
umen
t wur
de z
um p
ersö
nlic
hen
Geb
rauc
h he
runt
erge
lade
n. V
ervi
elfä
ltigu
ng n
ur m
it Z
ustim
mun
g de
s V
erla
ges.
Koffein
Das verbreitete Genussmittel Kaffee zeigt in der täg-lichen Beobachtung eine stimulierende Wirkung auf dieDarmfunktion. Aus diesem Grund wurden mehrere Stu-dien zu dessen Einsatz beim POI und dessen Präventiondurchgeführt. Die 3 × tägliche Einfuhr von 100ml Kaffeeab dem 1. postoperativen Tag verkürzte die Zeit bis zurersten Defäkation im Vergleich zur Einnahme derselbenMenge warmen Wassers signifikant [35,36]. Zu bemer-ken ist, dass auch die Gabe von entkoffeiniertem Kaffeezu einer Stimulation der Kolonaktivität führt, allerdingsin einem etwas geringeren Ausmaß.
Gastrografin
Orales Kontrastmittel wird im Alltag häufig angewandt,um einen Subileus zu therapieren oder einen postopera-tiven Ileus zu lösen.
Es zeigt sich eine klinisch gute Wirkung von Gastrografinvor allem auf den unteren Gastrointestinaltrakt, aber kei-ne signifikante Wirkung auf die Toleranz von flüssigeroder fester Kost [37,38].
MerkeDer Vorteil der Gastrografin-Gabe liegt neben dertherapeutischen in seiner zeitgleich bestehendendiagnostischen Einsatzmöglichkeit.
In Geros Expertenumfrage befürworteten ein Drittel derTeilnehmer den Einsatz von wasserlöslichen Kontrastmit-teln beim POI [2].
Nichtsteroidale Antiphlogistika
Nichtsteroidale Antiphlogistika (NSAID) wirken vor allemder Entzündungsreaktion im Rahmen eines Ileus ent-gegen. Die von den Makrophagen produzierten Zytokineführen zu einer vermehrten Aktivierung der Cyclooxyge-nasen, welche durch die NSAID geblockt werden.
Über die neurogen getriggerte vermehrte NO-Produk-tion kommt es außerdem zu einer vermehrten Aktivie-rung der Cyclooxygenase 2.
Einige Autoren geben allerdings zu bedenken, dass derEinsatz von NSAID die Wundheilung beeinträchtigt undzu einer erhöhten Rate an Anastomoseninsuffizienzenführen kann.
Während dieser Effekt noch diskutiert wird, ist ein klarerBenefit in Bezug auf die Wiederherstellung der Darmpas-sage führend [39]. Der kurzzeitige Einsatz von NSAIDnach elektiven kolorektalen Eingriffen wird nach Berück-sichtigung sowohl der Kontraindikationen einer NSAID-Therapie als auch der Risikofaktoren für eine Anastomo-seninsuffizienz empfohlen.
Meißner T, Reißfelder C. Therapie postoperativer Darmpassagestörungen… Intensivmed
PRAXISTIPP
Der Einsatz von NSAID sollte zunächst auf 48 Stun-
den postoperativ begrenzt werden. Hinzu kommt,
dass der Einsatz von NSAID den Opioidkonsum redu-
zieren und so indirekt die Wiederherstellung der
Darmfunktion beeinflussen kann.
Magnesium i. v.
Die intraoperative i. v. Gabe von Magnesium kann dieSchmerzwahrnehmung reduzieren und damit den post-operativen Opioidbedarf und in dessen Folge das Risikoeines POI reduzieren [4].
Daikenchuto (TU-100)
Die traditionelle japanische Medizin Kampo steht für dieBehandlung von Krankheiten mit Heilkräutern. Ein Ge-misch aus Japanischem Pfeffer, Ingwer und Gingseng er-gibt Daikenchuto [40]. In vorgegebenen Mengen werdendie Substrate zusammengefügt, dann mit heißemWasserein Auszug gewonnen, welcher wiederum pulverisiertwird. Diese Arznei wird traditionell bei Meteorismus, Obs-tipationen und einem intraabdominellen Kältegefühl ver-abreicht.
Viele placebokontrollierte Studien zeigten, dass die lin-dernde Wirkung auf Blähungen offenbar auf eine Stimu-lierung der Kolonmotilität durch dieses Medikament zu-rückzuführen ist. Letztere wird am ehesten über die Be-einflussung von Neurotransmittern wie Acetylcholin undCalcitonin Gene related Peptide (CGRP) vermittelt. Studi-en zur Pharmakokinetik sind allerdings schwierig, da sichdas simultane Nachverfolgen der einzelnen Komponen-ten und deren synergistischer Wirkung als Herausforde-rung darstellt. Endo et al. fanden an ihrer Studie an Mäu-sen heraus, dass Daikenchuto außerdem eine antiinflam-matorische Wirkung im Gastrointestinaltrakt entfaltet.
Die Ergebnisse einer multizentrischen Studie über dieorale Gabe von 5 g Daikenchuto 3 × täglich zu den Mahl-zeiten zwischen dem 3. präoperativem und dem 14. post-operativen Tag nach Pankreatikoduodenektomie ist nochnicht veröffentlicht. Zur positiven Wirkung auf die gas-trointestinale Motilität nach kolorektalen, Magen- undLebereingriffen liegen hingegen schon vielversprechendeErgebnisse vor [41,42].
Serotonin-Rezeptor-Agonisten (Metoclopramid,Mosaprid)
Mosaprid, ein selektiver 5-HT4-Agonist, scheint eine po-sitive prophylaktische Wirkung auf das Wiedereinsetzender gastrointestinalen Funktion zu haben. Hierzu wurdenab dem 1. postoperativenTag 3 × täglich 15mg Mosapridper os verabreicht. Zur Verifizierung dieser Ergebnissesind allerdings weiter qualitativ hochwertige Studien not-wendig. Die Effekte scheinen auf der antientzündlichen
95izin up2date 2018; 14: 87–102

96
CME-Fortbildung
Die
ses
Dok
umen
t wur
de z
um p
ersö
nlic
hen
Geb
rauc
h he
runt
erge
lade
n. V
ervi
elfä
ltigu
ng n
ur m
it Z
ustim
mun
g de
s V
erla
ges.
Wirkung zu beruhen, die Mosaprid auf den Gastrointesti-naltrakt hat.
Metoclopramid zeigte diesbezüglich hingegen keinen Ef-fekt [32]. Diese Substanz stimuliert vornehmlich die gas-trale Sekretion. Die Wirkung von Metoclopramid auf ei-nen POI ist insgesamt wenig untersucht. Obwohl auchdieses Medikament in der klinischen Anwendung häufigzum Tragen kommt, zeigen die hierzu durchgeführtenStudien keinen Effekt auf das Lösen eines POI.
Laxanzien
▪ Andersen et al. [43] fanden keine Wirkung von Mag-nesiumoxid nach kolorektalen Eingriffen. Eine Wir-kung wurde in anderen randomisiert kontrolliertenStudien [44] bei Leberresektionen und abdominellenHysterektomien allerdings beschrieben.
▪ Bisacodyl nach kolorektalen Eingriffen im Rahmeneines ERAS-Protokolls zeigte ebenfalls eine positiveWirkung auf die Beschleunigung der Darmpassage.
Daher empfehlen die ERAS Guidelines von 2012 denpostoperativen Einsatz von Laxanzien, allerdings mitniedrigem Evidenzlevel.
Nikotin
Sowohl in den prä- und paravertebralen Ganglien als auchim in- und extrinsischen Nervensystem des Kolons findensich Nikotinrezeptoren. Durch Nikotinkonsum kommt eszu einer Geschwindigkeitszunahme der Passage im Ko-lon, gefolgt von einer Relaxation im Colon descendens[4]. Bei Gesunden zeigt sich nach Administration von Ni-kotin eine beschleunigte Darmpassage. Außerdem unter-drückt Nikotin die Wirkung und Freisetzung von Entzün-dungsmediatoren.
Hat ein Raucher mit POI postoperativ das starke Bedürfnisnach Zigarettenkonsum, könnte das Zulassen des Niko-tinabusus in diesem Fall förderlich für die Darmpassagesein. Bei Nichtrauchern könnte die transdermale Applika-tion oder die Anwendung von nikotinhaltigen Kaugum-mis zur POI-Behandlung in Erwägung gezogen werden.Dies wird aber weder von den ERAS-Protokollen nochden von Gero zusammengerufenen Experten empfohlen.
Erythromycin
Erythromycin wirkt schon in niedriger Dosierung als Mo-tilin-Rezeptor-Agonist. Die Daten zu dessen Verwendungstammen allerdings aus älteren kleineren Studien und be-ziehen sich vor allem auf eine verzögerte Magenentlee-rung [45]. Aufgrund des ausgedehnten Risikoprofils mitEntwicklung von Antibiotikaresistenzen, kardiovaskulä-ren Nebenwirkungen und der Interferenz mit dem Cyto-chrom-P450-System wird von der prophylaktischen Gabevon Erythromycin abgeraten. Sollte es postoperativ zueiner verzögerten Magenentleerung kommen, empfeh-len Schulze u. Heidecke [45], die Therapie auf maximal
Meißner T, Reißfelder C. Therapie posto
3 Tage zu beschränken. Hinzu kommt, dass es ab diesemZeitpunkt zu einer Herunterregulation der Motilinrezep-toren kommt.
Ondansetron (5-HT‑3-Rezeptor-Antagonist)
Die Kombination von 5-HT‑3-Rezeptor-Antagonisten undDexamethason scheint sehr wirksam gegen postopera-tive Übelkeit und Erbrechen zu sein. Eine Wirkung aufden POI ist nicht beschrieben [4].
Der Vollständigkeit halber sei Cisapride erwähnt. Obwohlin einigen Studien die Förderung der gastronintestinalenMotilität nachgewiesen werden konnte, wurde dieser 5-HT‑3-Rezeptor-Antagonist aufgrund einer hohen Inzi-denz von kardiovaskulären Ereignissen vom Markt ge-nommen.
Ghrelin-Rezeptor-Agonisten (Ghrelin, Ipamorelin,Ulimorelin)
Die Gabe von Ghrelin-Rezeptor-Agonisten zeigte sich inder Übersichtsarbeit von Drake u. Ward [32] nur bedingtbis nicht wirkungsvoll zur Prophylaxe des POI. Eine Meta-analyse war hier aufgrund der mangelhaften Daten aller-dings nicht möglich. Auch bei der Gabe von Ghrelin-Re-zeptor-Agonisten waren die unerwünschten Nebenwir-kungen vergleichbar mit denen in der Placebogruppe.
Neostigmin
Bei Neostigmin handelt es sich um ein indirektes Para-sympathomimetikum und einen reversiblen Cholineste-rasehemmer. Der moderaten Wirkung von Neostigminauf die träge Darmpassage steht allerdings ein aus-geprägtes Nebenwirkungsprofil mit Hypersalivation, Er-brechen, abdominellen Krämpfen und Bradykardien ge-genüber. Aus diesem Grund besteht Konsens, dass Neo-stigmin nicht zur Behandlung des postoperativen Ileuseingesetzt werden sollte [2].
ZusammenfassungMerke
Da bis dato unterschiedlichste Definitionen des POIund des PPOI vorlagen, ist die Vergleichbarkeit inallen zu dem Thema bisher vorliegenden Studienbegrenzt.
Erst im Jahr 2017 fand eine Delphi-Umfrage [2] statt, wel-che einen Konsens zur Definition des postoperativen Ileusfand. Demnach handelt es sich um eine vorübergehendeInhibierung der gastrointestinalen Motilität nach chirurgi-scher Intervention aufgrund nichtmechanischer Ursa-chen, welche eine ausreichende orale Nahrungsaufnahmeverhindert. Zu hoffen ist, dass man über die neue Konsen-susdefinition ein homogeneres Patientenkollektiv und da-mit eine erhöhte Aussagekraft der zukünftigen Studien zudem Thema erreicht. Infolgedessen sind auch qualitativhöherwertige Aussagen zur Therapie des POI zu erwarten.
perativer Darmpassagestörungen… Intensivmedizin up2date 2018; 14: 87–102

Die
ses
Dok
umen
t wur
de z
um p
ersö
nlic
hen
Geb
rauc
h he
runt
erge
lade
n. V
ervi
elfä
ltigu
ng n
ur m
it Z
ustim
mun
g de
s V
erla
ges.
Fest steht, dass es sich bei der Entwicklung eines POI umeine zunächst physiologische Paralyse der Magen-Darm-Tätigkeit handelt, die vor allem nach Manipulation amDarm bei offenen abdominalchirurgischen, aber auch an-deren, z. B. orthopädischen oder kardialen Eingriffen auf-treten kann.
Wenn das multifaktoriell bedingte Krankheitsbild überden 4. postoperativen Tag hinaus andauert, spricht manvon einem prolongierten postoperativen Ileus, der durchein schmerzhaft gespanntes Abdomen und eine Intole-ranz gegenüber oraler Nahrungsaufnahme gekennzeich-net ist. Zusätzlich kann es zu Übelkeit, Erbrechen unddemverzögerten Abgang vonWindenund Stuhl kommen.
Ein manifester Ileus ist für die Patienten subjektiv starkbelastend und führt häufig zu einem prolongierten Kran-kenhausaufenthalt. Durch den POI selbst und die verlän-gerten Liegezeiten können Komplikationen entstehen,welche für die Gesundheitssysteme immense Mehrkos-ten verursachen.
Daher ist es eminent wichtig, dass vor allem durch um-sichtige perioperative Maßnahmen der Entstehung einesPOI vorgebeugt wird. Aufgrund der eingeschränkten the-rapeutischen Möglichkeiten bei manifestem Ileus kommtder Prävention eine besonders wichtige Aufgabe zu.
Hierbei ist eine gute interdisziplinäre Zusammenarbeitvon Chirurgen, Anästhesisten und Pflegepersonal ge-fragt. Im Rahmen der ERAS-Programme nimmt zusätz-lich die präoperative Aufklärung des Patienten einen ho-hen Stellenwert ein. Bei nicht intensivpflichtigen Patien-ten ist über das Setzen postoperativer Nahziele und auf-grund des Hintergrundwissens mit einer erhöhten Selbst-wirksamkeit und einer gesteigerten Compliance zu rech-nen. Dies führt nachweislich zu einer schnelleren Entlas-sung aus dem Krankenhaus.
Patienten, die nach den ERAS-Protokollen behandelt wur-den, konnten 2,5 Tage früher das Krankenhaus verlassen.Die 30-Tage-Morbidität war halbiert und die Wiederauf-nahmerate nicht höher als bei Patienten außerhalb desRegimes [46].
Präoperativ sollten schon durch den Patienten beeinfluss-bare Risikofaktoren wie Rauchen und Übergewicht redu-ziert werden. Auf eine Darmreinigung sollte verzichtetwerden und der Patient bis kurz vor dem Eingriff am bes-ten hochkalorische Nahrung zu sich nehmen. Vor undwährend der Operation ist auf einen ausgeglichenenWasser- und Elektrolythaushalt zu achten. Des Weiterenwird die Anlage einer Epiduralanalgesie mit Nachdruckempfohlen. Die Gabe von Opioiden sollte perioperativ sogering wie möglich gehalten werden.
Meißner T, Reißfelder C. Therapie postoperativer Darmpassagestörungen… Intensivmed
Zur Prophylaxe des POI wird vom Operateur eine mög-lichst geringe Manipulation des Darms erwartet. Laparo-skopische Interventionen zeigten sich hierbei vorteilhaftgegenüber offenen Eingriffen. Außerdem ist auf eine kur-ze OP-Dauer und einen geringen Blutverlust zu achten.
Postoperativ ist vor allem die Begrenzung der Schmerzenwichtig, welche innerhalb der ersten 48 Stunden nachdem Eingriff auch mit Unterstützung von NSAID kupiertwerden können. Eine nasogastrale Sonde sollte, soweitkeine Kontraindikationen gegen diese Maßnahme spre-chen, umgehend entfernt werden. Der Patient solltevom ärztlichen und pflegerischen Personal bereits am1. postoperativen Tag zur Mobilisation angehalten wer-den und mit dem Kostaufbau beginnen.
Kommt es unter diesen Allgemeinmaßnahmen dennochzu einem postoperativen Ileus, können Kaffeekonsumund das regelmäßige Kaugummikauen die Darmmotilitätsteigern. Diese einfachen Maßnahmen repräsentiereneine deutlich kostengünstigere Alternative zum Einsatzvon Alvimopan. Auf Intensivstationen sind aufgrund derKrankheitsschwere der Patienten allerdings die meistenAllgemeinmaßnahmen schwieriger umzusetzen.
Wache Patienten sollten so gut wie möglich in die ERAS-Programme eingebunden werden.
Bei intubierten Patienten kommt das Problem der entera-len Ernährung hinzu. Im Vergleich zur parenteralen Er-nährung ist die enterale Ernährung sicherer und mit bes-seren Therapieverläufen verbunden. Enteral zugeführteNährstoffe erhalten über trophische Effekte die intestina-le Funktion und Flora aufrecht. Eine Atrophie der Darm-zotten wird verhindert und die intestinale Permeabilitätreduziert. Außerdem wird die intestinale Durchblutungstimuliert und dadurch der Magen-Darm-Trakt vor Ischä-mie und Reperfusionsschäden geschützt. Zusätzlich wirddie Immunfunktion des Darms aufrechterhalten.
Eine 24–48 Stunden nach Aufnahmen auf die Intensivsta-tion begonnene enterale Ernährung reduziert infektiöseKomplikationen [47]. Dennoch beeinträchtigen Funk-tionsstörungen des Gastrointestinaltrakts häufig dieDurchführung einer adäquaten enteralen Ernährung. Ne-ben dem POI spielen Magenentleerungsstörungen, ins-besondere bei neurochirurgischen Patienten, und Diar-rhöen eine große Rolle.
Aufgrund der kritischen Erkrankungen von Intensivpa-tienten, welche oft mit Funktionsstörungen mehrerer Or-gansysteme einhergehen, sind z.B. Elektrolytstörungenund Störungen des Wasserhaushaltes häufig zu beobach-ten. Die Umverteilung der Volumina bei Sepsis oder Herz-insuffizienz sowie der häufige Ausfall der Nierenfunktionund entsprechende Störungen im Gleichgewicht derElektrolyte sind nur als einige Beispiele zu nennen. Hinzu
97izin up2date 2018; 14: 87–102

KERNAUS
▪ Beim po
siologisc
mit sowo
objektive
▪ Das mult
eine suff
▪ Präopera
tion ein a
präopera
▪ Intraope
Opioiddo
sollten m
pulation
▪ Postope
ab dem 1
oralen N
▪ Tritt trot
aufgetrie
über ora
Stuhlabg
▪ Das Kran
▪ Bei Auftr
und das
▪Weitere
die Beha
kenchut
98
CME-Fortbildung
igun
g nu
r m
it Z
ustim
mun
g de
s V
erla
ges.
kommen die meist hohe Kumulativdosis von Opioiden,die Gabe von Diuretika und Katecholaminen.
Ein akribisches Flüssigkeitsmanagement mit Dokumenta-tion von Ein- und Ausfuhr, Stundenurin und der Messungdes intravasalen Volumens wird zum Erreichen einer Null-bilanz empfohlen. Ebenso die mindestens 1 × täglicheÜberprüfung der Elektrolyte.
Kommt es zum postoperativen Ileus, gilt es, die wenigenmedikamentösen Möglichkeiten zur Therapie des mani-festen POI auszuschöpfen. Hierbei steht neben Alvimo-pan und der Reduktion der Kumulativdosis an Opioidennoch die Gabe von Lidocain i. v., Magnesium i. v. – beidesbereits intraoperativ zur Schmerzreduktion verabreicht –,Nikotin, Mosapride, Erythromycin, Laxanzien oder Gas-trografin zur Verfügung. Aufgrund der begrenzten Wirk-samkeit liegt aber auch und vor allem bei Patienten derIntensivstation ein ganz besonderes Augenmerk auf derPrävention und der Reduktion von durch den Patientenund das perioperativ betreuende Team beeinflussbarenRisikofaktoren.
SAGEN
stoperativen Ileus handelt es sich um eine häufige phy-
he bis pathologische Paralyse des Magen-Darm-Traktes
hl subjektiver Belastung des einzelnen Patienten als auch
r Belastung des Gesundheitssystems.
ifaktoriell bedingte Krankheitsbild sollte vor allem durch
iziente Prävention abgewendet werden.
tiv zählen zu den beeinflussbaren Faktoren der Präven-
usgeglichener Wasser- und Elektrolythaushalt, die kurze
tive Nahrungskarenz, ggf. mit Carbohydrate Loading.
rativ sollten eine Epiduralanalgesie eingesetzt und die
sis so gering wie möglich gehalten werden. Außerdem
inimalinvasive Operationstechniken mit geringer Mani-
am Darm bevorzugt werden.
rativ sollte eine Nasensonde zeitnah entfernt, der Patient
. Tag mobilisiert werden und ab demselbenTagmit der
ahrungsaufnahme beginnen.
z alledem ein POI auf, sind die typischen Symptome ein
benes, schmerzhaftes Abdomen, die Intoleranz gegen-
ler Nahrungsaufnahme, fehlendeWinde und fehlender
ang sowie Übelkeit und Erbrechen.
kheitsbild wird klinisch diagnostiziert.
eten eines POI werden die Gabe von Alvimopan per os
Kauen von Kaugummi empfohlen.
mögliche Therapieansätze umfassen die Gabe von Kaffee,
ndlung mit NSAID, Gastrografin, Magnesium i. v., Dai-
o, Mosapride, Laxanzien, Nikotin und Erythromycin.
Meißner T, Reißfelder C. Therapie posto
Interessenkonflikt
perati
Die Autoren geben an, dass keine Interessenkonflikte vor-liegen.
Autorinnen/Autoren
ver Darmpassages
Theresa Maria Meißner
Dr. med., Jahrgang 1987. 2006–2012 Studiumder Humanmedizin an der Ruhr-UniversitätBochum, Université de Strasbourg, in Brüssel,Bozen und Neuchâtel, 2013–2015 Weiter-bildungsassistentin Innere Medizin amSt. Elisabeth Hospital Bochum, 2014 Promotion
an der Ruhr-Universität Bochum, 2015 Fachkunde Rettungs-dienst. Seit 2015 Assistenzärztin der Klinik und Poliklinik fürViszeral-, Thorax- und Gefäßchirurgie der UniversitätsklinikDresden. Schwerpunkte: Notfall- und Intensivmedizin.
viel
fält
Christoph Reißfelder
Prof. Dr. med., MHBA. Studium der Human-medizin an der Universität Hamburg und derFreien Universität Berlin. 2003–2006 wissen-schaftlicher Mitarbeiter in der Abteilung fürAllgemein-, Gefäß- und Thoraxchirurgie an derCharité, Universitätsklinikum Berlin. 2006–
her
unte
rgel
aden
. Ver
2012 wissenschaftlicher Mitarbeiter der Klinik für Allgemein-,Viszeral- und Transplantationschirurgie der UniversitätsklinikHeidelberg. 2009 Facharzt für Chirurgie, 2014 Facharzt fürGefäßchirurgie, 2016 Facharzt für Viszeralchirurgie. 2012Habilitation. Seit 2012 Oberarzt und seit 2015 LeitenderOberarzt und stellvertretender Klinikdirektor der Klinik undPoliklinik für Viszeral-, Thorax- und Gefäßchirurgie der Univer-sitätsklinik Dresden.
Geb
rauc
h
Korrespondenzadresse
de z
um p
ersö
nlic
hen
Dr. med. Theresa MeißnerKlinik und Poliklinik für Viszeral-, Thorax- und GefäßchirurgieUniversitätsklinikum Carl Gustav CarusAn der Technischen Universität DresdenFetscherstraße 7401307 Dresdentheresa.meissner@universitätsklinikum-dresden.de
okum
ent w
ur
Wissenschaftlich verantwortlichgemäß Zertifizierungsbestimmungen
Die
ses
D
Wissenschaftlich verantwortlich gemäß Zertifizierungs-bestimmungen für diesen Beitrag ist Dr. med. TheresaMeißner, Dresden.törungen… Intensivmedizin up2date 2018; 14: 87–102

Die
ses
Dok
umen
t wur
de z
um p
ersö
nlic
hen
Geb
rauc
h he
runt
erge
lade
n. V
ervi
elfä
ltigu
ng n
ur m
it Z
ustim
mun
g de
s V
erla
ges.
Literatur
[1] Vather R, Josephson R, Jaung R et al. Development of a riskstratification system for the occurrence of prolonged postop-erative ileus after colorectal surgery: a prospective risk factoranalysis. Surgery 2015; 157: 764–773. doi:10.1016/j.surg.2014.12.005
[2] Gero D, Gie O, Hubner M et al. Postoperative ileus: in search ofan international consensus on definition, diagnosis, and treat-ment. Langenbecks Arch Surg 2017; 402: 149–158.doi:10.1007/s00423-016-1485-1
[3] Vather R, Trivedi S, Bissett I. Defining postoperative ileus: re-sults of a systematic review and global survey. J GastrointestSurg 2013; 17: 962–972. doi:10.1007/s11605-013-2148-y
[4] Bragg D, El-Sharkawy AM, Psaltis E et al. Postoperative ileus:Recent developments in pathophysiology and management.Clin Nutrit 2015; 34: 367–376. doi:10.1016/j.clnu.2015.01.016
[5] Delaney CP. Postoperative ileus profiles, risk factors, and defi-nitions – a framework for optimizing surgical outcomes in pa-tients undergoing major abdominal and colorectal surgery.Clin Consens Update Gen Surg 2006. Im Internet: http://www.clinicalwebcasts.com/pdfs/GenSurg_WEB.pdf; Stand:01.03.2018
[6] Wolthuis AM, Bislenghi G, Fieuws S et al. Incidence of pro-longed postoperative ileus after colorectal surgery: a system-atic review and meta-analysis. Colorectal Dis 2016; 18: O1–O9. doi:10.1111/codi.13210
[7] Gan TJ, Robinson SB, Oderda GM et al. Impact of postsurgicalopioid use and ileus on economic outcomes in gastrointestinalsurgeries. Curr Med Res Opin 2015; 31: 677–686.doi:10.1185/03007995.2015.1005833
[8] Murphy MM, Tevis SE, Kennedy GD. Independent risk factorsfor prolonged postoperative ileus development. J Surg Res2016; 201: 279–285. doi:10.1016/j.jss.2015.10.047
[9] Holte K. Postoperative ileus progress towards effective ma-nagement. Drugs 2002; 62: 2603–2615. doi:10.2165/00003495-200262180-00004
[10] Koscielny A, Engel D, Maurer J et al. The role of lymphoid tissuein the attenuation of the postoperative ileus. Am J Physiol Gas-trointest Liver Physiol 2013; 304: G401–G412. doi:10.1152/ajpgi.00161.2012
[11] The FO, Bennink RJ, Ankum WM et al. Intestinal handling-in-duced mast cell activation and inflammation in human post-operative ileus. Gut 2008; 57: 33–40. doi:10.1136/gut.2007.120238
[12] Gan TJ, Diemunsch P, Habib AS et al. Consensus guidelines forthe management of postoperative nausea and vomiting.Anesth Analg 2014; 118: 85–113. doi:10.1213/ANE.0000000000000002
[13] Goldstein JL, Matuszewski KA, Delaney CP et al. Inpatient eco-nomic burden of postoperative ileus associated with abdomi-nal surgery in the United States. Pharm Ther 2007; 32: 82–90
[14] Gustafsson UO, Scott MJ, Schwenk W et al. Guidelines for peri-operative care in elective colonic surgery: Enhanced RecoveryAfter Surgery (ERAS®) Society recommendations. World J Surg2013; 37: 259–284. doi:10.1007/s00268-012-1772-0
[15] Zingg U, Miskovic D, Hamel CT et al. Influence of thoracic epi-dural analgesia on postoperative pain relief and ileus after lap-aroscopic colorectal resection: Benefit with epidural analgesia.Surg Endosc 2009; 23: 276–282. doi:10.1007/s00464-008-9888-x
Meißner T, Reißfelder C. Therapie postoperativer Darmpassagestörungen… Intensivmed
[16] Khan SA, Khokhar HA, Nasr AR et al. Effect of epidural analge-sia on bowel function in laparoscopic colorectal surgery: a sys-tematic review and meta-analysis. Surg Endosc 2013; 27:2581–2591. doi:10.1007/s00464-013-2794-x
[17] Marret E, Remy C, Bonnet F et al. Meta-analysis of epidural an-algesia versus parenteral opioid analgesia after colorectal sur-gery. Br J Surg 2007; 94: 665–673. doi:10.1002/bjs.5825
[18] Levy BF, Scott MJ, Fawcett W et al. Randomized clinical trial ofepidural, spinal or patient-controlled analgesia for patientsundergoing laparoscopic colorectal surgery. Br J Surg 2011;98: 1068–1078. doi:10.1002/bjs.7545
[19] Borzellino G, Francis NK, Chapuis O et al. Role of epidural anal-gesia within an eras program after laparoscopic colorectal sur-gery: a review and meta-analysis of randomised controlledstudies. Surg Res Pract 2016; 2016: 7543684. doi:10.1155/2016/7543684
[20] Venara A. Postoperative ileus: Pathophysiology, incidence, andprevention. J Visc Surg 2016; 153: 439–446
[21] Watt DG, McSorley ST, Horgan PG et al. Enhanced recoveryafter surgery: which components, if any, impact on the sys-temic inflammatory response following colorectal surgery?: Asystematic review. Medicine (Baltimore) 2015; 94: e1286.doi:10.1097/MD.0000000000001286
[22] Zhuang CL, Ye XZ, Zhang CJ et al. Early versus traditional post-operative oral feeding in patients undergoing elective colorec-tal surgery: a meta-analysis of randomized clinical trials. DigSurg 2013; 30: 225–232. doi:10.1159/000353136
[23] Boelens PG, Heesakkers FF, Luyer MD et al. Reduction of post-operative ileus by early enteral nutrition in patients under-going major rectal surgery: prospective, randomized, con-trolled trial. Ann Surg 2014; 259: 649–655. doi:10.1097/SLA.0000000000000288
[24] Shum NF, Choi HK, Mak JC et al. Randomized clinical trial ofchewing gum after laparoscopic colorectal resection. BrJ Surg 2016; 103: 1447–1452. doi:10.1002/bjs.10277
[25] Topcu SY, Oztekin SD. Effect of gum chewing on reducingpostoperative ileus and recovery after colorectal surgery: Arandomised controlled trial. Complement Ther Clin Pract2016; 23: 21–25. doi:10.1016/j.ctcp.2016.02.001
[26] Zhang H, Deng Y‑H, Shuai T et al. Chewing gum for postoper-ative ileus after colorectal surgery: A systematic review ofoverlapping meta-analyses. Chin Nurs Res 2017; 4: 92–104.doi:10.1016/j.cnre.2017.02.001
[27] van den Heijkant TC, Costes LM, van der Lee DG et al. Random-ized clinical trial of the effect of gum chewing on postopera-tive ileus and inflammation in colorectal surgery. Br J Surg2015; 102: 202–211. doi:10.1002/bjs.9691
[28] Lee H, Cho CW, Yoon S et al. Effect of sham feeding with gumchewing on postoperative ileus after liver transplantation-arandomized controlled trial. Clin Transplant 2016; 30: 1501–1507. doi:10.1111/ctr.12849
[29] Atkinson C, Penfold CM, Ness AR et al. Randomized clinical tri-al of postoperative chewing gum versus standard care aftercolorectal resection. Br J Surg 2016; 103: 962–970.doi:10.1002/bjs.10194
[30] Nelson R, Edwards S, Tse B. Prophylactic nasogastric decom-pression after abdominal surgery. Cochrane Database SystRev 2007; (3): CD004929. doi:10.1002/14651858.CD004929.pub3
[31] Traut U, Brugger L, Kunz R et al. Systemic prokinetic pharma-cologic treatment for postoperative adynamic ileus followingabdominal surgery in adults. Cochrane Database Syst Rev2008; (1): CD004930. doi:10.1002/14651858.CD004930.pub3
99izin up2date 2018; 14: 87–102

100
CME-Fortbildung
en G
ebra
uch
heru
nter
gela
den.
Ver
viel
fälti
gung
nur
mit
Zus
timm
ung
des
Ver
lage
s.
[32] Drake TM, Ward AE. Pharmacological management to preventileus in major abdominal surgery: a systematic review andmeta-analysis. J Gastrointest Surg 2016; 20: 1253–1264.doi:10.1007/s11605-016-3140-0
[33] McCarthy G. Impact of intravenous lidocaine infusion on post-operative analgesia and recovery from surgery. Drugs Aging2010; 70: 1149–1163
[34] Wongyingsinn M, Baldini G, Charlebois P et al. Intravenous li-docaine versus thoracic epidural analgesia: a randomized con-trolled trial in patients undergoing laparoscopic colorectal sur-gery using an enhanced recovery program. Reg Anesth PainMed 2011; 36: 241–248. doi:10.1097/AAP.0b013e31820d4362
[35] Gungorduk K, Ozdemir IA, Gungorduk O et al. Effects of coffeeconsumption on gut recovery after surgery of gynecologicalcancer patients: a randomized controlled trial. Am J Obstet Gy-necol 2017; 216: 145.e1–145.e7. doi:10.1016/j.ajog.2016.10.019
[36] Muller SA, Rahbari NN, Schneider F et al. Randomized clinicaltrial on the effect of coffee on postoperative ileus followingelective colectomy. Br J Surg 2012; 99: 1530–1538.doi:10.1002/bjs.8885
[37] Vather R, Josephson R, Jaung R et al. Gastrografin in prolongedpostoperative ileus: a double-blinded randomized controlledtrial. Ann Surg 2015; 262: 23–30. doi:10.1097/SLA.0000000000001062
[38] Biondo S, Miquel J, Espin-Basany E et al. A double-blinded ran-domized clinical study on the therapeutic effect of gastrogra-fin in prolonged postoperative ileus after elective colorectalsurgery. World J Surg 2016; 40: 206–214. doi:10.1007/s00268-015-3260-9
[39] Paulasir S, Kaoutzanis C, Welch KB et al. Nonsteroidal anti-in-flammatory drugs: do they increase the risk of anastomoticleaks following colorectal operations? Dis Colon Rectum2015; 58: 870–877. doi:10.1097/DCR.0000000000000430
[40] Kono T, Shimada M, Yamamoto M et al. Complementary andsynergistic therapeutic effects of compounds found in Kampomedicine: analysis of daikenchuto. Front Pharmacol 2015; 6:159. doi:10.3389/fphar.2015.00159
Meißner T, Reißfelder C. Therapie posto
[41] Yoshikawa K, Shimada M, Wakabayashi G et al. Effect of dai-kenchuto, a traditional Japanese herbal medicine, after totalgastrectomy for gastric cancer: a multicenter, randomized,double-blind, placebo-controlled, phase II trial. J Am Coll Surg2015; 221: 571–578. doi:10.1016/j.jamcollsurg.2015.03.004
[42] Shimada M, Morine Y, Nagano H et al. Effect of TU‑100, a tra-ditional Japanese medicine, administered after hepatic resec-tion in patients with liver cancer: a multi-center, phase III trial(JFMC40-1001). Int J Clin Oncol 2015; 20: 95–104.doi:10.1007/s10147-014-0678-2
[43] Andersen J, Christensen H, Pachler JH et al. Effect of the laxa-tive magnesium oxide on gastrointestinal functional recoveryin fast-track colonic resection: a double-blind, placebo-con-trolled randomized study. Colorectal Dis 2012; 14: 776–782.doi:10.1111/j.1463-1318.2011.02796.x
[44] Hansen CT, Sorensen M, Moller C et al. Effect of laxatives ongastrointestinal functional recovery in fast-track hysterec-tomy: a double-blind, placebo-controlled randomized study.Am J Obstet Gynecol 2007; 196: 311–317
[45] Schulze T, Heidecke CD. Behandlung postoperativer Passa-gestörungen, Cholangitis und Pankreatitis. Chirurg 2015; 86:540–546. doi:10.1007/s00104-015-0004-1
[46] Adamina M, Kehlet H, Tomlinson GA et al. Enhanced recoverypathways optimize health outcomes and resource utilization: ameta-analysis of randomized controlled trials in colorectal sur-gery. Surgery 2011; 149: 830–840. doi:10.1016/j.surg.2010.11.003
[47] Btaiche IF, Chan LN, Pleva M et al. Critical illness, gastrointesti-nal complications, and medication therapy during enteralfeeding in critical ill adult patients. Nutrit Clin Pract 2010; 25:32–49. doi:10.1177/0884533609357565
Bibliografie
perati
DOI https://doi.org/10.1055/s-0043-120030Intensivmedizin up2date 2018; 14: 87–102© Georg Thieme Verlag KG Stuttgart · New YorkISSN 1614-4856
ver Darmpassagestörungen… Intensivmedizin up2date 2018; 14: 87–102
Die
ses
Dok
umen
t wur
de z
um p
ersö
nlic
h

Meißner
Punkte sammeln auf CME.thieme.de
T, Reißfelder C. Ther
Diese Fortbildungseinheit ist 12 Monate online für die Teilnahme verfügbar.Sollten Sie Fragen zur Online-Teilnahme haben, finden Sie unter cme.thieme.de/hilfeeine ausführliche Anleitung. Wir wünschen viel Erfolg beim Beantwortender Fragen!
lage
s.
Unter eref.thieme.de/ZZX9326 oder über den QR-Code kommen Siedirekt zum Artikel zur Eingabe der Antworten.
VNR 2760512018154651749
Die
ses
Dok
umen
t wur
de z
um p
ersö
nlic
hen
Geb
rauc
h he
runt
erge
lade
n. V
ervi
elfä
ltigu
ng n
ur m
it Z
ustim
mun
g de
s V
er
Frage 1
Wie ist der postoperative Ileus definiert?A als ein mechanischer Ileus, der nach abdominalchirurgischen
Eingriffen regelmäßig auftrittB als eine vorübergehende Inhibierung der gastrointestinalen
Motilität nach chirurgischer Intervention aufgrund nicht me-chanischer Ursachen, welche eine ausreichende orale Nah-rungsaufnahme verhindert
C als eine funktionelle Störung der gastrointestinalen Motilität,die vor allem nach der Anlage einer Anastomose auftritt undzur Insuffizienz derselben führt
D als starke, von Erbrechen begleitete postoperative Übelkeitaufgrund der intraoperativen Manipulation am Darm
E als eine postoperative Passagestörung, welche nur durch ei-nen erneuten chirurgischen Eingriff behoben werden kann
Frage 2
Einer der folgenden Aspekt der Pathophysiologie eines postope-rativen Ileus (POI) ist nicht korrekt beschrieben. Welcher?A Das Geschehen ist multifaktoriell bedingt.B Hormonelle und neurogene Ursachen spielen eine wichtige
Rolle.C Die Aktivierung der Entzündungskaskade ist involviert.D Es gibt keine Hinweise auf iatrogene Faktoren.E Ein ausgeglichener Wasser- und Elektrolythaushalt ist ein
protektiver Faktor.
Frage 3
Wie häufig wird ein postoperativer Ileus (POI) in der Praxis beob-achtet?A in 10–30% der FälleB in mindestens 50% der Fälle bei offenen abdominal-chirurgi-
schen EingriffenC in unter 10% der FälleD in 20% der Fälle bei orthopädischen EingriffenE Bei Manipulation des Darms während der OP kommt es in
99% der Fälle zum postoperativen Ileus.
apie postoperativer Darmpassagestörungen… Intensivmedizin up2d
Frage 4
Welches ist kein Risikofaktor für das Auftreten eines postoperati-ven Ileus?A lange OP-ZeitenB präoperativer NikotinabususC präoperativ erhöhtes SerumalbuminlevelD AdipositasE offene Eingriffe
Frage 5
Einer der folgenden Befunde ist kein Symptom eines postopera-tiven Ileus (POI). Welcher?A aufgetriebenes, schmerzhaftes AbdomenB Unfähigkeit, orale Nahrung bei sich zu behaltenC FieberD Übelkeit und ErbrechenE verzögerter Abgang von Winden und Stuhl
Frage 6
Wie wird ein postoperativer Ileus (POI) in erster Linie diagnosti-ziert?A über Kontrastmitteldarstellung der Magen-Darm-PassageB Spiegelbildung im konventionellen RöntgenC Spiegelbildung und Darstellung einer mechanischen Ob-
struktion mittels ComputertomografieD klinischE distendierte, flüssigkeitsgefüllte Darmschlingen in der Abdo-
mensonografie
▶ Weitere Fragen auf der folgenden Seite…
101ate 2018; 14: 87–102

CME-Fortbildung
Punkte sammeln auf CME.thieme.de
Fortsetzung…
. Ver
viel
fälti
gung
nur
mit
Zus
timm
ung
des
Ver
lage
s.
Frage 7
Wie hoch sind bei Vorliegen eines postoperativen Ileus (POI)durchschnittlich die zusätzlichen Kosten für das US-amerikani-sche Gesundheitssystem?A 1,5 Milliarden US-Dollar/JahrB 50Millionen US-Dollar/JahrC 300Millionen Euro/JahrD 10Millionen Euro/JahrE 3Milliarden Britische Pfund/Jahr
Frage 8
Welche ist die Hauptmaßnahme bei dem Management einespostoperativen Ileus (POI)?A die Gabe von OndansetronB die Anlage einer nasogastralen SondeC die Gabe von Gastrografin per osD 3 × tägliche SchwenkeinläufeE angemessene Prävention
102 Meißner T, Reißfelder C. Thera
Frage 9
Welche Maßnahme reduziert das Auftreten eines postoperati-ven Ileus (POI) nicht?A adäquate Schmerztherapie mit OpioidenB die Gabe von AlvimopanC orale Aufnahme von KoffeinD die perioperative Anlage einer EpiduralanalgesieE der Beginn von Mobilisation und oraler Nahrungsaufnahme
am 1. postoperativen Tag
Frage 10
Welches der im Folgenden genannten Medikamente wird beiVorliegen eines postoperativen Ileus (POI) nicht empfohlen?A Lidocain i. v.B ErythromycinC DaikenchutoD NeostigminE nichtsteroidale Antiphlogistika (NSAID)
pie postoperativer Darmpassagestörungen… Intensivmedizin up2date 2018; 14: 87–102
Die
ses
Dok
umen
t wur
de z
um p
ersö
nlic
hen
Geb
rauc
h he
runt
erge
lade
n