Update Radiotherapie beim Kleinzelligen Lungenkarzinom · PDF file- mit kleinem oder zentral...
Transcript of Update Radiotherapie beim Kleinzelligen Lungenkarzinom · PDF file- mit kleinem oder zentral...

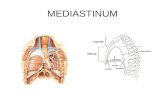
Update Radiotherapie beim Kleinzelligen Lungenkarzinom – SCLC
Frank Zimmermann
Universitätsspital Basel
Klinik für Strahlentherapie und
Radioonkologie

Übersicht
Technik der Strahlentherapie
Strahlentherapie bei Limited Disease
Primärtumor und Lymphknoten: Zeitpunkt, Fraktionierung, Dosis, Zielgebiet
Strahlentherapie bei Extensive Disease
Primärtumor und Lymphknoten: Indikation, Zeitpunkt, Fraktionierung, Dosis
Prophylaktische Strahlentherapie des Hirns
Sonderfälle
Zusammenfassung

Technik der Strahlentherapie

Intensitätsmodulierte und stereotaktische Strahlentherapie

Bildgeführte Strahlentherapie
CT
Kontrolle der Einstellung vor oder während jeder Strahlenbehandlung
Atemgating möglich

Strahlentherapie bei limited disease

Strahlentherapie bei limited disease: Historie
Dosiseskalation bis zur MTD:
3 Zyklen: Cisplatin 3 x 33 mg/qm; Cyclophosphamid 1 x 500 mg/qm;
Etoposid 3 x 80 mg/qm
2 Zyklen: Cisplatin 3 x 33 mg/qm; Etoposid 3 x 80 mg/qm
Phase-I-Studie: 55 Pat.
bei 1 x 2 Gy: 70 Gy in 7 Wochen
bei 2 x 1,5 Gy: 45 Gy in 3 Wochen
Choi et al. JCO 1998; Hügli et al. JCO 2000

Strahlentherapie bei limited disease: Historie
Ergebnis mit 2 x 1,5 Gy bis 45 Gy, initialer RT-Beginn:
1 Zyklus: Cisplatin 3 x 25 mg/qm; Etoposid 3 x 100 mg/qm
5 Zyklen: Cisplatin 1 x 100 mg/qm; Etoposid 3 x 100 mg/qm
Phase-II-Studie: 52 Pat.
32 % 4-Jahresüberleben
38 % Ösophagitis CTC° III-IV
Choi et al. JCO 1998; Hügli et al. JCO 2000

Strahlentherapie bei limited disease: Historie
Dosiseskalation: 61,2 bis 70,0 Gy mit mässiger Toxizität möglich
Phase-II-Studie: 63 Pat., Paclitaxel 1 x 175 mg/qm, Topotecan 5 x 1 mg/qm
– Carboplatin 1 x AUC5, Etoposid 3 x 100 mg/qm
21 % CTC° III / IV Ösophagitis
12 % / 4 % CTC° III / IV Neutropenie
92 % Remission
22,4 Monate medianes Überleben
Bogart et al. IJROBP 2004; Komaki et al. IJROBP 2005

Strahlentherapie bei limited disease: Historie
Dosiseskalation: 50,4 bis 64,8 Gy (5 x 1,8 Gy, akzeleriert innerhalb von 5
Wochen mit Dosisboost), Etoposid 1 x 240 mg/qm, Cisplatin 1 x 60 mg/qm
Phase-I-Studie: 64 Pat.,
MTD: 61,2 Gy; dosislimitierend Ösophagitis
Bogart et al. IJROBP 2004; Komaki et al. IJROBP 2005

Strahlentherapie bei limited disease: Fraktionierung
2 x 1,5 Gy vs. andere, mit kurzer oder langer Therapiedauer
2 x 1,5 Gy in 3 Wochen zu einem frühen Zeitpunkt bestes Konzept
Baymann et al. Lung Cancer 2009

Strahlentherapie bei limited disease: doch 70 Gy ?
Gepoolte Daten der CALGB Studien: 70,0 Gy bei 157 / 200 Pat.
Variable CTx:
Beginn mit 2 Zyklen Topotecan/Paclitaxel; Etoposid/Topotecan/Paclitaxel;
Cisplatin/Irinotecan
Simultan: 2 Zyklen Carboplatin/Etoposid
5-J-Überleben: 20 %
Nebenwirkungen: > 80 % CTC°III Hämatotoxizität; 23 % Ösophagitis
Salama et al. J Thorac Oncol 2013

Strahlentherapie bei limited disease: CONVERT
4 Zyklen Cisplatin / Etoposid
Randomisiert: 547 / 532 Pat.
2 x 1,5 Gy / 45 Gy vs. 1 x 2,0 Gy / 66 Gy
Faivre-Finn et al. BMJ 2016; Groom et al. BJR 2014

Strahlentherapie bei limited disease: Chemotherapie
Chemotherapievergleich: 45 Gy (2 x 1,5 Gy pro Tag) und 3 x 100 mg/qm
Etoposid ; 1 x 80 mg/qm Cisplatin
Stratifizierte Randomisation (ECOG, Remission, Institution): 258 / 281 Pat.
3 Zyklen: 100 mg/qm Etoposid ; 1 x 80 mg/qm Cisplatin
3 Zyklen: 3 x 60 mg/qm Irinotecan ; 1 x 60 mg/qm Cisplatin
Med. OS: 3,2 vs. 2,8 Jahre (HR 1,09, p=0,70)
Kubota et al. Lancet Oncol 2014
NW ° 3-4 Etoposid Irinotecan
Neutropenie 95 % 78 %
Febrile Neutrop. 17 % 14 %
Thrombopenie 21 % 5 %
Anämie 35 % 39 %
Diarrhoe 2 % 13 %
Mortalität < 1 % < 1 %

Strahlentherapie bei limited disease: Chemotherapie
Med. OS:
3,2 vs. 2,8 Jahre (HR 1,09; p=0,70)
5-Jahresüberleben:
35,8 % vs. 33,7 %
Beste Subgruppe (geplant; HR 2,56):
Frauen unter Etoposid
Standard: Platin mit Etoposid
Kuboat et al. Lancet Oncol 2014

Limited disease: Zeitpunkt der Strahlentherapie
Takada et al. JCO 2002
4 Zyklen
Cisplatin/Etoposid
Aber: 3-wöchiger vs.
4-wöchiger Zyklus

Limited disease: Zeitpunkt der Strahlentherapie
De Ruysscher et al. Ann Oncol 2005

Limited disease: Zeitpunkt der Strahlentherapie
De Ruysscher et al. Ann Oncol 2005
Daten für Konzepte mit Cisplatin: Signifikanter Überlebensvorteil nach 5 Jahren
bei Beginn der Strahlentherapie innerhalb von 30 Tagen nach Beginn der
Chemotherapie

Limited disease: Zeitpunkt der Strahlentherapie
Lu et al. Mol Clin Oncol 2013
Daten für Konzepte mit Cisplatin/Etoposid: Kein signifikanter Überlebensvorteil
nach 5 Jahren bei Beginn der Strahlentherapie innerhalb von 30 Tagen nach
Beginn der Chemotherapie

Limited disease: Zeitpunkt der Strahlentherapie
Pijls-Johannesma et al. Cancer Treat Rev 2007

Limited disease: Zeitpunkt der Strahlentherapie
Initiale Strahlentherapie in Zyklus 1-2 bei
- jungen Patienten
- in gutem AEZ
- mit kleinem oder zentral gelegenen Tumor
Spätere Strahlentherapie (in Zyklus 3-4) bei
- Älteren Patienten
- Patienten mit relevanten Begleiterkrankungen
- Nach Remission (auf das Zielgebiet nach Remission)

Strahlentherapie bei limited disease: Mediastinum
Analyse lokoregionärer Tumorrezidive
Retrospektiv: 227 Pat., Cisplatin, Etoposid; variable RT-Konzepte; nur CT !;
keine elektive Lk-RT
Lokoregionäre Rezidive:16/70 Pat.
2 lokale Rezidive
10 regionale Rezidive
4 kombinierte Rezidive
5 / 7 lokale Rezidivvolumina marginal / ausserhalb
27 / 39 regionale Rezidivvolumina marginal / ausserhalb
Guiliani et al. Radiother Oncol 2012

Strahlentherapie bei limited disease: Mediastinum
Selektive mediastinale Strahlentherapie auf FDG-PET-Basis: nur PET-
positive Lk eingeschlossen (vs. CT-positive Lk)
Prospektiv: 60 Pat.
45 Gy, Carboplatin, Etoposid
3 % isolierte regionale Rezidive vs. 10 % kumulativ (11 % mit CT-Planung*)
Kombinierte PET-CT-Definition ?
Van Loon et al. Radiother Oncol 2010; *De Ruysscher et al. Radiother Oncol 2006

Strahlentherapie bei limited disease: Mediastinum
Selektive vs. komplette mediastinale Strahlentherapie
Bedeutung der FDG-PET-Diagnostik
Retrospektiv: 80 Pat.
54 Gy, Cisplatin/Carboplatin, Etoposid
Ergebnisse nach 3 Jahren
Selektiv Komplett
ÜL 44,6 51,1
PET-Plan 52,1 53,7
Ohne PET-Plan 29,3 56,3
PF-ÜL 24,2 42,8
Kombinierte PET-CT-Definition
Jin Han et al. Jpn J Clin Oncol 2012

Strahlentherapie bei limited disease: Mediastinum
Selektive mediastinale Strahlentherapie auf CT-Basis: Lk > 1 cm kurze Achse
eingeschlossen: Ösophagitis CC° III-IV
Prospektiv: 38 Pat., Cisplatin, Etoposid; randomisiert in 45 vs. 66 Gy
0 % isolierte regionale Rezidive vs. 6,5 % kumulativ
Colaco et al. Lung cancer 2012

Strahlentherapie bei limited disease: Mediastinum
Zielvolumen vor oder nach Chemotherapie
Keine elektive Strahlentherapie
Mit FDG-PET-CT
Prospektiv-randomisiert: 85 Pat.
45 Gy, Cisplatin, Etoposid
28,6 vs. 31,6 % lokoregionale Rezidive
2,4 vs. 2,6 % isolierte regionale Rezidive
Zielvolumen nach 2 Zyklen Chemo mit PET-CT-Definition sicher
Hu et al. Cancer 2012

Strahlentherapie bei extensive disease

Strahlentherapie bei extensive disease: Primärtumor
Rand. Studie: 206 / 210 Pat., 3 Zyklen Cisplatin / Etoposid, bei CR/PR
randomisiert
4 Zyklen PE
1 Zyklus Carboplatin/Etoposid mit RT 2 x 1,5 Gy bis 54 Gy, 2 Zyklen PE
5-J-Überleben: 9,1 vs. 3,7 % (p = 0,041)
Bei CR: prophylaktische Ganzhirn-RT
Jeremic et al. JCO 1999

Strahlentherapie bei extensive disease: Primärtumor
Rand. Studie: 495 Pat., 4-6 Zyklen Platinum / Etoposid, Ganzhirn-RT
bei Remission Randomisation: Thorakal 10 x 3,0 Gy auf Resttumor
Ziel: 1 Jahresüberleben + 10 % (von 27 %)
Ergebnisse: 33 % vs. 28 % 1 Jahresüberleben (p= 0,066)
n.s. s. s.
Slotman et al. Lancet 385, 2015: 36-42

Strahlentherapie bei extensive disease: Primärtumor
1 Jahresüberleben: 33 % vs. 28 % (p = 0,066)
2 Jahresüberleben: 13 % vs. 3 % (p = 0,004)
Slotman et al. Transl Lung Cancer 2015

Strahlentherapie bei extensive disease: Primärtumor
Palma et al. Clin Lung Cancer 2015

Prophylaktische Strahlentherapie des Hirns

Strahlentherapie bei limited disease: Hirn
Retrospektiv SEER: 670 / 7995 Pat.
2-JÜL: 42 % vs. 23 % (p < 0,001)
Patel et al. Ann Oncol 2011

Strahlentherapie bei limited disease: Hirn
Gepoolte Daten der NCCTG-Studien: 459 / 739 Pat.
3-Jahres-Überleben: 18 % vs. 5 %
10 x 2,5 Gy > 15 x 2,0 Gy
Schild et al. Ann Oncol 2012

Prophylaktische Strahlentherapie des Hirns
Metaanalyse: 16 Studien, 1983 Pat.
Bei Tumorremission: 5 % geringere Mortalität (vs. 0 % bei PD/NC)
Limited disease: 4 % geringere Mortalität
Extensive disease: 8 % geringere Mortalität !?
Viani et al. J Bras Pneumol 2012

Prophylaktische Strahlentherapie des Hirns
Viani et al. J Bras Pneumol 2012

Prophylaktische Strahlentherapie des Hirns
Randomisiert, limited disease: 10 x 2,5 Gy vs. 18 x 2,0 Gy/20 x 1,5 Gy b.i.d.
Rezidivrate identisch
geringe Einbussen bei
Kommunikation
Gedächtnis
intellektueller Fähigkeit
Le Péchoux et al. Ann Oncol 2011

Prophylaktische Strahlentherapie des Hirns
Randomisiert, extensive disease: geplante Interim-Analyse 163 / 330 Pat.
Cisplatin/Irinotecan; Carboplatin/Etoposid; Cisplatin/Etoposid
Alle Hirn-MRT vor Beginn der Strahlentherapie
Nosaki et al. Cur Treat Opt Oncol 2015
Mit RT Ohne RT
CR nach CTx 12 % 15 %
1-J-Hirnfiliae 32,4 % 58,0 %
Rezidivtherapie Hirn (Ganzhirn, Stereotaxie) 31,3 % 80,4 %
Rezidivtherapie systemisch 82 / 43 % 89 / 53 %
Medianes Überleben 10,1 Mon 15,1 Mon

Besondere Aspekte

Chirurgie bei limited disease
Nur retrospektive Daten
88 Pat. / 54 Pat.
5-JÜL: zusätzliche Op-Arm 62 % vs. 25 % im Stadium I (vs. 37 % nur Op)
Matched pair Analyse: Op + RCT > RCT alleine
Moderne Chirurgie bei Resttumor ?
Takenaka et al. Lung Cancer 2015; Stish et al. Clin Lung Cancer 2015

Maintenance in extensive disease
Randomisierte Phase-II-Studie (CALGB 30504), nach 4-6 Zyklen
Cisplatin/Carboplatin und Etoposid: 85 / 144 Pat.
Placebo
Sunitinib 37,5 mg/Tag
Medianes PF-ÜL:
3,7 vs. 2,1 Monate (p = 0,02)
Med. ÜL:
9,0 vs. 6,9 Monate (n.s.)
Nebenwirkungen:
19 % vs. 10 % Fatigue
ca. 20 % vs. 0 % Hämatotoxizität
Ready et al. JCO 2015

Chemotherapie in very extensive disease
2 Studien mit 1. Line gegen BSC (Ifosfamid; ACNU): + 2,5 Monate median
3 Studien bei Tumorrezidiv gegen BSC (MTX-Doxorubicin / Topotecan /
Picoplatin): + 2 Monate median (nach 4 Zyklen CTx, für Frauen)
Aber: alte Studien, unter optimaler Begleittherapie keine aktuellen Studien
Alvarez et al. Cochrane 2013; Kokron et al. Onkologie 1982; Spiro et al. BJC 1989; O’Brien JCO 2006

Chemotherapie bei Hirnfiliae
3 kleine randomisierte Studien: RT +/- CTx oder CTx +/- RT
Ergebnis:
progressionsfreies Überleben mit kombinierter Therapie besser
Überleben ohne signifikante Unterschiede
Konzept je nach führender Symptomatik
Reveiz et al. Cochrane 2012

Strahlentherapie bei älteren Menschen (> 70 Jahre)
Limited disease: Anteil der Älteren in Studien unter 15 %
Im Vergleich mit Jüngeren bei mediastinaler Strahlentherapie:
Häufiger schwere hämatologische NW (84 % vs. 61 %, p < 0,01)
Mehr fatale NW (10 % vs. 1 %, p = 0,01)
Schlechteres 5-J-Überleben ( 16 % vs. 22 %, p = 0,05)
Ähnliches rezidivfreies 5-J-Überleben (16 % vs. 19 %, p = 0,18)
Bayman et al. Lung Cancer 2010; Yuen et al. Cancer 2000

Strahlentherapie bei älteren Menschen (> 75 Jahre)
Prophylaktische Hirn-RT (> 70 Jahre)
Medianes ÜL: 12,0 vs. 7,6 Monate
3-JÜL: 13,2 vs. 3,1 %
Aber: CTC°III NW 71,4 vs. 47,5 %
Rule et al. J Ger Oncol 2015; Eaton et al. Cancer 2013

Strahlentherapie bei älteren Menschen (> 75 Jahre)
Konventionell fraktionierte Strahlentherapie des Primärtumors nach
Remission (im 3.-4. Zyklus) bei nur 4 Zyklen CTx
Prophylaktische Hirn-RT bei Remission
Zumindest bis 80. Lebensjahr
Bayman et al. Lung Cancer 2010; Yuen et al. Cancer 2000; Rule et al. J Ger Oncol 2015

Zusammenfassung
Die Strahlentherapie des Primärtumors sollte bei jedem kleinzelligen
Lungenkarzinom bedacht werden
- Bei limited disease früh, kurze Therapiezeit, 2 x 1,5 Gy/Tag bis 45 Gy
- Bei extensive disease nach 4 Zyklen bei Remission der Metastasen
- Vor allem bei geringer extrathorakaler Tumorlast
- Bei jüngeren Patienten in gutem AEZ, kurze Therapiezeit (z.B. 30 Gy)
Die prophylaktische Hirnbestrahlung gehört zur Therapie des kleinzelligen
Lungenkarzinoms:
- Bei Limited disease (10 x 2,5 Gy)
- Fraglich bei Extensive disease (MRT-Diagnostik)
Die Operation des Primärtumors im Stadium I im Einzelfall, ersetzt nicht die
Strahlentherapie des Mediastinums
Jeremic et al. IJROBP 2014