Wärmeleiähigkeit Kenneigenschaen von Reinstoffen · Elektronenpaarbindung (Atombindung/...
Transcript of Wärmeleiähigkeit Kenneigenschaen von Reinstoffen · Elektronenpaarbindung (Atombindung/...

1
2
3
4
Kenneigenscha�en von Reinstoffen
Aggregatzustand
Stoffgemische
Des�lla�on
charakteris�sche Eigenscha�en eines Reinstoffes
z.B.: Dichte (Masse/Volumen)
Löslichkeit
Wärmelei�ähigkeit
Aggregatzustand bei Raumtemperatur
Geruch
Geschmack
Farbe/Aussehen
Siedetemperatur
Schmelztemperatur
elektrische Lei�ähigkeit
...
flüssig (l)
Teilchen bewegen sich aneinander vorbei,mi�elstarke Anziehungs-krä�e zwischen den Teilchen
fest (s)
Teilchen schwingen am Gi�erplatz,starke Anziehungskrä�e zwischen den Teilchen
gasförmig (g)
Teilchen bewegen sich frei; schwache Anziehungskrä�e zwischen den Teilchen
heterogene Stoffgemische:
homogene Stoffgemische:
mehrere Phasen unterscheidbar, Teilchen in Grüppchen zusammenz.B. Suspension (Feststoff in Flüssigkeit), Emulsion (zwei Flüssigkeiten)
einheitliches Aussehen, nur eine Phase, Teilchen gleichmäßig miteinander vermischtz.B. Lösung (Feststoff, Flüssigkeit oder Gas in einer Flüssigkeit)
Trennverfahren für Stoffe mit unterschiedlichen Siedetemperaturen
Stoffgemisch wird langsam erhitzt bis die Siedetemperatur des einen Stoffes erreicht wird, dieser verdamp� und steigt auf. Am Kühler kondensiert der Stoff wieder und trop� in die Vorlage
a: Kolben mit Stoffgemisch b: Thermometer, c: Kühler d: Vorlage mit Des�llat
sieden/verdampfenkondensieren
resublimierensublimieren
sch
mel
zen
erst
arre
n
a
b
c
d
Gemische aus zwei oder mehr Reinstoffen; mehrere Sorten kleinster Teilchen
Phase: Bereich mit einheitlichen Eigenscha�en

5
6
7
8
Reinstoffe
Chemische Reak�on
exotherme Reak�on
endotherme Reak�on
Defini�on: Reak�on, bei der Energie frei wird
Kennzeichen: Umgebung erwärmt sich, Lichterscheinungen
Defini�on: Reak�on, bei der Energie gebunden wird
Kennzeichen: Umgebung kühlt ab, Reak�on bricht ohne Energiezufuhr ab
Stoff mit spezifischen Eigenscha�en,nur eine Sorte kleinster Teilchen
Atome Moleküle aus gleichar�gen
Atomen
Element
Moleküle aus verschiedenen
Atomsorten
Salze: Kristalle aus Anionen
und Ka�onen
Reinstoff
Verbindung
Stoffumwandlung (Änderung der Eigenscha�en)
Umgruppierung von AtomenAuf Teilchenebene:
(Aufnahme oder Abgabe von innererEnergie)
Energieumsatz
Eduktemetastabil
Produktestabil
Reaktionsverlauf
Energie
Übergangszustandinstabil
ReaktionsenergieEi
AktivierungsenergieEA
Eduktestabil
Reaktionsverlauf
Energie
Übergangszustandinstabil
ReaktionsenergieEi
AktivierungsenergieEA
Produktemetastabil

9
10
11
12
Katalysator
Aufstellen von Reak�onsgleichungen
Aufstellen von Formeln
Benennung von einfachen Verbindungen
Stoff, der eine Reak�on beschleunigt, indem er die
Ak�vierungsenergie senkt
wird bei der Reak�on selbst nicht verbraucht
1. Elemente links/unten zuerst
2. Wer�gkeit der Elemente bes�mmen (PSE)
3. Kürzen möglich?
4. Überkreuzregel
Bsp.: Verbindung aus Kohlenstoff und Sauerstoff
C O2
Wer�gkeit IV II
gekürzt „II“ „I“
1. Element mit unverändertem dt. Namen2. Element abgeleitet vom lat./griech. Namen, Endung „-id“
Hauptgruppen-elemente mit abweichender
Wer�gkeit
Nur
Hauptgruppen
-elemente
oderNebengruppen
-elemente
II I
MgCl2
Magnesiumchlorid
VI II
S O3
Schwefeltrioxid
IV II
MnO2
Mangan(IV)oxid
1. Wortgleichung in Elementsymbole und Formeln übersetzen
3. Atomanzahlen jedes Elements auf beiden Seiten des Reak�onspfeils prüfen
wenn nö�g Atomanzahlen durch geeignete Koeffizienten ausgleichen (Gesetz der Massenerhaltung)
4.
2. bei Verbindungen: Wer�gkeiten der Elemente beachten
bei Elementen: Index 2 bei H O N Cl Br I F ergänzen

13
14
15
16
Atombau
Elemen�nforma�onen im PSE
Okte�regel
Salzbildung
Schalenmodell
Ener
gie
-maximal mögliche e -Anzahl
2pro Schale: 2n
+ 0Atomkern: p und n Masse des Atoms (in u)
-Atomhülle: Schalen mit e
Energiestufenmodell
C12
6
Nukleonenzahl(Anzahl Protonen + Neutronen)
Kernladungszahl = Ordnungszahl (Anzahl Protonen bzw. Elektronen)
Hauptgruppennummer: Anzahl der Valenzelektronen
Isotope:
Periode: Anzahl der besetzten Schalen (Energiestufen)
Atome mit gleicher Protonenzahl, aber unterschiedlicher Neutronenzahl
aus Metall und Nichtmetall
->
entstehendes Nichtmetallanion: entstehendes Metallka�on:
nega�v geladenposi�v geladen
beide erreichen durch Elektronenübertragung die Edelgaskonfigura�on
Ionenbindung:
Ionengi�er:
elektrosta�sche Anziehung zwischen Anionen und Ka�onen
dreidimensionale Anordnung von Anionen und Ka�onen
Atomkern
Valenzelektron (äußerste Energiestufe)max. 8
-
++
--
--
-
-
---
-
-2. Energiestufe (Schale)
1. Energiestufe (Schale)
3. Energiestufe (Schale)= Valenzschale
-
- - - - - - - -
- - 1. Energiestufe
2. Energiestufe
3. Energiestufe
Edelgaskonfigura�on:
Ausnahme Duple� (2 Elektronen):
Nichtmetalle sind Elektronenakzeptoren Metalle sind Elektronendonatoren
-Atome haben das Bestreben 8 e (Okte�) in der äußersten Schale (höchsten Energiestufe) zu erreichen
Wasserstoff, HeliumLithium, Beryllium

17
18
19
20
Eigenscha�en von Salzen
Molekulare Stoffe und
Elektronenpaarbindung (Atombindung/ kovalente Bindung)
Valenzstrichformeln
Metallbindungsmodell
meist hohe Schmelz- und Siedetemperaturen
als Feststoffe Nichtleiter
leiten in Wasser gelöst oder als Schmelze den elektrischen Strom
hart und sprödeDRUCK
-+
-+
-+
- +
-
-+
-+
-+
- +
- + +
-+
-+
-+
- +
- +
Ab
sto
ßu
ng
Jeder Valenzstrich entspricht einem bindenden oder freien Elektronenpaar der äußersten Schale
Regeln:
1. Die Summe der Valenzelektronen der freien Atome und im Molekül ist gleich
Jedes Atom im Molekül besitzt die Edelgaskonfigura�on2.
3. Jeder Bindungspartner liefert die Häl�e der bindenden Elektronen
4.
Die Bindigkeit entspricht der Zahl der zur Edelgaskonfig. benö�gten Elektronen
5. Kohlenstoff, S�ckstoff und Sauerstoff (sowie Elemente ab der 3. Periode) können Mehrfachbindungen bilden
Metallatome geben ihre VE ab und werden zu Ka�onen (Metall-Atomrümpfen) mit der Edelgaskonfigura�on.
Die abgegebenen Elektronen bilden in den Lücken zwischen den Metallatomrümpfen ein Elektronengas aus delokalisierten frei beweglichen, gleichmäßig verteilten Elektronen.
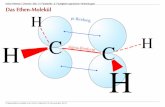
neutrale Teilchen aus Nichtmetall-Atomen
Kohlenstoff, S�ckstoff und Sauerstoff können neben Einfach-
bindungen auch Mehrfachbindungen (Doppel-, evtl. Dreifach-
bindungen) knüpfen
Zahl der Bindungen (= Bindigkeit) entspricht den für die Edelgas-
konfigura�on benö�gten Elektronen (= Wer�gkeit)
+ + + ++ + + +
+ + + ++ + + +
- - - -- - - -
- - - -----
Atomrumpf
Elektronengas
bindende Elektronenpaare: zur Häl�e von jedem Bindungspartner -im Überlappungsbereich der e -Hüllen
zwischen den Atomkernen
jedes Atom im Molekül erreicht durch
bindende und freie Elektronen die
Edelgaskonfigura�on

brennbar
21
22
23
24
Eigenscha�en von Metallen
Sicherheit
Au�au Protokoll
Gas-Nachweise
dichteste Kugelpackungen
das frei bewegliche Elektronengas
wandert im elektrischen Feld
weitere: Farbe, Glanz, thermische Lei�ähigkeit
Elektrische Lei�ähigkeit
Mechanisch verformbare Feststoffe
-
Schichten können durch äußere Kra�-
einwirkung leicht gegeneinander ver-
schoben werden, das Elektronengas
fixiert die neue Lage
Gefahrensymbole
umwelt-gefährlich
explosions-gefährlich
brand-fördernd
gi�ig reizend ätzend gesundheits-schädlich
Chemikalienabfälle werden nach Anweisung des Lehrers entsorgt
Entsorgung
Keine Speisen und Getränke
Fluchtwege freihalten
Zuhören Denken Handeln!
allg. Verhaltensregeln
Schutzbrille und Labormantel tragen
sachliche Sprache, Formulierung im Präsens-Passiv (Es wird…, Man nimmt…)
Gliederung
Durchführung:Zur Wiederholung des Versuchs wesentliche Arbeitsan-weisungen, verwendete Geräte und Chemikalien
Beobachtung:Beschreibung der wahrgenommenen Veränderungen, Messwerte
Schlussfolgerung/Erklärung:Erklärung der Beobachtungen, Ableiten von Schluss-folgerungen, Auswertung der Messwerte
weißer Niederschlag beim Einleiten des Gases in Kalkwasser
Kohlenstoffdioxidnachweis
Glimmspanprobe Nachweis von Sauerstoff
Aufglühen eines glimmenden Holz-spans im Gas
Knallgasprobe Nachweis von Wasserstoff
hörbarer Knall bei Entzünden des Gases
- +

25
26
27
28
Formeln wich�ger Elemente und Verbindungen
Formeln wich�ger Basen
und zugehöriger Ionen
Formeln wich�ger Säuren
und zugehöriger Ionen
Chemisches Rechnen I
Stoffmenge (n) 231mol = 6,022 10 Teilchen
n = mM
molare Masse (M) entspricht Massenzahl des PSE gEinheit /mol
molares Volumen (V )m abhängig von Temperatur und Druck lEinheit /mol
n = VVm
für Feststoffe/ Flüssigkeiten verschieden
lfür Gase gleich: 24 /mol
bei 20°C, 1013 hPa
Salzsäure
Schwefelsäure
Schweflige Säure
Salpetersäure
Salpetrige Säure
Phosphorsäure
Kohlensäure
Essigsäure
HCl (aq)
H SO2 4
H SO2 3
HNO3
HNO2
H PO3 4
H CO2 3
CH COOH3
-Cl2-
SO4
2-SO3
-NO3
-NO2
3-PO4
2-CO3
-CH COO3
Chlorid
Sulfat
Sulfit
Nitrat
Nitrit
Phosphat
Carbonat
Acetat
Hydroxid
Ammonium
-OH+
NH4
Natronlauge
Kalilauge
Calciumhydroxid
Bariumhydroxid
Ammoniak
NaOH
KOH
Ca(OH)2
Ba(OH)2
NH3
(Kalkwasser)
(Barytwasser)
Wasserstoff
Sauerstoff
S�ckstoff
Chlor
Brom
Iod
Fluor
H2
O2
N2
Cl2
Br2
I2
F2
Methan
Wasserstoffperoxid
Schwefelwasserstoff
Braunstein
Kaliumpermanganat
Kaliumdichromat
Silbernitrat
CH4
H O2 2
H S2
MnO2
KMnO4
K Cr O2 2 7
AgNO3

29
30
31
Chemisches Rechnen II
Fällungsreak�onen
Avogadro-Konstante (N )A
Stoffmenge in einem bes�mmten
Volumen eines Lösungsmi�elsmolEinheit /l
n = NNA
Teilchenzahl (N)
Dichte () Masse pro Volumen kgEinheit /l
Konzentra�on (c)
236,022 10 Teilchen pro mol
n = cV
Qualita�ve Analy�k
32
Iden�fizierung von Ionen oder Molekülen mit Hilfe von
bes�mmten Nachweisreagenzien
nega�ve
Blindprobe:
Durchführung des Nachweises ohne die
nachzuweisende Substanz
nega�ves Ergebnis zeigt Sauberkeit der
Reagenzien
Flammenfärbung+
-
-I II
Methode zur Iden�fizierung von Metall-Ionen
Na: gelb
Grundlage:
Ein Valenzelektron des Metalls
nimmt Energie der Bunsen-
brennerflamme auf und wird
auf ein höheres Energieniveau
angehoben
I
Beim Zurückfallen in den Grundzustand gibt das Elektron die aufgenommene Energie in Form von Licht wieder ab
II
posi�ve
Blindprobe:
Durchführung des Nachweises mit der
nachzuweisenden Substanz
posi�ves Ergebnis zeigt Funk�onsfähig-
keit der Reagenzien
Ca: ziegelrot Li: karminrot
Ba: fahlgrün
K: viole�
Das Anion eines leicht löslichen Salzes verbindet sich mit
dem Ka�on eines anderen leicht löslichen Salzes zu einem
schwer löslichen Salz und fällt als Niederschlag aus
Beispiele:
* ermöglicht Unterscheidung von NS mit Carbonat-Ionen (löst sich bei Anwesenheit von Säure auf)
*Halogenid-Ion + AgNO + Säure3 weißer NS = AgCl
fahlgelber NS = AgBr
weißer NS
weißer NS
gelber NS = AgI
weißer NS
*Barium-Ion + Na SO + Säure2 4
Calcium-Ion + Na CO2 3
Carbonat-Ion + CaCl / BaCl2 2

33
34
35
Dipol
Elektronenpaarbindung bei der die bindenden Elektronen
zum elektronnega�veren Bindungspartner verschoben sind.
(Kennzeichnung durch Par�alladungen)
Elektronega�vität (EN)
polare Atombindung
= polares Molekül
ungeladenes Molekül mit polaren Atombindungen ohne
symmetrischen Molekülbau36
VSEPR
Elektronenpaarabstoßungsmodell
1.
2.
3.
Elektronenpaare stoßen sich auf Grund ihrer nega�ven
Ladung gegensei�g ab und ordnen sich deshalb mit größt-
möglichem Abstand zueinander an
Nichtbindende Elektronenpaare benö�gen mehr Raum als
bindende Elektronenpaare
Mehrfachbindungen zählen bei der Bes�mmung des räumlichen
Baus wie eine Bindunglinear 180°
tetraedrisch109,5°
pyramidal 107°
gewinkelt 105°
gewinkelt <120°
trigonal-planar120°
Maß für die Fähigkeit eines Atoms die Elektronen einer
Elektronenpaarbindung zu sich zu ziehen
EN ist abhängig von Atomgröße und Kernladung
B C
H
Li
Na
K
Be
Mg
Ca
Al Si
Ga Ge
N
P
As
O
S
Se
F
Cl
Br
He
Ne
Ar
Kr
H - Br
EN: 2,2 EN: 2,96
nega�ve Par�alladung
posi�vePar�alladung
keine Dipol-Moleküle
H - C - H- H
-
H
Cl - Cl
H - Cl
Dipol-Moleküle
OH H
- - H - C - Cl- H
-
H

Säuren und
saure Lösungen
37
38
39
ZusammenhangZMK - Stoffeigenscha�en
Orbital
40
Bes�mmung der Zwischenmolekularen Krä�e
Je stärker die ZMK zwischen den Teilchen
eines Stoffes sind, desto höher ist die Siede-
temperatur dieses Stoffes
Gleiches gilt für die Schmelztemperatur
Siedetemperatur :
Hydrata�on: Umhüllung von Ionen mit den Dipolmolekülen
des Wassers aufgrund elektrosta�scher Wechsel-
wirkung (Dipol-Ionen-Wechselwirkung)
Die Wasserhülle wird als Hydrathülle bezeichnet
Löslichkeit: „Gleiches löst sich gut in Gleichem“
polare Stoffe lösen sich gut in polaren LM
unpolare Stoffe lösen sich gut in unpolaren
Lösungsmi�eln
Aufenthaltsraum für Elektronen
Jedes Orbital kann mit maximal2 Elektronen besetzt sein
z.B. 2. Energiestufe
bis zu 8 Valenzelektronen in 4 Orbitalen:
1s-Orbital + 3p-Orbitalep -Orbitaly
p -Orbitalx
p -OrbitalzAtomorbital (s-Orbital)
MolekülorbitalDurch Überlappung von 2 Atomorbitalen verschiedener Atome entsteht ein Molekül-orbital mit einem bindenden Elektronenpaar
Dipol
nein ja
stark pos. polarisiertes H-Atom?Van-der-WaalsKrä�e
Dipol-DipolWechselwirkungen
abhängig von
Stärke
nein
H-Brücken
ja
OberflächeAtommasse EN Anzahl
Säuren = Protonendonatoren+= Stoffe, die Protonen (H ) abgegeben können Säuren
Molekülbau:
Teilchen besitzen mindestens ein H-Atom, das über eine stark
polare Elektronenpaarbindung (an ein O-, Cl-, F- oder Br-Atom)
gebunden ist
+Saure Lösungen = wässrige Lösungen, die Oxoniumionen (H O (aq)) 3
enthaltenSaure Lösungen = + -es gilt n(H O ) > n(OH )3Saure Lösungen =

Indikatorenund
pH-Wert
41
42
43
Ampholyte
Protolyseund
Neutralisa�on
44
Basenund
alkalische Lösungen
Basen = Protonenakzeptoren+= Stoffe, die Protonen (H ) aufnehmen können Säuren
Molekülbau:
Teilchen besitzen mindestens ein freies Elektronenpaar, das sie
zur Bindung des Protons zur Verfügung stellen
Alkalische Lösungen/ Laugen = wässrige Lösungen, die Hydroxid- -Ionen (OH (aq)) enthaltenAlkalische Lösungen/ Laugen =
+ -es gilt n(H O ) < n(OH )3Alkalische Lösungen/ Laugen =
Molekülbau:
Teilchen besitzen mindestens ein H-Atom, das über eine stark
polare Elektronenpaarbindung (an ein O-, Cl-, F- oder Br-Atom)
gebunden ist und ein freies Elektronenpaar, das sie zur Bindung
des Protons zur Verfügung stellen
Stoffe, die als Base und Säure reagieren können
Beispiele: H O 2
-HSO4
Säure-Base-Reak�on = Protonenübergang+ein Proton (H ) wird von einem Säureteilchen auf ein Baseteilchen
übertragen, dabei entsteht aus der Säure ein korrespondierendes
Baseteilchen und aus der Base ein korrespondierendes Säure-
teilchen - +| |HS + B S + HB
korrespondierende Säure-Base-Paare
Sonderform: Neutralisa�ons-Reak�on
Sonderform: exotherme Reak�on einer sauren mit einer
alkalischen Lösung, bei der ein Salz entstehtSonderform: + - - +
X + OH + Y + H O XY + 2H O3 2(aq)}
Lauge
}
saure Lösung Salz Wasser
+ -Indikatoren = Stoffe, die je nach Anwesenheit von H O - oder OH -3
Indikatoren = Ionen ihre Farbe verändern
Beispiele: Indikator
Lackmus
Phenolphtalein
Bromthymolblau
sauer
rot
farblos
gelb
neutral
viole�
farblos
grün
alkalisch
blau
pink
blau
Universalindikator = Mischindikator, lässt eine Bes�mmung des
pH-Wertes zu (zeigt großes Farbspektrum)Universalindikator =
+pH-Wert = Maß für die Konzentra�on der H O -Ionen in der Lösung 3
+pH = log c(H O )10 3pH-Wert =
Verdünnen auf das 10-fache bedeutet pH + 1 pH-Wert =
0 7 14<<sauer neutral alkalisch

Aufstellenvon
Redoxgleichungen
45
46
47
Redoxreak�onen
Oxida�onszahlen
48
Titra�on
Maßanalyse zur Bes�mmung der Konzentra�on einer
unbekannten sauren/ alkalischen Lösung
Au�au:Büre�e mit
Maßlösung bekannter Konzentra�on
Probenlösung unbekannter Konzentra�on
Am Äquivalenzpunkt (= Umschlag der Indikatorfarbe) gilt+ -n(H O ) = n(OH )3
mit Indikator
Ermi�eln der Redoxpaare und der Oxida�onszahlen
Formulieren der Ox.-/Red.-Teilgleichungen
(Atombilanz beachten!) incl. Elektronenabgabe/ -aufnahme
+Vorhandene Ladungen mit H O -Ionen (saures Milieu) 3
-oder OH -Ionen (basisches Milieu) ausgleichen
Ausgleichen der Atombilanz mit H O2
Mul�plizieren der Teilgleichungen
Addi�on der Teilgleichungen zur Redoxgleichung
1.
2.
3.
4.
5.
6.
(Atombilanz beachten!) incl. Elektronenabgabe/ -aufnahme
-oder OH -Ionen (basisches Milieu) ausgleichen
Elektronenübertragungsreak�onen
bestehen aus Elektronenabgabe und Elektronenaufnahme
Oxida�on = Abgabe von Elektronen
(Oxida�onszahl steigt)
Oxida�onsmi�el
Elektronenakzeptor
Reduk�on = Aufnahme von Elektronen
(Oxida�onszahl sinkt)
Reduk�onsmi�el
Elektronendonator
Teilchen ist