700 Thermodynamik 710 Temperatur 720 Wärme und Energie ...Für ideales Gas...
Transcript of 700 Thermodynamik 710 Temperatur 720 Wärme und Energie ...Für ideales Gas...
-
700 Thermodynamik
710 Temperatur720 Wärme und Energie730 Chemische Reaktionen740 Wärmetransport und Transportphänomene
-
um was geht es?
Eine neue Grösse: Die Temperatur TVerhalten der Materie als Funktion der
TemperaturEnergieumwandlungNoch eine neue Grösse: Entropie SChemische SystemeTransportphänomene:
Diffusionsgleichung
-
711 thermische Ausdehnung von Gasen
-
711 Ziele
• Temperatur mikroskopisch erklären können
• Annahmen für ein ideales Gas erklären können
• Ideales Gasgesetz anwenden können
-
711 Theorie
Druck
Impulsübertrag durch Stösse ``harter Teilchen´´
dAdF
p x
x
px
-
711 Theorie
Druck
Impulsübertrag durch Stösse ``harter Teilchen´´
dAdF
p x
x
px
dtdv
mdtmvd
F xxx 2)2(
-
711 Theorie
Druck
Impulsübertrag durch Stösse ``harter Teilchen´´
vx = ?
x
px
dtdv
mdtmvd
F xxx 2)2(
-
711 Theorie
vx = ?
Geschwindigkeitsverteilung f(v): Anz. Teilchen dN im Intervall v + dv:px
( )dN N f v dv
-
711 Theorie
vx = ?
Normierung von f(v):
px( ) 1f v dv
-
711 Theorie
vx = ?
Erwartungswert für v2:
px
2 2
0
( )v v f v dv
-
711 Theorie
vx = ?
Für ideales Gas Maxwell-Boltzmann-Verteilung:
Neue Grösse: Temperatur T
[T] = Kelvin K
px
23/22 24( )
2
mvkTmf v v e
kT
-
23/22 24( )
2
mvkTmf v v e
kT
0
0.0005
0.001
0.0015
0.002
0.0025
0 500 1000 1500 2000 2500
Reihe1Reihe2Reihe3Reihe4Reihe5
T= 2000 K
T= 273 K
-
711 Theorie
Erwartungswert für v2:
2322 2 2 2 2
0 0
4( )2
mvkTmv v f v dv v v e dv
kT
-
711 Theorie
Erwartungswert für v2:
2
2
322 2 2 2 2
0 0
32 4 2
0
4( )2
42
mvkT
mvkT
mv v f v dv v v e dvkT
m v e dvkT
-
711 Theorie
Erwartungswert für v2:
2
2
322 2 2 2 2
0 0
3 3 52 2 24 2
0
4( )2
4 4 3 22 2 8
mvkT
mvkT
mv v f v dv v v e dvkT
m m kTv e dvkT kT m
-
711 Theorie
Erwartungswert für v2:
2
2
322 2 2 2 2
0 0
3 3 52 2 24 2
0
3 52 2
4( )2
4 4 3 22 2 8
3 2 2 32
mvkT
mvkT
mv v f v dv v v e dvkT
m m kTv e dvkT kT m
kT kT kTm m m
-
711 Theorie
vx = ?
Erwartungswert für v2:
px 2 2
0
( )v v f v dv
kTmv23
21 2
-
711 Theorie
Zurück zur Frage nach dem Druck: Impuls px = ?
Pro Zeit: Kraft pro Fläche =
Druck p = ?px
dtdv
mdtmvd
F xxx 2)2(
-
711 Theorie
Zurück zur Frage nach dem Druck: Impuls px = ?
Pro Zeit: Kraft pro Fläche =
Druck p = ?px
kTVNp
x
x
dAdFp … ?
-
711 Theorie
Druck p = f(N,V,T)
N = Anz. Teilchen
V = Volumen
T = Temperaturpx
kTVNp
-
711 Theorie
pV = f(N,T)
N = Anz. Teilchen
Chemisch besser Anz. Mol npx
nRTpV R = NA·k (mit NA = Avo-gadrozahl). R = 6.022·1023(mol-1)·1.38·10-23(JK-1) = 8.31 J mol-1K-1.
-
712 thermische Ausdehnung von Flüssigkeiten und
Festkörpern
-
712 Ziele
• thermische Längenausdehnung von Festkörpern berechnen können
• thermische Volumenausdehnung von Festkörpern und Flüssigkeiten berechnen können
• Grundlagen eines Flüssigkeitsthermometers verstehen
-
712 Theorie
Längenausdehnung
Tll
l
-
712 Theorie
Volumenausdehnung
TVV
-
712 Theorie
Für Festkörper
TVV
3
-
712 Aufgaben
Flüssigkeitsthermometer
TVV
h=f(T)
V= …?
-
713 Temperaturabhängigkeit des elektrischen Widerstands
-
713 Ziele
• thermische Änderungen des elektrischen Widerstandes berechnen können
• Grundlagen der elektrischen Temperaturmessung verstehen
-
713 Theorie und Aufgaben
Temperaturabhängige Änderung des elektrischen Widerstandes R:
TRR AlR
A
l
-
713 Theorie und Aufgaben
Temperaturabhängige Änderung des elektrischen Widerstandes R:
TRR AlR
A
l
RdTdR
-
713 Theorie und Aufgaben
Temperaturabhängige Änderung des elektrischen Widerstandes R:
AlR
A
l RdTdR
)(1
1)()( TTeTRTR
-
713 Theorie und Aufgaben
Temperaturabhängige Änderung des elektrischen Widerstandes R
Achtung – a ist nur in einem begrenzten Temperaturbereich konstant!
AlR
A
l
RTdTdR )(
-
721 Wärmekapazität
-
721 Ziele
• Begriff Innere Energie definieren / anhand von Beispielen erklären können
• Temperaturerhöhung bei Wärmezufuhr berechnen können
• Begriff Wärmekapazität definieren und für ideale Gase / Kristalle berechnen können
-
721 Theorie
Innere Energie U: Änderung durch Zufuhr von Wärme oder Arbeit
WQdU
-
721 Theorie
Innere Energie U: Änderung durch Zufuhr von Wärme oder Arbeit
WQdU
0dU
T
p
U(T,p)
-
721 Theorie
Q
Innere Energie U: Änderung durch Zufuhr von Wärme oder Arbeit
WQdU QdU
m
-
721 Theorie
Q
Innere Energie U: Änderung durch Zufuhr von Wärme oder Arbeit
WQdU
xx dTm
Qc
QdU m
-
721 Theorie
Q
Wärmekapazität für ideales Gas
QdU m RTvm 2
321 2
-
721 Theorie
Q
Wärmekapazität für ideales Gas
QdU m
RTvm23
21 2
nTCnRTQ V 23
-
721 Theorie
Q
Äquipartitionstheorem: Befindet sich ein System vieler Teichen im Gleichgewicht, entfällt auf jeden Freiheitsgrad eine Energie von
QdU m
RTE21
kTE21
pro Mol bzw.
pro Teilchen
-
721 Theorie
Q
Wärmekapazität für Kristall (Gesetz von Dulong-Petit):
QdU m
RCV 3
-
721 Theorie
Modellierung eines einfachen Wärmespeichersystems:
Auskühlender Körper
IQ
Q
-
721 Theorie
Modellierung eines einfachen Wärmespeichersystems:
Auskühlender Körper
IQ
QQ
dQ Idt
-
721 Theorie
Modellierung eines einfachen Wärmespeichersystems:
Auskühlender Körper
IQ
Q( )Q u
dQ I k T Tdt
-
721 Theorie
Modellierung eines einfachen Wärmespeichersystems:
Auskühlender Körper
IQ
Q( )Q u
dQ I k T Tdt
0
( )udT k T Tdt mc
-
721 Theorie
Substitution:
IQ
Q0
( )udT k T Tdt mc
uT T
ud d dTT Tdt dt dt
-
721 Theorie
Substitution:
IQ
Q0
( )udT k T Tdt mc
uT T
ud d dTT Tdt dt dt
p
d kdt mc
-
721 Theorie
Separation und Integration:
IQ
Qp
d kdt mc
p
d k dtmc
-
721 Theorie
Separation und Integration
IQ
Qp
d kdt mc
. ln
p
p
d k dtmc
k t constmc
-
721 Theorie
Separation und Integration
IQ
Q
p
d kdt mc
. ln
p
p
d k dtmc
k t constmc
0( ) pk t
mct e
-
722 Phasenübergänge
-
722 Ziele
• Gesetz für reales Gas beschreiben können (Was bedeuten die einzelnen Terme?)
• Bedeutung des kritischen Punkt kennen
• Energie, welche in Phasenumwandlungen steckt, berechnen können
-
722 Theorie
reales Gas: zwischenmolekulare Kräfte spielen eine Rolle
-
722 Theorie
Isothermen
pV nRT
-
722 Theorie
Isothermen “relaes Gas”
( ...)( ...)p V nRT
-
722 Theorie
reales Gas: zwischenmolekulare Kräfte spielen eine Rolle
a: Kohäsionsdruck
b: Kovolumen
nRTnbVVanp
2
2
-
722 Theorie
Steigung der Isothermen: nRTnbV
Vanp
2
2
T const
pV
-
722 Theorie
Steigung der Isothermen:
2
2
2
2( )
anp V nb nRTV
nRT anp VV nb V
...T const
pV
V
-
722 Theorie
Steigung der Isothermen:
2
2
2
2( )
anp V nb nRTV
nRT anp VV nb V
...T const
pV
V
-
722 Theorie
Steigung der Isothermen:
2
2
2
2( )
anp V nb nRTV
nRT anp VV nb V
2
2
T const
pV
nRT anV V nb V
-
722 Theorie
Steigung der Isothermen:
2
2
2
2( )
anp V nb nRTV
nRT anp VV nb V
2
3
2T const
pV
nRT anV V nb V
-
722 Theorie
Steigung der Isothermen:
2
2
2
2( )
anp V nb nRTV
nRT anp VV nb V
2
2 3
2( )
T const
pV
nRT anV nbV V nb V
-
722 Theorie
Steigung der Isothermen: nRTnbV
Vanp
2
2
23
2
)(2
nbVnRT
Van
Vp
constT
-
722 Theorie
Bedingung für den Trippelpunkt:
nRTnbVVanp
2
2
23
2
)(2
nbVnRT
Van
Vp
constT
0Vp
022
V
p
-
722 Theorie
Stoffe ohne und mit Anomalie
Temperatur T
Dru
ck p
Trippelpunkt
festflüssig
gasförmig
Temperatur T
Dru
ck p
Trippelpunkt
festflüssig
gasförmig
-
Quelle: https://de.wikipedia.org/wiki/Phasendiagramm#/media/File:He4_de.svg
-
Quelle: https://commons.wikimedia.org/wiki/File:Phasendiagramm_des_Kohlenstoffs.png
-
Hatziantoniou et al. (2005): Phasenübergänge von Lipiden und Liposomen. UserCom 1/2005, 16-18
-
722 Theorie
Phasenübergänge sind mit Bindungskräften assoziert:
Grössere räumliche Trennung benötigt Energie, bei Kondensation oder Bildung von Festkörpern wird Energie frei
mQL f
mQLv
mLQ V
mLQ f
-
722 Theorie
Das Konzept lässt sich auch auf chemische Umwandlungen anwenden:
Bsp. Brennwert
mLQ V
mLQ f
HmQ
-
723 Zweiter Hauptsatz der Thermodynamik, Entropie
-
723 Ziele
• Entropie als Ordnungsmass verstehen
• thermodynamische Entropie makroskopisch definieren können
• Aus Entropiestrom Leistung berechnen können
-
723 Theorie
Was ist der Unterschied?
-
723 Theorie
Was ist der Unterschied?
(An-) Ordnung
physikalischer Prozess:Diffusion, Wärmeleitung
Diese Prozesse sind gerichtet, sie laufen spontan nur in eine Richtung!
-
723 Theorie
physikalisches Ordnungsmass: Entropie
Dieses Mass lässt sich mikroskopisch (statistisch-mechanisch) aus den Zuständen der einzelnen Teilchen berechnen
Wie die Temperatur lässt sich die Entropie nur für viele Teilchen definieren.
-
723 Theorie
Entropie S: die bei einer bestimmten Temperatur reversibel ausgetauschte Wärme
TQ
dS rev
revQT1
T2
revQ
-
723 Theorie
revQ
Entropie S: die bei einer bestimmten Temperatur reversibel ausgetauschte Wärme
TQ
dS rev
revQT1
T2Für T2 > T1 gilt:
012
12 TQ
TQdSdS revrev
-
723 Theorie
1SI
21 SS II
Oder mit Entropiestrom IS:
Qi
Sii
IT
IdtdS
1
T1
T2
Für T2 > T1 gilt:
2SI
-
723 Theorie
1SI
21 SS II
Oder mit Entropiestrom IS:
Qi
Sii
IT
IdtdS
1
T1
T2
Für T2 > T1 gilt:
2SI
-
723 Theorie
Zusammenhang zwischen Entropie und innerer Energie:
TdSQrev
-
723 Theorie
Zusammenhang zwischen Entropie und innerer Energie:
TdSQrev
dVpdspAdsFW
-
723 Theorie
Zusammenhang zwischen Entropie und innerer Energie:
TdSQrev
dVpdspAdsFW
dVpdSTdU
-
723 Theorie
Zusammenhang zwischen Entropie und innerer Energie:
dVpdSTdU
,...,NVSUT
,...,NSVUp
-
723 Theorie
Zusammenhang zwischen Entropie und innerer Energie:
dVpdSTdU
,...,NVSUT
,...,NSVUp
IntensiveGrössen
ExtensiveGrössen
pV =nRT
Druck p Volumen V
TS =pot.Energie
TemperaturT
Entropie S
-
723 Theorie
Entropiestrom und Leistung:SITdt
dSTP
-
723 Theorie
Entropiestrom und Leistung:SITdt
dSTP
-
723 Aufgaben
Entropie als generelles Ordnungsmass?
k
kk xxS log
-
724 Wärmekraftmaschinen
-
724 Ziele
• Kreisprozesse in einem pV-Diagramm darstellen können (isotherm, isobar, isochor,isentrop)
• Verrichtete Arbeit aus pV-Diagramm herauslesen können
• thermodynamischer Wirkungsgrad definieren und berechnen können
-
724 Theorie
Einfaches Modell einer Wärmekraftmaschine
nicht-zyklisch arbeitend
zyklisch arbeitend, wenn Wärmebad gewechselt wird
T2
V
-
724 Theorie
Einfaches Modell einer Wärmekraftmaschine
nicht-zyklisch arbeitend
zyklisch arbeitend, wenn Wärmebad gewechselt wird
T2
V
dhmgdsFdW
-
724 Theorie
Einfaches Modell einer Wärmekraftmaschine
nicht-zyklisch arbeitend
zyklisch arbeitend, wenn Wärmebad gewechselt wird
T2
V
dVpdhmgdsFdW
-
724 Theorie
Carnotscher Kreisprozess
-
724 Theorie
Isotherme Expansion mit Arbeitsmedium ideales Gas
2
1
1
2
pp
VV
-
724 Theorie
Isotherme Expansion mit Arbeitsmedium ideales Gas
2
1
1
2
pp
VV
0 AAA QWU
-
724 Theorie
Isotherme Expansion mit Arbeitsmedium ideales Gas
2
1
1
2
pp
VV
0 AAA QWU
2
1
2
V
VAA V
dVNkTWQ
-
724 Theorie
Isotherme Expansion mit Arbeitsmedium ideales Gas
2
1
1
2
pp
VV
0 AAA QWU
1
22
2
ln
2
1
VVNkT
VdVNkTWQ
V
VAA
-
724 Theorie
adiabatische Expansion:
dTmcdVpdU
V
-
724 Theorie
adiabatische Expansion:
dTmcdVpdU
V
dVV
NkTdTmcV
-
724 Theorie
adiabatische Expansion:
dVV
NkTdTmcV
2
3
2
1
V
V
T
T
V
VdV
TdT
Nkmc
-
724 Theorie
adiabatische Expansion:
dVV
NkTdTmcV
3
2
1
2 lnln
2
3
2
1
VV
TT
Nkmc
VdV
TdT
Nkmc
V
V
V
T
T
V
-
724 Theorie
adiabatische Expansion:
3
2
1
2 lnlnVV
TT
NkmcV
NkmcV 23
2
323
1
2
1
3
223
1
2
1
2 lnlnln23
VV
TT
VV
TT
TT
-
724 Theorie
Isotherme Kompression:
4
3
3
4
pp
VV
3
41 ln V
VNkTQC
-
724 Theorie
adiabatische Kompression:
23
2
1
4
1
TT
VV
)( 124
TTmcUW
V
D
-
724 Theorie
Bilanz:
DCCB
AAtotal
WWQWWQU
012
TQ
TQ CA
-
724 Theorie
Entropie im Carnotschen Kreisprozess:
DCCB
AAtotal
WWQWWQU
0 TQrev
-
724 Theorie
Entropie im Carnotschen Kreisprozess:
DCCB
AAtotal
WWQWWQU
0 TQrev
T
S
-
724 Theorie
Wirkungsgrad im Carnotschen Kreisprozess:T
S
2
111TT
QQ
QQQ
QW
A
B
A
BA
A
-
724 Theorie
Wirkungsgrad im Carnotschen Kreisprozess (Betrachtung Entropiestrom):
T
S
S
S
S
mech
therm
mech
ITITT
ITP
PP
2
12
2
)(
-
724 Theorie
Anderer Kreisprozess (einfach zur Berechnung der abgegebenen Arbeit (vom Prozess umschlossene Fläche), aber nicht optimaler Wirkungsgrad)
p
V
-
724 Theorie
Anderer Kreisprozess (einfach zur Berechnung der abgegebenen Arbeit (vom Prozess umschlossene Fläche), aber nicht optimaler Wirkungsgrad)
p
V
VpW
-
731 Reaktionsenergie und Enthalpie
-
731 Ziele
• Begriffe exotherme und endotherme Reaktiondefinieren können
• Reaktionsenthalpie für einfache chemische reaktionen berechnen können
• Satz von Hess erklären können
-
731 Theorie
Energien bei chemischer Reaktion
-
731 Theorie
Energien bei chemischer Reaktion
-
731 Theorie
Energien bei chemischer Reaktion
Def. Reaktionsenthalpie
VpUH
-
731 Theorie
Energien bei chemischer Reaktion
Def. Reaktionsenthalpie
VpUH
HUVpUW
12
-
731 Theorie
Berechnung über Standard-Enthalpien
)Reaktanden(
)Produkte(0
0
f
f
H
HH
-
731 Theorie
Berechnung über Standard-Enthalpien
)Reaktanden(
)Produkte(0
0
f
f
H
HH
Bindung
Bindungsenergie kJ/ mol
Bindung
BindungsenergiekJ / mol
Bindung
BindungsenergiekJ / mol
Br-Br 193 C-O 335 I-I 151
C-C 347 Cl-Cl 243 N-H 389
C=C 619 F-F 155 N-N 159
C-H 414 H-Br 364 O-H 463
C-F 485 H-Cl 431 O-O 138
C-N 293 H-H 435 O2 494
-
732 Chemische Reaktionskinetik
-
732 Ziele
• zeitlicher Verlauf von chemischen Reaktionen modellieren und simulieren können
• Reaktionen nullter, erster und zweiter Ordnung beschreiben können
• für einfache Fälle aus chemischer Reaktion kinetische Ordnung bestimmen können
• Reaktionskinetik bei enzymatischen /katalytischen Reaktionen beschreiben können
-
732 Theorie
Reaktionsgeschwindigkeit:
dtdcc
Zeit t
-
732 Theorie
Reaktionsgeschwindigkeit ist temperaturabhängig
Ansatz: Kollisionstheorie
Zeit t
-
732 Theorie
Reaktionsgeschwindigkeit ist temperaturabhängig
Anz
ahl M
olek
üle
Energie
T1
T2
-
732 Theorie
Aktivierungsenergiepo
tent
ielle
Ene
rgie
Reaktionskoordinate
Ea
-
732 Theorie
Kinetik nullter Ordnung
kdt
dcA
-
732 Theorie
Kinetik nullter Ordnung
kdt
dcA
)0()( AA ckttc
Zeit t
c
-
732 Theorie
Kinetik erster Ordnung
AA ck
dtdc
-
732 Theorie
Kinetik erster Ordnung
Zeit t
cA
A ckdt
dc
ktA ectc
0)(
-
732 Theorie
Kinetik zweiter Ordnung
BAA cck
dtdc
2A
A ckdt
dc
-
732 Theorie
Kinetik zweiter Ordnung
2A
A ckdt
dc
AA
A
ccktdtk
cdc 1
2
-
732 Theorie
Kinetik zweiter Ordnung
Zeit t
c
2A
A ckdt
dc
AA
A
ccktdtk
cdc 1
2
1
)0(1)(
AA c
kttc
-
732 Theorie
Weitere Varianten
2BA
A cckdt
dc
A + 2B Produkte
-
732 Theorie
Temperaturabhängigkeit der Reaktionskonstante
pote
ntie
lle E
nerg
ie
Reaktionskoordinate
Ea )/(RTEaeAk
-
732 Theorie
katalytische bzw. enzymatische Reaktionen
dm
m
Vckcv
dtdc
)(
-
732 Theorie
katalytische bzw. enzymatische Reaktionen
dm
m
Vckcv
dtdc
)(
cVk
vVck
cv
dm
m
dm
m
c
)(
lim0
-
732 Theorie
katalytische bzw. enzymatische Reaktionen
dm
m
Vckcv
dtdc
)(
cVk
vVck
cv
dm
m
dm
m
c
)(
lim0
d
m
dm
m
c Vv
Vckcv
)(
lim
-
732 Theorie
katalytische bzw. enzymatische Reaktionen
dm
m
Vckcv
dtdc
)(
cVk
vVck
cv
dm
m
dm
m
c
)(
lim0
d
m
dm
m
c Vv
Vckcv
)(
lim
dcdt
c(t)
c =
c max = vm
vm2
km
-
732 Supplement
Oszillierende Reaktionen: Belousov-Zhabotinskii-Reaktion BZR:
A: BrO3-
X: HBrO2Y: Br-
Z: Ce(IV)
fYZ
QXZXXA
PYXXYA
k
k
k
k
k
5
4
3
2
1
22
-
732 Supplement
Oszillierende Reaktionen: Belousov-Zhabotinskii-Reaktion BZR
fYZ
QXZXXA
PYXXYA
k
k
k
k
k
5
4
3
2
1
22
ZkAXkdtdZ
ZfkXYkAYkdtdY
XkAXkXYkAYkdtdX
53
521
24321 2
-
732 Supplement
Oszillierende Reaktionen: Belousov-Zhabotinskii-Reaktion BZR
ZkAXkdtdZ
ZfkXYkAYkdtdY
XkAXkXYkAYkdtdX
53
521
24321 2
-
732 Supplement
Oszillierende Reaktionen: Belousov-Zhabotinskii-Reaktion BZR
Fig.69. Oszillationsformen in Abhängigkeit des Anfangswertes X0: (a) X0 = 0.2, (b) X0 = 1.5, (c) X0 = 3, (d) X0 = 4; Y0= Z0 = 0, A = 3; k1 = 1 s-1, k2 = 0.5 s-1, k3 = 0.175 s-1, k4 = 0.175 s-1, k5 = 1 s-1, f = 4; Nummerik: Runge-Kutta-Verfahren, t = 10-3 s.
-
741 Wärmeleitung
-
741 Ziele
• Wärmestrom und Temperaturprofile für einfache Geometrien berechnen können
• Die physikalische Bedeutung von Gradient und Divergenz erläutern können
• Die Bedeutung der einzelnen Terme / Teile der Diffusionsgleichung beschreiben können
• Zwischen stationären und transienten Lösungen (der Diffusionsgleichung) unterscheiden können
-
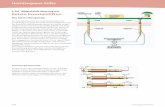
741 Theorie
Wärmestrom / Wärmestromdichte
dtdAdQj
dxdTkj
A
x
IQ
-
741 Theorie
Wärmestrom / Wärmestromdichte für Stab:
dxdTkj
A
x
IQ
xkjdx
kjdT
T
T
1
-
741 Theorie
Wärmestrom / Wärmestromdichte für Stab:
dxdTkj
A
x
IQ
1
1
TT
xkjdx
kjdT
T
T
-
741 Theorie
Wärmefluss in 2D und 3D: Wärmediffusion
Ansatz: Wärmestrombilanz für ein Masseelement
)( dxxIQx )(xIQx
dVdx dy dz
-
741 Theorie
Wärmefluss in 2D und 3D: WärmediffusiondV dx dy dz
)/( dzdydtdQjx
dzdydxxjx )(dzdyxjx )(
-
741 Theorie
Wärmefluss in 2D und 3D: WärmediffusiondV dx dy dz
)/( dzdydtdQjx
dxxj
xjdxxj xxx
)()(
dzdydxxjx )(dzdyxjx )(
-
741 Theorie
Wärmefluss in 2D und 3D: Wärmediffusion
dzdyxjx )(
dxdydzzjz )(
dzdyxjx )(
dzdydxzj
yj
xj
dxdydzzjdzdxdy
yj
dzdydxxj
tQ
zyx
zyx
dzdydxxjx )(
-
741 Theorie
Wärmedichte
dzdydxzj
yj
xj
dxdydzzjdzdxdy
yj
dzdydxxj
tQ
zyx
zyx
)/(/ dzdydxQVQu
-
741 Theorie
Wärmedichte
dzdydxzj
yj
xj
dxdydzzjdzdxdy
yj
dzdydxxj
tQ
zyx
zyx
)/(/ dzdydxQVQu
)( jdivjzj
yj
xj
dtdu zyx
-
741 Theorie
Zusammenhang zwischen Wärmestromdichte und Wärmedichte bzw. Temperaturgradient?
)( jdivjzj
yj
xj
dtdu zyx
-
741 Theorie
Zusammenhang zwischen Wärmestromdichte und Wärmedichte bzw. Temperaturgradient?
Ficksches Gesetz
)( jdivjzj
yj
xj
dtdu zyx
)(ugradkukj
-
741 Theorie
)( jdivjzj
yj
xj
dtdu zyx
)(ugradkukj
xukjx
yukj y z
ukjz
-
741 Theorie
)( jdivjzj
yj
xj
dtdu zyx
)(ugradkukj
xukjx
yukj y z
ukjz
2
2
2
2
2
2
zu
yu
xuk
dtu
-
741 Theorie
2
2
2
2
2
2
zu
yu
xuk
dtu
cTdV
Tcdmdzdydx
dQu
2
2
2
2
2
2
dzT
dyT
dxT
ck
dtdT
-
741 Aufgaben
Lösungen für langer Stab
2
2
2
2
2
2
dzT
dyT
dxT
ck
dtdT
2
2
dxT
ck
dtdT
A
x
IQ
-
741 Aufgaben
Lösungen für langer Stab
txeTtxT 210),(
2
2
2
2
2
2
dzT
dyT
dxT
ck
dtdT
2
2
dxT
ck
dtdT
A
x
IQ
-
741 Aufgaben
Lösungen für langer Stab
Je nach Randbedingungen
transiente Lösungen
stationäre Lösungen
Wärme-Reservoirmit T(l,t)=const.
T(x)
x
T(x,0) T(x,t)
T(x)
x
T(x,0)T(x,t)
Wärme-Reservoirmit T(0,t)=const.
stationärer Fall
T(x)
x
T(x,0)
T(x,t)
Wärme-Reservoirmit T(0,t)=const.
stationärer Fall
Isolation
-
742 Wärmestrahlung
-
742 Ziele
• von einem Körper in Form von Wärmestrahlung abgestrahlte Leistung berechnen können
• Aussagen über Emissions-Spektrum und Temperatur machen können
• die Arten des Wärmetransportes kennen
-
742 Theorie
Möglichkeiten des Wärmetransports:
Konvektion: Wärme wird mit Material transportiert
Wärmeleitung (kunduktiv): Wärme wird als molekulare Schwingung durch Stösse im Medium transportiert
Strahlung (radiativ): ????
-
742 Theorie
Experiment / Beobachtung
Ein heisses Objekt strahlt Wärme ab Wärmestrahlung
Diese Strahlung geht auch durch ein Vakuum hindurch
Strahlung benötigt kein Medium!
?
-
742 Theorie
Experiment / Beobachtung
Ein heisses Objekt strahlt Wärme ab Wärmestrahlung
Diese Strahlung geht auch durch ein Vakuum hindurch
Strahlung benötigt kein Medium!
elektromagnetische Strahlung (Kap. 800 & 900)
E
B
E
B
-
742 Theorie
Experiment / Beobachtung
Ein heisses Objekt strahlt Wärme ab Wärmestrahlung
Diese Strahlung geht auch durch ein Vakuum hindurch
Strahlung benötigt kein Medium!
elektromagnetische Strahlung (Kap. 800 & 900)
-
742 Theorie
Wellenlänge des Strahlungsmaximums (Wiensches Verschiebungsgesetz)
Tb
max
-
742 Theorie
Wellenlänge des Strahlungsmaximums (Wiensches Verschiebungsgesetz)
abgestrahlte Leistung
Tb
max
4ATP
-
742 Theorie
Wellenlänge des Strahlungsmaximums (Wiensches Verschiebungsgesetz)
abgestrahlte Leistung
Emissionszahlen
Tb
max
4ATP
Material Temperatur /°CAluminium poliert 170 0.05Stahl poliert 20 0.16Kupfer oxidiert 20 0.78Wasser 0...100 0.95















![Luftqualität in Brandenburg Jahresbericht 20132013 in Deutschlandals in weiten Teilen mit -0,2 Kelvin (K) etwas zu kühl (nach dem neu eingeführten Referenzzeitraum 19812010)- [2].](https://static.fdokument.com/doc/165x107/6102a12636b94d0ad658c07b/luftqualitt-in-brandenburg-jahresbericht-2013-2013-in-deutschlandals-in-weiten.jpg)

