Große dsDNA-Viren II: Pockenviren und Baculoviren · Klassifikation von Viren nach der Art der...
Transcript of Große dsDNA-Viren II: Pockenviren und Baculoviren · Klassifikation von Viren nach der Art der...

Vorlesung: „Molekulare Virologie“, WS2018/2019
Rainer G. Ulrich
Friedrich-Loeffler-Institut
Institut für neue und neuartige Tierseuchenerreger
D-17493 Greifswald - Insel Riems
Große dsDNA-Viren II:
Pockenviren und Baculoviren

1. EINLEITUNG

(Nichttaxonomische) Klassifizierung von Viren
nach infiziertem Wirt: Bakterien, Pflanzen, Pilze, Tiere, Mensch

DNA-Viren bei Wirbellosen und Wirbeltieren

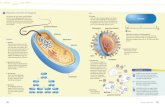
Struktur und Klassifizierung von DNA-Viren

Klassifikation von Viren nach der Art der mRNA-
Synthese (Baltimore-Klassifikation)
Gruppe I: dsDNA. Genomform aller
Lebewesen (Papilloma-,
Polyoma-, Adeno-, Herpes-,
Baculo- und Poxviridae)
Gruppe II: ssDNA. Enthält DNA sowohl
positiver als auch negativer
Polarität (Parvoviridae)
Gruppe III: dsRNA (Reoviridae)
Gruppe IV: (+)ssRNA. Sie wirkt direkt als
mRNA (Picorna-, Toga-, Flavi-,
Calici-, Coronaviridae)
Gruppe V: (-)ssRNA. Sie wirkt als Matrize
zur mRNA-Synthese (Bunya-,
Arena-, Rhabdo-, Paramyxo-,
Orthomyxo-, Filoviridae)
Gruppe VI: (+)ssRNA, die in DNA
zurückgeschrieben und ins
Zellgenom eingebaut wird
(Retroviridae)

2. FAMILIE POXVIRIDAE

Variola
Ramses V.:
Tod (1157 v. Chr.)
infolge von Pocken?

Poxviridae

Poxviridae: Aktuelle Taxonomie

Poxviridae: Phylogenie der Genera

Poxviridae: Phylogenie der Genera

Phylogenie im Genus Orthopoxvirus

Franke et al., 2017
Phylogenie im Genus Orthopoxvirus

Molluscipoxvirus
Vacciniavirus
Ovale, ziegelsteinähnliche Form mit strukturierter Oberfläche
Morphologie der Pockenviruspartikel

Parapoxvirus: bienenkorbartige Anordnung
der Filamente auf der Oberfläche
Avipoxvirus
Morphologie der Pockenviruspartikel

Poxviridae
Virion
Genom
Proteine
im Virion
Replikation
Besonderheiten
oval, ziegelsteinartig, pleomorph,
300 x 200 x 100 nm
lineare dsDNA, kovalent geschlossen
137-360 kbp
>70 Strukturproteine sowie enzymatisch
und regulatorisch aktive Proteine
Cytoplasma („Virus factories“, Virosomen)
größte und komplexeste Viren; resistent
gegen Inaktivierung; erste virale
Erkrankung, die ausgerottet wurde

IMV: intracellular mature virus
IEV: intracellular enveloped virus
CEV: cell-associated enveloped virus
EEV: extracellular enveloped virus
Stadien des Virusassembly

Schematischer Aufbau eines Pockenvirus-Partikels
(Intracellular mature virus “IMV”)

Schematischer Aufbau eines Pockenvirus-Partikels
(Extracellular enveloped virus “EEV”)

Genomstruktur

Vergleich der Genome von Pockenviren

Genomorganisation und Kodierungsstrategie

Replikation der Pockenviren

Replikation der Pockenviren

Enzymatische Partikelkomponenten
a) DNA-abhängige RNA-Polymerase (Transkription)
b) DNA-Polymerase (Replikation)
c) Early Transcription Factor (Promotorerkennung)
d) Capping-Enzymkomplex (Guanyltransferase,
RNA-Triphosphatase, Guanine-7-Methyltransferase)
e) Poly(A)-Polymerase (Polyadenylierung)
f) DNA-Topoisomerase (Sequenzspezifisches Nicking)
g) DNA-Helikase (Replikation)
h) Thymidinkinase (Phosphorylierung)

Pockenviren: Genomorganisation

Pockenviren: Genexpression

Pockenviren: Genexpression

Pockenviren: DNA-Replikation

Pockenvirus-kodierte Immunmodulatoren

• Anzucht: Hühnerei, Zellkultur, Tier
• Antigen-ELISA
• Antikörpernachweis: Immunfluoreszenztest
und Neutralisationstest
• Elektronenmikroskopie
• Genomuntersuchung (RFLP)
• Consensus PCR/Spezies-spezifische PCR
• Genomsequenzierung
Pockenvirus-Diagnostik

CPE auf der Chorioallantoismembran

Chorioallantoismembran mit Hämorrhagien

Orientierende Erstdiagnostik im BSL 3-Labor
(Empfehlung des RKI)
• Inaktivierung für die Elektronenmikroskopie
(10% Formaldehyd)
• Inaktivierung für die PCR
(Guanidiniumchlorid-Puffer, QIAamp kit)
• Asservierung/Versand an BSL 4-Labor

Krankheit durch das
Variolavirus
Variola major
(Variola vera)
Letalität
~ 40 %
Variola minor
(Alstrim Virus)
Letalität
~ 1-2 %
Afrika, Asien,
Europa
Afrika, Südamerika,
Australien

Pocken (Variola vera): Merkmale der Erkrankung
• sehr ansteckende, hochfieberhafte und akut verlaufende
Viruskrankheit
• keine chronischen Verlaufsformen
• keine gesunden Virusausscheider
• hinterlässt eine langandauernde Immunität
• Zyklische Infektionskrankheit
- Infektion über den Respirationstrakt und lokale Vermehrung
- erste Virämie: Leber, Milz, Lymphknoten
- zweite Virämie: Hautmanifestationen

Gewöhnliche Variola major

Pusteln an den
Händen
Flache Läsionen
an den Sohlen

Variola major
Hämorrhagischer Typ

Die 1. Variola-Vakzination
Jenner 1796 Kuhpockenläsionen an der Hand von
Sarah Nelmes (Fall XVI in Jenner’s
Erhebung), von welcher das Material
für die Impfung des James Phipps
(1796) genommen wurde.

Massenimpfkampagne
ab 1958 weltweites Impfprogramm

Variola-Endemiegebiete 1945
Endemische Variola

Variola-Endemiegebiete 1967
Endemisch Importe Übertragung unterbrochen

Letzte Fälle von Variola**
Rahima Banu – 16. Oktober 1975 Variola major-Bangladesh
Ali Maow Maalin – 26. Oktober 1977 Variola minor-Somalia
** zwei Laborinfektionen in UK 1978

1979
Heute im Besitz von Virus:
• CDC in Atlanta, Georgia,
USA
• Russisches Forschungs-
zentrum für Virologie und
Biotechnologie, Koltsovo
bei Novosibirsk, Russland

Eradication of smallpox
• The combination of :
early detection,
isolation of infected individuals,
• surveillance of contacts and
• vaccination policy
has successfully eradicated smallpox.

Voraussetzungen für die Ausrottung
eines Virus
• Menschen sind einziger Wirt des Virus, kein
tierisches Reservoir
• Hohe genetische Stabilität des Erregers,
geringe genetische Divergenz (Virusstämme)
• Praktische diagnostische Werkzeuge
• Impfling ist leicht zu erkennen
• Effektive Möglichkeiten zur Verhinderung der
Übertragung

Vacciniavirus - Impfstoff
• Von Jenner genutztes Originalmaterial war
Kuhpockenvirus.
• Das heute genutzte Virus ist kein Kuhpockenvirus
und kein Variolavirus. Die Herkunft ist unbekannt
(Vacciniavirus).

Origin of vaccinia virus?
• From cowpox virus by passage and mutation.
• From variola virus by passage and mutation.
• By recombination between cowpox and variola viruses.
• A distinct species of orthopoxvirus from an unrecognised host or from a host in which it is no longer endemic. Horsepox?

Impfstoffproduktion (früher)
• Gezüchtet auf der Haut von Kälbern, Schafen, Wasserbüffeln
• Läsionen wurden vor Verkrustung geerntet

Neuer Vacciniavirus-Impfstoff 2003
• in Zellkultur produziertes Lebendvirus
• lyophilisierter Puder
• bessere Verträglichkeit

Normaler Impfverlauf
Tag Beschreibung
0 Impfung
3-4 Ausbildung einer Papel
5-7 Ausbildung eines Bläschen
mit kreisförmigem Erythem
8-10 Ausbildung einer eindeutig
erkennbaren Pustel
10-12 Verschorfung der Pustel
ab 17 Ablösung des Schorfs,
eine Impfnarbe bleibt zurück
Wenn sich keine Pustel bildet, muss die Impfung wiederholt werden

Impfnebenwirkungen • Nebenpocken (Häufigkeit: 1 : 2000) bei Autoinokulation:
Auge (Hornhauttrübung), Nase, Gesicht, Mund, Genital, Rektum
• Ekzema vaccinatum

• Vaccinia generalisata (Häufigkeit: 1 : 100 000)
• Vaccinia progressiva (Häufigkeit in Immunsupprimierten:
1 : 1 Million)
• postvaccinale Enzephalitis (Häufigkeit: 1 : 50 000)
Impfnebenwirkungen

Neue Ansätze zur Bekämpfung
- Modifiziertes Vacciniavirus Ankara (MVA)
- Replikation in Hühnerfibroblasten
- umfangreiche Deletionen und Gen-Rearrangements
- in Säugetierzellen keine Virusreplikation
- Impfungen von 180000 Menschen (keine Impf-
zwischenfälle)
- Vaccinia-Immunglobulin (VIG)
- Cidofovir
Gebrauch bei generalisierter Vaccinia,
Ekzema vaccinatum, progressiver Vaccinia


Andere Humanpathogene Pockenviren:
Orthopoxviren
Kuhpockenvirus
• Erkrankungen bei Haus- und Wildtieren (Zootiere)
• Mensch: gelegentlich zoonotische Erkrankungen mit Pustelbildung,
schwerwiegend bei Immunsuppression
• Reservoir in Nagetieren
• Rind, Mensch, Katze und Zootiere sind Endglieder einer Infektkette
Zunahme humaner Kuhpockenvirusinfektionen (?)
• Einstellung der Impfung (Schwindende Immunität)
• Höhere Aufmerksamkeit behandelnder Ärzte
• Ökologische Veränderungen bei Reservoirnagern?
• Beliebtheit von „Schmuseratten“

Affenpocken
Affenpockenvirus (Monkeypox)
• mit dem Variolavirus eng verwandt
• auch der Mensch ist für Affenpocken
empfänglich
• Affenpocken in weiten Teilen Afrikas
endemisch
• Reservoir in Nagern (Präriehunde) –
Zoonose

Andere Humanpathogene Pockenviren:
Molluscipoxvirus
Molluscum contagiosum (Dellwarzen)
Infektionswege
• Mikroverletzte Haut in Schwimmbädern
• sexueller Kontakt
Vorkommen und Durchseuchung
• weltweit, besonders häufig auf den Inseln des pazifischen Ozeans
Inkubationszeit
• 2-8 Wochen
Symptome und Klinik
• gutartige Viruserkrankung der Haut
• tritt besonders bei Kindern, Erwachsenen unter Cortisontherapie
und Patienten mit Immunschwäche auf
• typische, stecknadelkopfgroße bis erbsengroße Papeln mit
zentraler Eindellung

Tierpathogene Pockenviren I

Tierpathogene Pockenviren II:
Lumpy skin disease-Virus (Genus Capripoxvirus)
– Erstbeschreibung im südlichen Afrika (1929)
– Ausbreitung in den mittleren Osten (2013)
und nach Südeuropa (2015)
FAO „SUSTAINABLE PREVENTION, CONTROL AND
ELIMINATION OF LUMPY SKIN DISEASE”

Vacciniaviren als Vektoren
• Einbau des Fremdgens durch homologe
Rekombination
• Rekombination führt zur Deletion des nicht
essentiellen Thymidinkinasegens
• Einsatz der Pockenviren zur Expression
von Fremdgenen für Vakzineentwicklung
• Rekombinante Pockenvirusvektoren als
Tollwutimpfstoff

3. FAMILIE BACULOVIRIDAE

Familie Baculoviridae
Genus Nucleopolyhedrovirus
Spezies Autographa californica multiple
nucleopolyhedrovirus (AcMNPV)
Genus Granulovirus
Spezies Cydia pomonella Granulovirus (CpGV)
Apfelwickler
Luzernenspanner

Baculoviren: Phylogenie

Figure 4 Phylogeny of the Baculoviridae. The maximum likelihood tree,
based on the alignment of 30 genes, shows the relationships of the 39
species for which a completely annotated genome was available at time
of analyses. Abbreviations are defined in lists of species and related
viruses.
ICTV,
2016
Baculoviren: Phylogenie

- zirkuläre dsDNA; behüllt
- Genom ca. 80 - 180 kbp
- sehr enges Wirtsspektrum (Arthropoden)
- Replikation im Zellkern
- kodieren für ca. 100 - 200 Proteine
Baculoviren

Strukturen der Alpha- und Betabaculoviren

Baculoviren: Genomorganisation
Autographa californica multiple nucleopolyhedrovirus (AcMNPV)


Anwendung von Baculoviren
- Herstellung rekombinanter Proteine
- Gentransfer in Säugerzellen
- Biologische Schädlingsbekämpfung (Obstbau)

- Einfügung eines Fremdgens in eine nicht-essentielle
Region des viralen Baculovirusgenoms via homologe
Rekombination oder Transposon-vermittelte
Integration
- hohe Expressionsrate
- korrekte Faltung der rekombinanten Proteine
- Oligomerisierung und posttranslationale Modifikation
- biologische Aktivität des exprimierten Proteins
Baculovirus-Expressionssystem


Purification of carboxyterminal 6xHis-tagged GFP
Protein by Ni-agarose affinity chromatography About 108 SF9 cells were infected with GFP-expressing
recombinant baculovirus
rGFP-BAC, cells were harvested 4 days p. i. and 6His-GFP was
purified using Ni-agarose. Total yield was approximately 3mg
protein.
1- cell lysate 4- elution 1
2- cleared supernatant 5- elution 2
3- flow trough 6- elution 3
kDa
30
1 2 3 4 5 6
Coomassie-blue stain
Western blot
with a-6His MAb
30

Plaque-Assay mit VSV
0
20
40
60
80
100
120
-1 -2 -3 -4 -5 -6 -7 -8Verdünnung IFN-a
VS
V I
nh
ibie
run
g i
n %
~16kDa
IFN-a-Expression mittels Baculoviren
Klonierung in pFBDhistag
Reinigung rekombinanter Baculoviren (RGS-6HIS)
Proteinreinigung über Ni-NTA (6 HIS)
Antikörperherstellung im Kaninchen
Biologische Wirksamkeit von
IFN-a im VSV-Test
IFN-a Aktivität: 3x106 U/ml
Neutralisierende Wirkung von
anti-IFN-a-Serum im VSV-Test
Serum Verdünnung 1:10 inaktiviert ca.1011
Moleküle IFN-a

Nucleokapside
binden an die
Kernporen.
Im Kern wird
das virale Genom
freigesetzt.
Entnommen aus van Loo et al. (2001). J.Virol. 75, 961-970
Baculovirus Infection of Nondividing Mammalian Cells: Mechanisms of Entry and Nuclear Transport of Capsids.
Umhüllte
Viren werden
via Endocytose
aufgenommen
Rekombiante Baculoviren für die Transduktion von
Säugerzellen (MammBac Technology)

Tn7R
PolH Tn7L
GmR
ApR GFP ORF
MKSV ORF
MCMVie1
DH10Bac E.coli Zelle Helferplasmid
TetR
Bacmid Transposition
Tn7R
PolH Tn7L
GmR
ApR
MCMVie1
Bacmid
mit
Insertion
Bacmid
mit
Insertion
Virusanreicherung in Insektenzellen
PolH Promotor: +++
MCMVie1 Promotor: (+)
Rekombinante Baculoviren
Expression heterologer Gene in Säugerzellen
PolH Promotor: --
MCMVie1 Promotor: +++
Transformation
Isolierung der
rekombinanten Bacmid-
DNA Transfektion der
Bacmid-DNA in
HIGH V Zellen
Transduktion

4. ZUSAMMENFASSUNG

DNA-Viren: Übersichtstabelle
Virusfamilie Parvoviridae Polyomaviridae Papillomaviridae Adenoviridae Poxviridae
Virusgröße 18-26 nm 40-45 nm 55 nm 80-110 nm 300 x 200 x 100 nm
Genom ssDNA, linear dsDNA, zirkulär dsDNA, zirkulär dsDNA, linear dsDNA, linear
Genomlänge 4,8-5,6 kB ca. 5,2 kBp ca. 8 kBp 36-38 kBp 137-360 kBp
Kodierungs-strategie
eine Leserichtung, überlappende ORF
ambisense, überlappende ORF
eine Leserichtung, überlappende ORF
ambisense, überlappende ORF
ambisense, selten überlappende ORF
Hülle keine keine keine keine mehrere Hüllmembranen
Kapsid ikosaedrisch, VP1, VP2, (VP3)
ikosaedrisch, VP1, VP2, VP3
ikosaedrisch, L1, L2
ikosaedrisch, Pentonbasisprotein (pIII), Fiberprotein (pIV), Hexonprotein (pII) u.a.
komplex, über 70 verschiedene virale Proteine (A56R, A4L, L4R, u.a.)
Replikation „rolling hairpin“-Modell bidirektional, semikonservativ
bidirektional, semikonservativ
semikonservativ ähnlich der Parvovirus-Replikation
Replikationsort Zellkern Zellkern Zellkern Zellkern Zytoplasma
Replikations-enzym
zelluläre DNA-Polymerase
zelluläre DNA-Polymerase
zelluläre DNA-Polymerase
virale DNA- Polymerase
virale DNA-Polymerase und weitere Enzyme
Übertragung Tröpfchen, fäkal-oral, vertikal, Blutprodukte
Schmierinfektion Hautkontakt, sexuell, perinatal
Aerosol, fäkal-oral, kontaminierte Gegenstände und Flüssigkeiten
unterschiedliche Übertragungswege (wichtige Zoonoseerreger)
Wirtsspezifität hoch (hoch) hoch niedrig unterschiedlich
Humanpatho-gene Vertreter
Parvovirus B19, Humanes Bocavirus (Parv4)
JCPyV, BKPyV, WU-PyV, KI-PyV, MCPyV und 9 weitere (3.1. 2018)
HPV 1-225 (4.12. 2018)
Arten (Subgenera) A-G , Genotypen (HAdV) 1-90 (7.1.2019)
(Variolavirus), Vacciniavirus, Affen- und Kuhpockenviren, u.a.
Erkrankungen Ringelröteln, Erkrankungen des Respirationstraktes und des Gastro-intestinaltraktes
PML bei HIV-Infektion, Organ-abstoßung nach Nierentransplan-tation
Papillome, Karzinome
Erkältungen und andere Erkrankungen des Respirationstraktes, gastrointestinale Erkran-kungen, Keratokonjunktivitis
Hautläsionen, Hämorrhagien, systemi-sche Erkrankungen, z.T. hohe Lethalität

DANKSAGUNG
Dr. G. Flunker, Greifswald
Dr. S. Eßbauer, München
Dr. G. Keil, Riems
J. Möller, Riems

Vielen Dank für Ihre
Aufmerksamkeit!