Nomenklatur HTL - Wels2004 / 2005 TheorieÜbung 1 H T L - Wels Übung 2 Dipl.-Ing. Dr. Günter...
-
Upload
achmed-amstutz -
Category
Documents
-
view
129 -
download
3
Transcript of Nomenklatur HTL - Wels2004 / 2005 TheorieÜbung 1 H T L - Wels Übung 2 Dipl.-Ing. Dr. Günter...

NomenklaturNomenklatur
HTL - Wels 2004 / 2005
Theorie Übung 1
H T L - Wels
Übung 2

Verb-1-
Verb-H
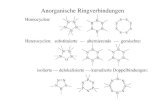
Verbindungen 1. Ordnung
Nomenklatur anorganischer Verbindungen
Verbind. höherer Ordnung
E1 => K+ + e-
Verbindungen mit nur EINATOMIGEN Ionen
E2 + e- => A-
Z
L
L L
L
KK A
E1.....MetalleE2.....Nicht Metalle
K +.....Kationen
A-......Anionen
Z........ZentralatomL.........LigandenK
+.......Kation
Verbindungen mit MEHRATOMIGEN Ionen
Komplexverbindungen

Verb-1-
Verb-H
Verbindungen 1. Ordnung
Nomenklatur anorganischer Verbindungen
Verbindungen höherer Ordnung
Name des Kationsin alphabetischer ReihenfolgeH+ kommt am Ende der Kationen
Anzahl der Liganden in griechischen Zahlwörtern( mono, di, tri, tetra, penta, hexa,.......)
Name der Liganden mit Endung „-o“Sauerstoff : => oxoSchwefel : => thioCyanid: => cyanoChlor: => chloroBrom: => bromo
Chlor => Chlorat
Brom => Bromat
Eisen => Ferrat
Mangan => Manganat
Name des KationDer Name des Kations ist gleich dem Namen des entsprechenden Elements,dh.: das Kation erhält keine Nachsilbe
Name des Anions
Der Name des Anions ist gleich dem Namen des entsprechenden Elements(oder dem griechischen Namen des Elements) mit der Nachsilbe „ -id “
Chlor => Chlorid
Brom => Bromid
Schwefel => Sulfid
Sauerstoff => Oxid
„ - at “ „ - it “Name des Zentralatoms mit der
EndungChlor => Chlorit
Brom => Bromit
Jod => Jodit
Eisen => Ferrit

1
Verbindungen 1.Ordnung
Verb. Höherer Ordnung
Verbindungen mit nur EINATOMIGEN Ionen Verbindungen mit MEHRATOMIGEN Ionen
K a
t i
o n
e n
A n
i o
n e
n
- it - at
- onium
- id
keine zusätzliche Endung
Die Kationen werden gleich wie die Elemente bezeichnet
Charakteristische Namensendungen bei Ionenverbindungen
+ 1 Hypo.......it
+ 3 ..............it
+ 5 .............at + 7 Per.......at
Komplexverbindungen

K a
t i
o n
e n
A n
i o
n e
n
Verbindungen 1.Ordnung
Verbindungen mit nur EINATOMIGEN Ionen Verbindungen mit MEHRATOMIGEN Ionen
1
- it
- at
- onium
Charakteristische Namensendungen bei Ionenverbindungen
- id
A-
K +
Z
L
L L
L
Z
L
L L
L
Verb. Höherer OrdnungKomplexverbindungen
Keine zusätzliche Endung

Verbindungen 1.Ordnung
Verbindungen mit nur EINATOMIGEN Ionen Verbindungen mit MEHRATOMIGEN Ionen
K a
t i
o n
e n
A n
i o
n e
n
1
Charakteristische Namensendungen bei Ionenverbindungen
Cl
-F
- Br
- J
-
O
2- S
2-
Mg
2+Na
+
Fe
3+ Mn
2+
K
+
Co
2+
Oxid, Sulfid
Fluorid, Chlorid, Bromid , Jodid
Eisen, Mangan, Kobalt
Natrium, Kalium, Magnesium
ClO4- NO3
- SO4
2-
SO3
2- NO2- PO3
3-
Sulfit, Nitrit, Phosphit,
Perchlorat, Nitrat, Sulfat
NH4+
PH4+ SH3
+ H3O+
Phosphonium, Sulfonium, Oxonium
Ammonium
Verb. Höherer OrdnungKomplexverbindungen

Vorsilben
Vorsilben
hypo
Die Vorsilbe hypo wird zur Kennzeichnung eines niedrigen
Oxidationszustandes benutzt.
HClO Hypo chlorige Säure
HBrO Hypo bromige Säure
HJO Hypo jodige Säure

Vorsilben
Vorsilben
Per-
Die Vorsilbe Per- ist benutzt worden, um einen höheren Oxidationszustand zu bezeichnen.
Diese Bezeichnung sollte jedoch nur mehr für :
HClO4 Per chlorsäure
HBrO4 Per bromsäure
HJO4 Per jodsäure
HMnO4 Per mangansäure, ....... verwendet werden !
Die Vorsilbe Per- sollte nicht mit der Vorsilbe Per oxo-verwechselt werden.
( = maximaler Oxidationszahl => keine freien Elektronenpaare am Zentralatom)
Achtung:

Vorsilben
Vorsilben
Peroxo-
Die Vorsilbe Peroxo- zeigt in Verbindung mit den Namen (Trivialnamen) einer Säure die Substitution
von -O- durch -O—O- an.
Beispiele:
H2S2O8 Peroxo dischwefelsäure
H2S2O5 Peroxo monoschwefelsäure ( Carosche Säure)
H4P2O8 Peroxo diphosphorsäure

Vorsilben
Die Vorsilben ortho- und meta- sind benutzt worden, um Säuren
zu unterscheiden, die verschiedenen „Wassergehalt“ besitzen.
ortho metaund
( HBO2 )n
Metaborsäure
H3BO3
Orthoborsäure- H2O
( H2SiO3 )n
Metakieselsäure
H4SiO4
Orthokieselsäure- H2O
( HPO3 )n
Metaphosphorsäure
H3PO4
Orthophosphorsäure- H2O

Vorsilben
Vorsilben
pyro
Die Vorsilbe pyro- ist benutzt worden, um eine Säure zu bezeichnen,
die durch Abspaltung eines Wassermoleküls aus zwei Molekülen
Orthosäure entsteht.
Solche Säuren werden jetzt allgemein als die einfachsten Fälle von Isopolysäuren betrachtet.
Für H4P2O7 kann der Trivialname Pyrophosphorsäure verwendet werden,
es wäre jedoch die Bezeichnung DIPHOSPHORSÄURE vorzuziehen.
- H2OP
OH
OH
O
P
OH
HO
O
OP
OH
HO OH
O
P
OH
HO OH
O
+
Pyrophosphorsäure
DIPHOSPHORSÄURE
PhosphorsäurePhosphorsäure +

ONIUM
„ Onium – Ionen “ :
Onium-Ionen sind positiv geladene Ionen (Kationen) die durch eine Reaktioneiner Verbindung mit freien Elektronenpaaren (Lewis Base) mit einer Elektronenacceptor-Verbindung (= Elektrophil oder Lewis Säure) entstehen.
Häufig ist dieser Elektronenacceptor ein Proton ( H+).
Diesem Ion wird die Nachsilbe „-ONIOM “ angehängt !
NR R
R
H
NR R
R
H
ElektronenAcceptor
ElektronenDonator
LewisSäure
LewisBase
„ - onium “
+

ONIUM
Onium – Ionen:
NR R
RH
Amin
+
PR R
RPhosphin
H+
R O
R
Ether
H+
R S
R
ThioetherH+
NR R
R
H
Amm onium
Phosph onium
PR R
R
H
Ox oniumR O
R
H
Sulf onium
R S
R
H

Übung 1

Ü-Plana
r
B
O
O
O
C
O
O
O
N
O
O
O
Nitrat
NO3-
Carbonat
CO3
2 -
Borat
BO3
3 -

Ü
Si O
O
O
O N
O
O
O
N
O
O
P
O
O O
O
Silicat
SiO4
4 -
Nitrat
NO3
-
Phosphat
PO4
3 -
Nitrit
NO2
-

Ü-PO4
Natrium-phosphat
Na3PO4
Phosphorsäure
H3PO4
Natrium-dihydrogen-phosphat
NaH2PO4
Dinatrium-hydrogen-phosphat
Na2HPO4
P
O
O O
O
P
O
O O
O
H
H
H
P
O
O O
O
H
Na
Na
P
O
O O
O
H
H
Na

Ü
S
O
O
OP
O
O O
O
H
H
H
S
O
O O
O
S
O
O S
O
P
O
O
O
Sulfat
SO4
2 -
Thiosulfat
S2O3
2 -
Phosphorsäure
H3PO4
Phosphit
PO3
3 -
Sulphit
SO3
2 -

Chlor
Cl OO
O
O
Cl O
O
O
Cl O
O
Cl O
Cl OO
O
O
H
Cl O
O
O
H
Cl O
O
H
Cl O H
Chlorate
Chlorite
Perchlorate
Hypochlorite
ClO3-
ClO2-
ClO4-
ClO -
Chlorsäure
Chlorige Säure
Per chlorsäure
Hypo chlorige Säure
HClO3
HClO2
HClO4
HClO

Brom
Bromate
Bromite
Per bromate
Hypo bromite
BrO3-
BrO2-
BrO4-
BrO -
Bromsäure
Bromige Säure
Per bromsäure
Hypo bromige Säure
HBrO3
HBrO2
HBrO4
HBrO
Br O
O
Br O
Br
O
O
O
Br O
O
O
O Br O H
O
O
O
Br
O
O
O H
Br
O
O H
Br O H

Jod
J O
J O
O
O
O
J O
O
J O
O
O
J O H
J O H
O
J O H
O
O
O
J O H
O
OJO3
-
JO2-
JO4-
JO -
Jodate
Jodite
Perj odate
Hypo jodite
HJO3
HJO2
HJO4
Jod säure
Jodige Säure
Per jodsäure
Hypo jodige Säure
HJO
freies Elektronenpaar

7-HG-Salze
J O
O
O
O
J O
O
Br O
Br
O
O
O
Cl O
O
O
Cl O
O
Chlorat
ClO3
-
Perjodat
JO4
-
Hypo bromit
BrO
-
Chlorit Jodit
JO2
-ClO2
-Bromat
BrO3
-
7. Hauptgruppe Salze der Sauerstoff - Säuren

7-HG-Säure
n
Chlorsäure
HClO3
Perjodsäure
HJO4
Hypo bromige Säure
HBrO
Chlorige Säure Jodige Säure
HJO2HClO2
Bromsäure
HBrO3
Cl O
O
O
H
Cl O
O
H J O H
O
J O H
O
O
O
Br
O
O
O H
Br O H
7. Hauptgruppe Salze der Sauerstoff - Säuren

Schwefel
Dithionit Dithionat
S
O
O S O
OO
O
S O
O
O
S
O
O
O
O O
S
O
O S O
O
S OO
O
O
O HH
S2O4
2- S2O6
2-
S2O8
2- H2SO5
Peroxidisulfat Carosche Säure

Cr-Mn
S
O
O O
O
Cr
O
O O
O
Mn O
O
O
O
Cl OO
O
O
ClO4-
Per chlorate
Per manganat
MnO4-
Sulfat
SO4
2-
Chromat
CrO4
2-
6. Hauptgruppe
6. Nebengruppe
7. Hauptgruppe
7. Nebengruppe

Chromat
Cr
O
O O
O
Chromat
CrO4
2-
Cr
O
HO OH
O
Cr
O
HO OH
O
Cr
O
OH
O
Cr
O
HO
O
O+
Chromsäure Chromsäure+
- H2O
Cr
O
O
Cr
O
O
O OO
Di chromat
Cr2O7
2-

C
C NO
C NS
C N
Cyanid Cyanat
Thiocyanat
CN-OCN-
SCN-
Rhodanid

Übung 2

Cyanat OCN -
Natriumsulfat Na2SO4
Calciumphosphat Ca3(PO4)2
Salpetersäure HNO3
Schwefelige Säure H2SO3
Kaliumdichromat
Natrium perchlorat NaClO4
K2Cr2O7

Cyanid CN -
Natriumsulfat Na2SO4
Calciumphosphat Ca3(PO4)2
Salpetersäure HNO3
Schwefelige Säure H2SO3
Kaliumdichromat
Natrium perchlorat NaClO4
K2Cr2O7

Cyanat OCN -
Natrium hydrogen carbonat NaHCO3
Calcium chlorid CaCl2
Salpetrige Säure HNO2
Chlorsäure HClO3
Natrium chromat
Ammonium dihydrogen phosphat
Na2CrO4
(NH4)H2PO4

Ü-Liste
Thiocyanat SCN -
Natriumhydrogensulfat NaHSO4
Calcium nitrat Ca(NO3)2
Perchlorsäure HClO4
Salpetrige Säure HNO2
Kalium jodit
Kalium per manganat KMnO4
KJO2
( Rhodanid )

Übersichtleer
Si O
O
O
O
Cl O
O
O
S
O
O O
O
J O
O
O
O
Br O
O
Cl O
Mn O
O
O
O
P
O
O O
O
N
O
O
O
H
N
O
O
Cr
O
O O
O
S
O
O
O H
H
Übung

E N D EE N D E