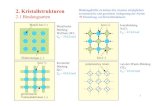
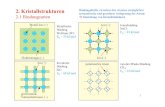
Synthese und Kristallstrukturen von heteronuklearen AgI/FeII-Koordinationspolymeren:...
-
Upload
stefan-gerber -
Category
Documents
-
view
212 -
download
0
Transcript of Synthese und Kristallstrukturen von heteronuklearen AgI/FeII-Koordinationspolymeren:...
Synthese und Kristallstrukturen von heteronuklearen AgI/FeII-Koordinationspolymeren: (Me3PhN)2[Ag2Fe(SCN)6],(Me3PhN)6[Ag6Fe3(ECN)18] (E � S, Se) und (Me3PhN)4[Ag2Fe(SCN)8]
Stefan Gerbera und Harald Krautscheida,*, Thomas Gelbrichb, Heike Vollmerc
a Leipzig, Institut für Anorganische Chemie der Universitätb Southampton/U.K., School of Chemistry, University of Southamptonc Karlsruhe, Institut für Anorganische Chemie der Universität (TH)
Bei der Redaktion eingegangen am 3. Mai 2004.
Professor Joachim Sieler zum 65. Geburtstag gewidmet
Inhaltsübersicht. Bei der Reaktion von AgSCN mit (Me3PhN)3-[Fe(NCS)6] in DMF bilden sich die SCN�-verbrückten, zweidimen-sional polymeren, heteronuklaren Komplexe (Me3PhN)2[Ag2Fe-(SCN)6] (1) und (Me3PhN)6[Ag6Fe3(SCN)18]·CH2Cl2·DMF (2a),während bei Zugabe von (Me3PhN)(SCN) zur Reaktionslösung derkettenförmige Komplex (Me3PhN)4[Ag2Fe(SCN)8] (3) entsteht.Die zu 2a homologe Selenocyanatverbindung 2b konnte ebenfalls
Synthesis and Crystal Structures of Heterometallic AgI/FeII Coordination Polymers:(Me3PhN)2[Ag2Fe(SCN)6], (Me3PhN)6[Ag6Fe3(ECN)18] (E � S, Se) and(Me3PhN)4[Ag2Fe(SCN)8]
Abstract. The reaction of AgSCN with (Me3PhN)3[Fe(NCS)6] inDMF yields two-dimensional polymeric, heteronuclear complexes(Me3PhN)2[Ag2Fe(SCN)6] (1) and (Me3PhN)6[Ag6Fe3(SCN)18] ·CH2Cl2·DMF (2a) with bridging SCN� ligands, whereas additional(Me3PhN)(SCN) leads to (Me3PhN)4[Ag2Fe(SCN)8] (3) with a one-dimensional structure. The selenocyanato complex 2b, homologousto 2a, could also be prepared. Single crystal X-ray structure deter-
Einleitung
Als ambidenter Ligand ist das SCN�-Ion in der Lage, ter-minal oder in verschiedenen verbrückenden Koordinations-modi an Übergangsmetallionen zu binden. Dabei koordi-niert der SCN�-Ligand entsprechend dem HSAB-Konzept[1] über das S-Atom bevorzugt an weiche Lewis-Säuren, mitdem N-Atom bevorzugt an kleinere Metallionen mit höhe-rer Ionenladung [2, 3]. Dementsprechend sind in (Et4N)2-[Ag2Fe(SCN)6], (Bu4N)4[Ag2Fe2(SCN)12] [4] und(C5H6NCO2)2[Ag4Fe2(SCN)12(H2O)2]·2H2O [5] die Ag�-Ionen tetraedrisch an vier S-Atome, die Fe2�- bzw. Fe3�-Ionen oktaedrisch an N-Atome der Thiocyanatoliganden
* Prof. Dr. H. KrautscheidInstitut für Anorganische Chemie der UniversitätJohannisallee 29D-04103 LeipzigFAX: 0341/9736199E-mail: [email protected]
Z. Anorg. Allg. Chem. 2004, 630, 1427�1432 DOI: 10.1002/zaac.200400138 2004 WILEY-VCH Verlag GmbH & Co. KGaA, 69451 Weinheim 1427
erhalten werden. Die Einkristall-Röntgenstrukturanalysen zeigen,dass die Ag�-Ionen in 1 und 2a tetraedrisch von vier S-Atomen,in 3 von einem N- und drei S-Atomen der verbrückenden SCN�-Liganden koordiniert sind, an die Fe2�-Ionen binden die SCN�-bzw. SeCN�-Liganden stets über die N-Atome in oktaedrischerAnordnung.
minations show, that the Ag� ions in 1 and 2a are coordinatedtetrahedrally by four S atoms, in 3 by one N and three S atoms ofthe bridging SCN� ligands; six N atoms of the SCN� or SeCN�
ligands bind to Fe2� in an octahedral arrangement.
Keywords: Coordination polymers; Crystal structures; Packingsimilarity; Polynuclear complexes; Thiocyanates
gebunden. Um zu untersuchen, ob das Gegenion einenstrukturbestimmenden Einfluss auf die Anionenstrukturausübt, wie es bei der Bildung von oligo- und polynukle-aren Halogenometallaten der schweren Hauptgruppenele-mente zu beobachten ist [6, 7], haben wir (Me3PhN)3-[Fe(SCN)6] bzw. (Me3PhN)4[Fe(SCN)6] mit AgSCN umge-setzt und berichten hier über die Kristallstrukturen von(Me3PhN)2[Ag2Fe(SCN)6] (1), (Me3PhN)6[Ag6Fe3(SCN)18]· DMF·CH2Cl2 (2a), (Me3PhN)4[Ag2Fe(SCN)8] (3) sowieüber den zu 2a homologen Selenocyanatokomplex(Me3PhN)6[Ag6Fe3(SeCN)18]·2CH2Cl2 (2b).
Ergebnisse und Diskussion
Die Verbindungen 1 und 2 kristallisieren aus der Reaktions-lösung (DMF) nach Überschichten mit Diethylether bzw.nach Einkondensieren von CH2Cl2. 3 bildet sich in Gegen-wart einer höheren Konzentration an (Me3PhN)SCN bzw.bei Verwendung von (Me3PhN)4[Fe(SCN)6] als Ausgangs-stoff (Schema 1).
S. Gerber, H. Krautscheid, T. Gelbrich, H. Vollmer
Schema 1
1 kristallisiert monoklin in der Raumgruppe C2/c, wobeisich die Fe-Atome auf den zweizähligen Drehachsen befin-den. Entlang der 21-Schraubenachsen bilden die Ag�-Ionenzusammen mit den über die S-Atome S1 gebundenenSCN�-Ionen zickzackförmige Ag(SCN)-Stränge (Abbil-dung 1). Zwei weitere SCN�-Liganden vervollständigen dietetraedrische Umgebung der Ag�-Ionen. Die N-Atome derThiocyanatoliganden koordinieren an die Fe2�-Ionen, diedadurch die Ag-SCN-Stränge zu zweidimensionalen Netzenin der ab-Ebene verknüpfen.
In der Anionenstruktur von 1 binden jeweils ein 1,1,3-µ3-und zwei 1,3-µ2-verbrückende SCN�-Liganden aus einemAg(SCN)-Strang an ein Fe2�-Ion. Durch die Koordinationder symmetrieäquivalenten SCN�-Ionen erhalten die Fe2�-Ionen oktaedrische Umgebung (Fe�N 213,4-220,0(5) pm;N�Fe�N 85,9-95,2 und 172,8-178,5(3)°).
Die Ag�-Ionen in 1 sind tetraedrisch koordiniert, wobeidie Ag�µ2-S-Abstände mit 250,8 und 257,9(2) pm erwar-tungsgemäß kürzer sind als die Ag�µ3-S-Abstände (262,2bzw. 276,6(2) pm). Die Verknüpfung der AgS4-Tetraederüber gemeinsame Ecken zu Tetraedersträngen erinnert an“Zweiereinfachketten“, wie sie auch in der Strukturchemieder Silicate bei den Pyroxenen bekannt sind [8]. In der or-thorhombischen Modifikation des AgSCN sind die Ag�-Ionen ebenfalls tetraedrisch von verbrückenden SCN�-Io-nen koordiniert, im Unterschied zu 1 binden jeweils nur dreiLiganden über die S-Atome, die vierte SCN-Gruppe überdas N-Atom [9]. Im monoklinen AgSCN wird etwa lineareKoordination durch 1,3-µ2-SCN�-Ionen beobachtet, wobeijeweils zwei zusätzliche Ag···S-Wechselwirkungen mit deut-lich größerem Abstand auftreten [10].
2a kristallisiert triklin in der Raumgruppe P1̄ mit zweiFormeleinheiten (Me3PhN)6[Ag6Fe3(SCN)18] · DMF ·CH2Cl2 pro Elementarzelle. Wie in 1 sind auch in 2a dieAg�-Ionen tetraedrisch über S-Atome koordiniert; an jedesder drei kristallographisch unabhängigen Fe2�-Ionen bin-den vier 1,3-µ2- und zwei 1,1,3-µ3-SCN�-Liganden über dieN-Atome (Abbildung 2). Im Unterschied zu 1 sind dieAg�-Ionen in 2a paarweise zu Ag2(SCN)6-Bitetraedernangeordnet, wie sie als diskrete Anionen auch inK4[Ag2(SCN)6] und Cs4[Ag2(SCN)6] [11] nachgewiesen wur-den. Die Verknüpfung dieser Ag2(SCN)6-Bitetraeder überFe2�-Ionen ähnelt dem Verknüpfungsmuster in den linea-ren Anionensträngen von (Et4N)2[Ag2Fe(SCN)6] [4], wobeiin 2a die Verknüpfung zu cyclischen Anordnungen von je-weils drei Ag2(SCN)6-Bitetraedern und drei Fe(NCS)6-Ok-taedern führt. Wie in Abbildung 2 dargestellt, koordinieren
2004 WILEY-VCH Verlag GmbH & Co. KGaA, 69451 Weinheim zaac.wiley-vch.de Z. Anorg. Allg. Chem. 2004, 630, 1427�14321428
Abb. 1 Ausschnitte aus dem zweidimensionalen, anionischenNetzwerk in 1 (oben: ORTEP-Darstellung mit 70 %-Ellipsoiden,Blick entlang der kristallographischen c-Achse).Abstände und Winkel:Ag�S1 262,2(2); Ag�S2 257,9(2); Ag�S3 250,7(2); Ag�S1� 276,6(2);Fe�N1 220,0(5); Fe�N2 213,2(5); Fe�N3 215,1(6); S1�C1 165,4(6);C1�N1 115,6(7) pm; S�Ag�S 105,14-115,63(6); Ag�S�Ag 156,04(7);N�Fe�N 85,9-95,2 und 172,8-178,5(3); Ag�S�C 93,7-104,2(2); Fe�N�C144,8-159,2(5); S�C�N 177,0-179,5(6)°.
drei der 1,1,3-µ3-verbrückenden Liganden (Thiocyanatio-nen mit S2, S4 und S6) an die Fe-Atome innerhalb einessolchen Ringes; drei weitere 1,1,3-µ3-Liganden (Thiocyana-tionen mit S1, S3 und S5) binden über die N-Atome (N1�,N3�, N5�) an Fe-Atome von drei benachbarten[Ag6Fe3(SCN)18]6�-Ringen. Zusammen mit den symmetrie-äquivalenten Liganden (Thiocyanationen mit N1, N3 undN5) verknüpfen damit 1,1,3-µ3-SCN�-Liganden jeden[Ag6Fe3(SCN)18]6�-Ring mit sechs weiteren Ringen. MitWinkelsummen von 346,5 bis 354,5° sind die zentralenAg2S2-Vierringe der Ag2(SCN)6-Bitetraeder um 26,91 bis37,22(6)° gefaltet. Die Ag�S-Abstände der µ3-Liganden be-tragen 257,0 bis 280,2(1) pm (Mittelwert 267,7 pm), die der
Synthese und Kristallstrukturen von heteronuklearen AgI/FeII-Koordinationspolymeren
Abb. 2 Struktur eines [Ag6Fe3(SCN)18]6�-Ringes in 2a. Blick etwaentlang der kristallographischen c-Achse.Ausgewählte Abstände und Winkel:Ag1�S1 263,5; Ag1�S2 263,9; Ag1�S7 261,5; Ag1�S9 250,0; Ag2�S1276,6; Ag2�S2 266,9; Ag5�S5 310,6; Ag5�S6 257,0; Ag5�S15 250,2;Ag5�S17 246,0(1); Fe1�N2 215,7; Fe1�N5 217,0; Fe1�N9 217,6;Fe1�N10 217,9; Fe1�N11 214,4; Fe1�N12 214,5(4) pm; S1�Ag1�S293,62; S1�Ag1�S7 105,57; S1�Ag1�S9 116,79; S7�Ag1�S9 103,38;S2�Ag1�S9 125,47; S1�Ag2�S2 90,03; S6�Ag5�S15 108,39;S6�Ag5�S17 125,47; S15�Ag5�S17 119,45; Ag1�S1�Ag2 80,56(4);Ag1�S1�C1 112,6; Ag2�S1�C1 106,9(2); N2�Fe1�N5 175,33;N2�Fe1�N9 84,75; N2�Fe1�N10 85,76; N5�Fe1�N9 90,64(2);Fe1�N2�C2 154,2(4); S1�C1�N1� 176,3(4)°.
µ2-verbrückenden Liganden 250,0 bis 261,5(2) pm (Mittel-wert 254,2 pm). Eine Ausnahme stellt der Abstand Ag5···S5dar, der mit 310,6(2) pm deutlich von den anderen Ag�S-Bindungslängen abweicht. Gleichzeitig sind die AbständeAg5�S6 (257,0(1)), Ag5�S15 und Ag5�S17 verkürzt unddas Atom Ag5 ist etwa planar koordiniert (Winkelsumme353,3°).
Die Me3PhN�-Ionen und die mitkristallisierenden Lö-sungsmittelmoleküle befinden sich teilweise zwischen denAnionenschichten, zum Teil ragen sie in die Hohlräume desAnionennetzes hinein und führen offensichtlich dadurch zueiner Kristallstruktur (Abbildung 3), die sich bei gleicherZusammensetzung (R4N)2[Ag2Fe(SCN)6] von der von 1und der von (Et4N)2[Ag2Fe(SCN)6] [4] unterscheidet.
Die zu 2a homologe Selenocyanatverbindung(Me3PhN)6[Ag6Fe3(SeCN)18]·2CH2Cl2 (2b) kristallisiert wie2a triklin mit ähnlichen Gitterparametern a, b, c und γ;allerdings unterscheiden sich die Winkel � und β der beidenVerbindungen signifikant. In beiden Verbindungen liegenentsprechend der angenäherten 3/m-Symmetrie der anioni-schen Netze in der ab-Ebene, die mit a � b und γ � 60°zum Ausdruck kommt, drei etwa gleich lange Translations-vektoren vor, die jeweils einen Winkel von etwa 60° ein-schließen. Da 2a und 2b gleichzeitig sehr ähnliche Anionen-teilstrukturen der [Ag6Fe3(ECN)18]6�-Netze aufweisen, ha-ben wir die beiden Kristallstrukturen mit Hilfe des Pro-grammes XPac [12] auf Packungsähnlichkeit untersucht.Dazu wurden als korrespondierende Punkte die Fe-Atomein 2a sowie drei an diese gebundene N-Atome (N1, N3, N5)
Z. Anorg. Allg. Chem. 2004, 630, 1427�1432 zaac.wiley-vch.de 2004 WILEY-VCH Verlag GmbH & Co. KGaA, 69451 Weinheim 1429
Abb. 3 Ausschnitt aus der Anionenstruktur von 2a, Blickrichtungetwa entlang der kristallographischen c-Achse. Die FeN6-Oktaedersind blau, die Ag2S6-Bitetraeder hellrot dargestellt.
ausgewählt und mit den möglichen Kombinationen von Po-sitionen entsprechender Atome in 2b verglichen. Die Vekto-ren zwischen den gewählten Atomen zeigen gute Überein-stimmung, wenn den Atompositionen von Fe1, Fe2, Fe3,N5, N1, N3 in 2a die der entsprechenden Atome in 2b ge-genübergestellt werden. Die Anionenstruktur von 2b ent-spricht auch bezüglich der Atomkoordinaten der von 2a,wenn die Elementarzelle von 2b mit der Matrix T transfor-miert wird.
T � �1̄ 0 01̄ 1 00 0 1̄�
Die ursprünglichen Elementarzellen sowie die transfor-mierte Elementarzelle von 2b sind in Tabelle 1 angegeben.Die a-Achsen beider Strukturen sind bis auf den Vor-zeichenunterschied äquivalent, der b-Achse in 2a entsprichtdie Flächendiagonale [1̄10] in 2b. Abbildung 4 zeigt dieÜbereinstimmung der Anionenstrukturen von 2a und 2b alsleast-squares-Anpassung. Aufgrund der vergleichbarenLage der Inversionszentren besteht das Konstrukt 1 auseiner inversionssymmetrischen Anionen-Doppelschicht, diesich in der ab-Ebene erstreckt und in beiden Strukturenkristallographisch gleich orientiert ist. Längendifferenzen inden korrespondierenden Paaren von Basisvektoren von 54,7bzw. 43,4 pm sind das Resultat der unterschiedlichenRadien von S und Se.
Eine weitere XPac-Analyse, durchgeführt für die sechsunabhängigen Me3PhN�-Ionen, ergibt ein weiteres Kon-strukt 2, in welches vier Kationen involviert sind, deren Pa-ckungsähnlichkeit ebenfalls durch eine least-squares-Anpas-sung bestätigt wird. Tatsächlich bilden diese vier unabhän-
S. Gerber, H. Krautscheid, T. Gelbrich, H. Vollmer
Tabelle 1 Die Transformation der Elementarzelle von 2b mit derMatrix T führt zu einer Aufstellung 2b, transf., in der die Atomedes Konstruktes 1 ebenso angeordnet sind wie in 2a.
2a 2b, transf. 2b, orig.
a /pm 1634,9 1689,6 1689,6b /pm 1690,7 1734,1 1718,1c /pm 2250,6 2382,6 2382,6� /° 88,90 76,81 71,80β /° 88,30 94,78 85,22γ /° 61,38 60,23 61,17
Abb. 4 Least-squares-Fit der beiden Instanzen des supramolekul-aren Konstruktes 1 (Ausschnitt mit neun symmetriegeneriertenEinheiten und Zentraleinheit) an allen äquivalenten Fe Atomen(punktierte Linien: 2b).
gigen Kationen (2a: Me3PhN� mit N20, N30, N40, N60)mit den Anionen-Doppelschichten eine gemeinsameBaueinheit, in der die beiden Anionenschichten die vier Ka-tionen einschließen. Sowohl 2a als auch 2b basieren auf die-sen Einheiten. Die grundlegende Differenz zwischen 2a und2b besteht in der Art und Weise, wie diese sehr ähnlichen,inversionssymmetrischen Anionen-Doppelschichten inner-halb der jeweiligen Struktur gestapelt werden. Die Stapel-richtung entspricht der c-Achse, die im Fall von 2a etwa dieEbenennormale darstellt. Daraus folgt, dass � und β in 2anahe 90° sind (88.90° bzw. 88.30°). Im Unterschied dazuerfolgt die Stapelung der Doppelschichten in 2b mit einersignifikanten Verschiebung; Stapelrichtung und Ebenennor-male weichen deutlich voneinander ab (Abbildung 5). Dieentsprechenden Winkel in 2b betragen 76.81° und 95.78°(Tabelle 1). Infolgedessen ordnen sich die beiden restlichenMe3PhN�-Kationen sowie die mitkristallisierenden Lö-sungsmittelmoleküle (violett dargestellt in Abbildung 5) in2a und 2b unterschiedlich an.
Verbindung 3 bildet sich, wenn die Umsetzung von(Me3PhN)3[FeIII(SCN)6] mit AgSCN in DMF in Anwesen-heit von (Me3PhN)(SCN) durchgeführt wird oder wenn(Me3PhN)4[FeII(SCN)6] mit AgSCN im Verhältnis 1:1 um-gesetzt und das Reaktionsprodukt durch Einkondensierenvon CH2Cl2 auskristallisiert wird. Während bei der Syn-these von 1 und 2a Fe3� zu Fe2� reduziert wird [13], führtdie Verwendung von (Me3PhN)4[FeII(SCN)6] als Ausgangs-stoff offensichtlich aufgrund der höheren (Me3PhN)�-Kon-zentration zur (Me3PhN)�-reicheren Verbindung 3.
2004 WILEY-VCH Verlag GmbH & Co. KGaA, 69451 Weinheim zaac.wiley-vch.de Z. Anorg. Allg. Chem. 2004, 630, 1427�14321430
Im Unterschied zu 1 und 2a, in denen die Ag�-Ionenausschließlich an S-Atome der SCN�-Liganden binden,werden in 3 die Ag�-Ionen über 1,3-µ2-SCN�-Liganden(S1-C1-N1) zu Ag2(SCN)2-Achtringen verbrückt. Jeweilszwei weitere, S-gebundene SCN�-Ionen vervollständigendie tetraedrische Koordination der Ag�-Ionen unter Bil-dung von [Ag2(SCN)6]4�-Einheiten, die auch in der Kri-stallstruktur des orthorhombischen AgSCN [9] auftreten,und verknüpfen gleichzeitig als 1,3-µ2-Liganden mit denFe2�-Ionen. Dadurch entstehen polymere, anionischeStränge, die entlang der kristallographischen c-Achse ver-laufen (Abbildung 6). Die Fe2�-Ionen, die sich auf Inver-sionszentren befinden, werden durch zwei zueinander trans-ständige, terminale NCS�-Liganden (N4-C4-S4) koordina-tiv abgesättigt. Die Fe�N-Abstände zu den verbrückendenNCS�-Liganden sind mit 216,3 und 221,0(3) pm etwas län-ger als zu den terminalen Liganden (Fe�N4 212,5(3) pm).Die terminalen Liganden sind etwa linear angeordnet(Fe�N4�C4 169,3(3)°), in den FeAg(SCN)2-Achtringenbeobachtet man mit Fe�N�C-Bindungswinkeln von 146,6bzw. 154,8(3)° eine deutliche Abweichung von der linearenAnordnung. Im Vergleich dazu betragen die Fe�N-Ab-stände im homoleptischen Komplex (Et4N)4[Fe(NCS)6]216,8 bis 218,9 pm, die Bindungswinkel Fe�N�C 163,1 bis177,4° [4]. Die Ag�S-Abstände für die 1,3-µ2-verbrücken-den Thiocyanationen liegen im Bereich von 253,6 bis261,0(1) pm.
Im Infrarotspektrum von 3 sind zwei intensive Bandender C�N-Streckschwingungen νCN bei 2081 und 2105 cm�1
sowie zwei schwache Deformationsbanden (δSCN: 475 und462 cm�1) zu erkennen, die den terminalen bzw. ver-brückend koordinierenden SCN�-Liganden zugeordnetwerden können. Die Banden der S�C-Streckschwingungen(νSC) sind schwach und aufgrund der Überlagerung mitBanden der Kationen nicht zuverlässig zuzuordnen [14].
Experimentelles
Darstellung von 1. In 5 ml DMF werden 0,41 g (0,50 mmol)(Me3PhN)3[Fe(SCN)6] und 0,25 g (1,50 mmol) AgSCN suspendiertund 12 h gerührt. Danach wird vom unlöslichen Feststoff abfiltriertund in die Lösung werden im Verlauf einiger Tage 20 ml Diethyl-ether einkondensiert. Dabei bilden sich farblose Kristalle von 1.
Darstellung von 2a. In 5 ml DMF werden 0,21 g (0,26 mmol)(Me3PhN)3[Fe(SCN)6] und 43 mg (0,26 mmol) AgSCN gelöst. Indie rote Lösung werden innerhalb mehrerer Tage 40 ml CH2Cl2einkondensiert. Dabei wachsen farblose, dünne Plättchen von 2a.Die Kristalle werden isoliert, mit Dichlormethan gewaschen undim Vakuum getrocknet. Ausbeute 25 mg (22 %). Elementaranalyse(berechnet für C72H84N24Ag6Fe3S18): C 32,3 (32,3), H 3,6 (3,2), N12,3 (12,6) %.
Darstellung von 2b. In 5 ml DMF werden 0,26 g (0,50 mmol)Fe(ClO4)3·9H2O, 0,48 g (2,0 mmol) (Me3PhN)SeCN und 0,42 g(2,0 mmol) AgSeCN gelöst. Nach 5 h Rühren wird vom weißen,ungelösten Feststoff abpipettiert und innerhalb weniger Tage wer-den 40 ml CH2Cl2 einkondensiert. Dabei fällt ein rotbraunes Pulveraus, neben dem farblose Plättchen von 2b wachsen. Ausbeute ca.160 mg (27 %).
Synthese und Kristallstrukturen von heteronuklearen AgI/FeII-Koordinationspolymeren
Abb. 5 Die relativen Positionen der Rahmen innerhalb einer Struktur zeigen den unterschiedlichen Verschiebungsbetrag zwischen denDoppelschichten in 2a bzw. 2b.
Abb. 6 Ausschnitt aus dem polymeren 1�[Ag2Fe(SCN)8]4�-Anion in 3. (ORTEP-Darstellung mit 70 %-Ellipsoiden). Ausgewählte Abstände
und Winkel:Ag�S1 261,03(9); Ag�S2 253,6(1); Ag�S3 257,0(1); Ag�N1� 234,6(3); Fe�N2 221,0(3); Fe�N3 216,3(3); Fe�N4 212,5(3) pm; S1�Ag�S2 118,77(4);S1�Ag�S3 105,10(3); S2�Ag�S3 119,51(3); N1��Ag�S1 97,15(8); N1��Ag�S2 106,08(9); N1��Ag�S3 107,5(1); Ag�S1�C1 97,43(12); Ag�S2�C2104,79(12); Ag�N1��C1� 154,3(3); Fe�N2�C2 146,6(3); Fe�N3�C3 154,8(3); Fe�N4�C4 169,3(3)°.
Darstellung von 3. In 5 ml DMF werden 0,50 g (0,53 mmol)(Me3PhN)4[Fe(SCN)6] und 88 mg (0,53 mmol) AgSCN suspendiertund 12 h gerührt. Danach wird vom unlöslichen Feststoff abfiltriert
Z. Anorg. Allg. Chem. 2004, 630, 1427�1432 zaac.wiley-vch.de 2004 WILEY-VCH Verlag GmbH & Co. KGaA, 69451 Weinheim 1431
und in die Lösung wird Dichlormethan einkondensiert. Es bildetsich ein Öl, die überstehende Lösung wird abpipettiert underneut Dichlormethan einkondensiert. Nach wenigen Tagen bilden
S. Gerber, H. Krautscheid, T. Gelbrich, H. Vollmer
Tabelle 2 Daten zu den Kristallstrukturanalysen von 1-3.
1 2a 2b 3
Summenformel C24H28Ag2FeN8S6 C72H84Ag6Fe3N24S18 ·CH2Cl2·DMF C72H84Ag6Fe3N24 Se18·2CH2Cl2 C44H56Ag2FeN12S8
Formelmasse/g·mol�1 892,49 2835,50 3691,53 1281,08Diffraktometer STOE STADI IV STOE IPDS STOE IPDS STOE IPDSMesstemperatur/K 210(2) 200(2) 200(2) 210(2)Kristallgröße/mm3 0,12�0,15�0,18 0,03�0,30�0,44 0,02�0,30�0,50 0,12�0,18�0,24Kristallsystem monoklin triklin triklin monoklinRaumgruppe C2/c (Nr. 15) P1̄ (Nr. 2) P1̄ (Nr. 2) P21/n (Nr. 14)Elementarzelle a/pm 1853,2(2) 1634,9(1) 1687,5(1) 1632,98(8)
b/pm 887,0(1) 1690,7(1) 1717,1(1) 1175,31(7)c/pm 2140,1(2) 2250,6(2) 2382,9(2) 1660,78(8)�/° 90 88,895(9) 71,59(1) 90β/° 103,017(9) 88,302(9) 85,18(1) 118,819(5)γ/° 90 61,383(8) 61,14(1) 90V/106 pm3 3427,5(6) 5458,5(7) 5718,2(7) 2792,7(3)
Z 4 2 2 2Röntgenogr. Dichte/g·cm�3 1,730 1,725 2,144 1,523µ/mm�1 1,943 1,884 7,243 1,292Meßbereich 2θ /° 3,9-47,0 4,5-48,2 4,0-45,0 4,4-48,0Gemessene Reflexe 4066 23528 25001 16081Unabhängige Reflexe [Rint] 2533 [0,0278] 15477 [0,0385] 14110 [0,048] 4313 [0,0359]Unabh. Reflexe mit I > 2σ(I) 2042 12009 10708 3626Parameter 190 1193 1013 304R1 [I > 2σ(I)] 0,0441 0,0381 0,0662 0,0345wR2 [alle Reflexe] 0,1015 0,0998 0,186 0,0997Max./min. Restelektronendichte/ 2,29 / �1,57 1,32 / �1,13 3,14 / �2,09 0,74 / �0,3910�6 e·pm�3
sich farblose Kristalle von 3. Für die Elementaranalyse und dasIR-Spektrum werden die Kristalle abfiltriert, mehrmals mit Pentangewaschen und anschließend im Vakuum getrocknet. Ausbeute0,145 g (43 %). Verbindung 3 entsteht ebenfalls, wenn die Synthesevon 2a durch Zugabe von zwei Äquivalenten (Me3PhN)SCN modi-fiziert wird. Elementaranalyse (berechnet für C44H56Ag2FeN12S8):C 41,1 (41,3), H 4,6 (4,4) N 13,1 (13,1) %.IR-Daten (KBr-Verreibung): νCN 2105(s), 2081(s), δSCN 475(sh),462(vw) cm�1.
Kristallstrukturuntersuchungen
Die Datensammlungen zu den Kristallstrukturanalysen von 1�3wurden auf Diffraktometern des Typs STOE STADI IV (1) undSTOE IPDS (2a, 2b und 3) unter Verwendung von Mo-Kα-Strah-lung (Graphitmonochromator) durchgeführt. Wasserstoffatomla-gen wurden für idealisierte Positionen berechnet. Verwendete Pro-gramme: SHELX-97 [15], DIAMOND2 [16]. Die Daten zu den Kri-stallstrukturanalysen sind in Tabelle 2 zusammengefasst, weitereEinzelheiten zu den Strukturanalysen von 1�3 können beim Cam-bridge Crystallographic Data Centre unter Angabe der Hinterle-gungsnummern CCDC 236982 bis 236985 angefordert werden.
Wir danken der Deutschen Forschungsgemeinschaft und demFonds der Chemischen Industrie für die finanzielle Unterstützungund dem Karl-Winnacker-Fonds für ein Stipendium (HK).
Literatur
[1] R. G. Pearson, J. Am. Chem. Soc. 1963, 85, 3533; M. K. Kroe-ger, R. S. Drago, J. Am. Chem. Soc. 1981, 103, 3250.
[2] J. Burmeister, Coord. Chem. Rev. 1966, 1, 205; 1968, 3, 225;1990, 105, 77.
[3] P. P. Singh, Coord. Chem. Rev. 1980, 32, 33.
2004 WILEY-VCH Verlag GmbH & Co. KGaA, 69451 Weinheim zaac.wiley-vch.de Z. Anorg. Allg. Chem. 2004, 630, 1427�14321432
[4] H. Krautscheid, S. Gerber, Z. Anorg. Allg. Chem. 1999, 625,2041.
[5] X.-L. Li, M.-L. Tong, D.-Z. Niu, J.-T. Chen, Chin. J. Chem.2004, 22, 64.
[6] C. Lode, H. Krautscheid, Z. Anorg. Allg. Chem. 2000, 626,326; 2001, 627, 1454; H. Krautscheid, F. Vielsack, J. Chem.Soc., Dalton Trans., 1999, 2731; H. Krautscheid, C. Lode, F.Vielsack, H. Vollmer, J. Chem. Soc., Dalton Trans. 2001, 1099;H. Gröger, C. Lode, H. Vollmer, H. Krautscheid, S. Lebedkin,Z. Anorg. Allg. Chem. 2002, 628, 57.
[7] G. A. Fisher, N. C. Norman, Adv. Inorg. Chem. 1994, 41, 233.[8] F. Liebau, Structural Chemistry of Silicates: Structure, Bon-
ding, and Classification, Springer-Verlag, Berlin, 1985.[9] D. L. Smith, J. E. Maskasky, L. R. Spaulding, J. Appl. Crystal-
logr. 1982, 15, 48.[10] I. Lindqvist, Acta Crystallogr. 1957, 10, 29; H. -L. Zhu, G.-F.
Liu, F.-J. Meng, Z. Kristallogr. � New Cryst. Struct. 2003,218, 263.
[11] H. Krautscheid, S. Gerber, Acta Crystallogr. 2001, C57, 781;G. Thiele, W. Kehr, Z. Anorg. Allg. Chem. 1984, 515, 199.
[12] T. Gelbrich, XPac. A program for the analyis of packing simi-larity in crystal structures. University of Southampton, Ver-sion 1.1, 2003.
[13] E. Itabashi, Inorg. Chem. 1985, 24, 4024; D. Rehorek, E. G.Janzen, Inorg. Chim. Acta 1986, 118, L29.
[14] R. A. Bailey, S. L. Kozak, T. W. Michelsen, W. N. Mills, Coord.Chem. Rev. 1971, 6, 407; A. H. Norbury, Adv. Inorg. Chem.Radiochem. 1975, 17, 231; A. Tramer, J. Chim. Phys. Chim.Biol. 1962, 59, 232; R. H. Toeniskoetter, S. Solomon, Inorg.Chem. 1968, 7, 617.
[15] G. M. Sheldrick, SHELX-97 � Programme zur Bestimmungvon Kristallstrukturen, Göttingen, 1997.
[16] K. Brandenburg, DIAMOND2, Crystal Impact GbR, Bonn,1998.
![Page 1: Synthese und Kristallstrukturen von heteronuklearen AgI/FeII-Koordinationspolymeren: (Me3PhN)2[Ag2Fe(SCN)6], (Me3PhN)6[Ag6Fe3(ECN)18] (E = S, Se) und (Me3PhN)4[Ag2Fe(SCN)8]](https://reader042.fdokument.com/reader042/viewer/2022020517/575025c11a28ab877eb5634c/html5/thumbnails/1.jpg)
![Page 2: Synthese und Kristallstrukturen von heteronuklearen AgI/FeII-Koordinationspolymeren: (Me3PhN)2[Ag2Fe(SCN)6], (Me3PhN)6[Ag6Fe3(ECN)18] (E = S, Se) und (Me3PhN)4[Ag2Fe(SCN)8]](https://reader042.fdokument.com/reader042/viewer/2022020517/575025c11a28ab877eb5634c/html5/thumbnails/2.jpg)
![Page 3: Synthese und Kristallstrukturen von heteronuklearen AgI/FeII-Koordinationspolymeren: (Me3PhN)2[Ag2Fe(SCN)6], (Me3PhN)6[Ag6Fe3(ECN)18] (E = S, Se) und (Me3PhN)4[Ag2Fe(SCN)8]](https://reader042.fdokument.com/reader042/viewer/2022020517/575025c11a28ab877eb5634c/html5/thumbnails/3.jpg)
![Page 4: Synthese und Kristallstrukturen von heteronuklearen AgI/FeII-Koordinationspolymeren: (Me3PhN)2[Ag2Fe(SCN)6], (Me3PhN)6[Ag6Fe3(ECN)18] (E = S, Se) und (Me3PhN)4[Ag2Fe(SCN)8]](https://reader042.fdokument.com/reader042/viewer/2022020517/575025c11a28ab877eb5634c/html5/thumbnails/4.jpg)
![Page 5: Synthese und Kristallstrukturen von heteronuklearen AgI/FeII-Koordinationspolymeren: (Me3PhN)2[Ag2Fe(SCN)6], (Me3PhN)6[Ag6Fe3(ECN)18] (E = S, Se) und (Me3PhN)4[Ag2Fe(SCN)8]](https://reader042.fdokument.com/reader042/viewer/2022020517/575025c11a28ab877eb5634c/html5/thumbnails/5.jpg)
![Page 6: Synthese und Kristallstrukturen von heteronuklearen AgI/FeII-Koordinationspolymeren: (Me3PhN)2[Ag2Fe(SCN)6], (Me3PhN)6[Ag6Fe3(ECN)18] (E = S, Se) und (Me3PhN)4[Ag2Fe(SCN)8]](https://reader042.fdokument.com/reader042/viewer/2022020517/575025c11a28ab877eb5634c/html5/thumbnails/6.jpg)